Актуальность. Отсутствие этиотропного лечения инфекционных заболеваний, вызванных опасными антибиотикорезистентными патогенами, частые случаи развития гипериммунных реакций и осложнений на фоне приёма дорогостоящих препаратов с огромным перечнем противопоказаний, отсутствие патогенетически обоснованного консервативного лечения онкобольных, свидетельствуют о том, что поиск альтернативных препаратов в стратегии консервативного лечения многих заболеваний на современном этапе является наиболее актуальным [10, 22].
Изучение противомикробных веществ в настоящее время является одним из самых новых направлений исследований. Известно, что hydrogen peroxide убивает бактерии, предотвращает заболевание десен и образование зубного налета. Исследования показали, что сифилис, кандидоз и различные вирусные инфекции поддаются лечению перекисью водорода. Эмпирически применяют пероксид и при инсультах/инфарктах, а также эндокринной патологии.
Известно, что перекись водорода необходима для образования гормоноподобных веществ – простагландинов, которые регулируют энергетический обмен в организме. Под воздействием витамина С образуется дополнительное количество перекиси, которая, в свою очередь, активирует синтез простагландинов [5, 19]. Тем не менее, отсутствие принципов применения hydrogen peroxide терапии, а также незнание потенциальных осложнений и известные случаи эмболии с последующим применением интубации, диктуют разработку стратегии в дозировке препарата и выявления механизмов его воздействия на клетки для адекватного патогенетически обоснованного лечения, профилактики, реабилитации.
Токсикокинетика и токсикодинамика hydrogen peroxide практически не изучена [1, 6]. Тем не менее, имеющиеся немногочисленные исследования на мышах и птицах, а также клеточных культурах человека свидетельствуют о несомненных перспективах применения hydrogen peroxide в медицинской практике, что и явилось основанием для выбора нами направления исследований [20].
Цель исследования. Систематизация имеющихся данных о возможных механизмах биологического воздействия hydrogen peroxide на клетки организма человека в условиях различной патологии.
Задачами исследования явилось проведение анализа механизмов воздействия hydrogen peroxide на клетки в условиях ишемии и микробной контаминации.
Материалы и методы исследования
Материал для патоморфологических исследований получен в соответствии с приказом Минздравмедпрома РФ от 29.04.94 N 82 «О порядке проведения патологоанатомических вскрытий». Забор материала производился через сутки после клинической смерти, всего изучено 52 биопсии. В работе использован трупный материал мозга человека в период с сентября 2013 по февраль 2015 г.) с диагнозом – инсульт, инфаркт (25/27), который распределили с учётом возраста и пола. Выбор участков забора биоптатов основывался на том, что одними из регуляторов артериального давления (АД) являются паравентрикулярные нейросекреторные ядра гипоталамуса, участвующие в выработке АДГ (антидиуретического гормона) – вазопрессина. Биопсийный материал гипоталамуса фиксировался по прописи для подготовки к иммуногистохимическим исследованиям сразу после забора. Исключение возможных артефактов основано на данных, полученных при специальном исследовании на собаках, свидетельствующих, что при сохранении трупов при температуре 7°С до 4–6 часов в морфологии гипоталамо-гипофизарной нейросекреторной системы микроскопически видимых изменений не наблюдается, кроме некоторого снижения интенсивности специфических реакций на нейросекрет. Использованы классические гистологические методы исследования с окрашиванием гематоксилином и эозином для получения общей морфологической картины нейронов переднего гипоталамуса человека. Анализ материала проведён с помощью микроскопа Olympus – Bx82 и цифровой камеры CDх82 с фирменным программным обеспечением.
Результаты исследования и их обсуждение
Нами отмечено, что у части нейронов при хронической ишемии мозга, в зоне, удалённой от острой ишемии и развившегося инсульта, имеется светлоокрашенное перинуклеарное пространство, которое может свидетельствовать о вступлении клеток в апоптоз (рис. 1). При этом, в нашем исследовании в апоптоз вступают как нейроглиальные клетки, так и нейроны (рис. 2). Встречаются апоптические тельца – результат апоптических процессов в нервной ткани вследствие ишемии. Это свидетельствует о том, что локальные изменения в ткани мозга присутствуют, но сам процесс ишемии мозга следует считать генерализованным по отношению к ткани всего мозга.
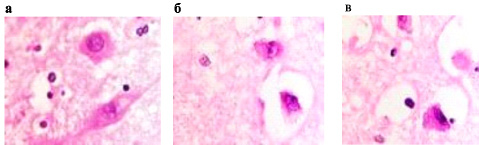
Рис. 1 а-в. Нейроны переднего гипоталамуса. Апоптоз глии и нейронов. Окраска г/э. Микрофото. Ув. х800
Структура ядер в нейронах переднего гипоталамуса свидетельствует о различном уровне дезорганизации хроматина, разрушении ядерной оболочки, апоптозе нейронов. Гранулы приобретают более тёмный коричневый цвет. В некоторых клетках вся цитоплазма заполнена гранулами, ядра не идентифицируются (рис. 2).
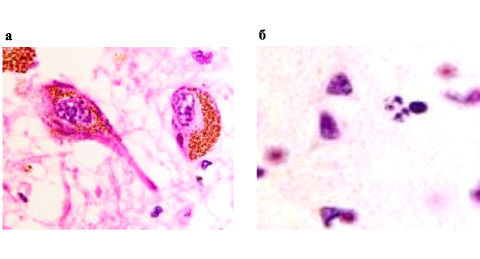
Рис. 2. Нейроны переднего гипоталамуса при ишемическом инсульте в области прецентральной извилины: а – гранулосодержащие нейроны; б – апоптическое тельце. Окраска г/э. Микрофото. Ув. х1000
Приобретение резкой базофилии окружающей нейроны глией также свидетельствует об апоптозе. Однако следует подчеркнуть, что патоморфологическое изменение нервных клеток наблюдается не только при ишемии мозга, но и при олигемических, аноксических, гипоксических и гипогликемических состояниях. Ишемическое изменение клеток характерно для хронической недостаточности кислорода, что характеризуется специфической морфологической картиной, свидетельствующей о проблеме ишемии ткани, как следствии нарушения в системе передачи кислорода клеткам гемоглобином. Вопрос включений в цитоплазме нервных клеток не закрыт, так как гранулы не изменяют цвет после проводки по спиртам, что может быть связано не с их возможной липофусциновой природой, а с наличием в них Fe3+.
Lago L., Nunes E.A., Vigato A.A., Souza V.C., Barbosa F.Jr., Sato J.R., Batista B.L., Cerchiaro G. (2017) отмечали нарушения содержания элементов металлов в головном мозге пациентов с нейродегенеративными заболеваниями [9]. Авторами были проведены эксперименты с использованием двух способов доступа к окислительному стрессу: лечение клеток с Н2О2 или Ар-42 пептида в его олигомерной форме. Оба вида лечения вызвали накопление маркеров окислительного стресса, такие как окисленные белки и липиды, а также изменения в ДНК, что также отмечали Millonig G., Gansleben I., Peccerella T. et al. [11]. Что касается микроэлементов, клетки, обработанные Н2О2, показали более высокие уровни Zn и более низких уровней Са в ядрах по сравнению с контрольными клетками, без каких-либо окислительных обработок. С другой стороны, клетки, обработанные с A – 42 пептида в олигомерной форме показали более высокие уровни Mg, Ca, Fe и Zn в ядрах по сравнению с контрольными клетками [17]. Эти различия свидетельствуют, что поток металла в клеточных органеллах во время внутреннего и внешнего окислительного состояния (обработка Н2О2) отличается от результатов современных методов лечения нейродегенеративных заболеваний.
Singh S, Goo JI, Noh H, Lee SJ, Kim MW, Park H, Jalani HB, Lee K, Kim C, Kim WK, Ju C, Choi Y. (2017) основываясь на том, что астроциты играют ключевую роль в гомеостазе мозга, защищая нейроны от нейротоксических стимулов, в том числе окислительного стресса, рассматривают в качестве многообещающей стратегии для снижения повреждения головного мозга нейропротекторные терапевтические средства, которые повышают функциональность астроцитов путем усиления митохондриальной функции после воздействия H2O2 [19].
Zhao J., Zhou H., Sun L., Yang B., Zhang L., Shi H., Zheng Y. ( 2017), напротив, считают главным виновником индуцированной дисфункции в трабекулярном эндотелии (ТЭ) дренажной системы глаза, ведущим к глаукоме, Н2О2, являющейся наиболее широко используемым средством для индукции окисления в клетках ТЭ в пробирке. При этом авторы считают, что геном имеет разную чувствительность к окислительному стрессу, индуцированному экзогенным Н2О2 [25].
Singh S.K., Thirumalai A., Pathak A., Ngwa D.N., Agrawal A. (2017) исследовали влияние перекиси водорода, прототипичную активной форме кислорода, присутствующей на участках воспаления, на функцию распознавания лиганда С-реактивного белка (СРБ) [19].
В анализах связывания лигандов на основе очищенной пентамерной Н2О2 обработанные СРБ связаны с иммобилизованными белками, включая IgG, бета-амилоид пептид 1–42, C4b-связывающий белок и фактор Н Ca2 + -независимым образом. Авторы пришли к выводу, что Н2О2 является биологическим модификатором функции и структуры лиганда распознавания СРБ [15].
De Santana F.R., Dalboni L.C., Nascimento K.F., Konno F.T., Alvares-Saraiva A.M., Correia M.S., Bomfim M.D., Casarin R.C., Perez E.C., Lallo M.A., Peres G.B., Laurenti M.D., Benites N.R., Buchi D.F., Bonamin L.V. (2017), изучая цитотоксическую активность макрофагов, наблюдали снижение миграции моноцитов и их фагоцитарной активности к месту инфекции под воздействием изменения электропотенциалов, которые объясняют клиническое ухудшение в естественных условиях при переходе 2–валентного железа в Fe3+, обладающим меньшей способностью отдавать кислород тканям [16, 21]. Большинство важнейших окислительно-восстановительных процессов протекает с участием иона металла, являющегося переносчиком одного электрона. Из этих реакций наиболее хорошо изучено взаимодействие перекиси водорода с ионом Fe2+. Реакцию открыл Фентон в 1894 г., а в 1932 г. Габер и Вайсс предложили механизм, который лишь с небольшими изменениями принят в настоящее время. Окисление органических соединений реактивом Фентона связано с генерированием гидроксильных радикалов. Однако предполагается, что гидроксильные радикалы участвуют в реакции Фентона, согласно которой перекись водорода в комбинации с солями железа окисляет альдозы до озонов [7]. В ночное время в качестве основного «поставщика» радикалов гидроксила в жидкой фазе выступает реакция Фентона – разложение Н2О2 ионами железа (П). которую можно рассматривать как реакцию переноса электрона [3]. Нерц и Вагнер высказали предположение, что кислород передается от перекиси водорода к ортофосфористой кислоте и что ион двухвалентного железа участвует в повторяющейся произвольное число раз цепи реакций, проходя соответствующие промежуточные степени окисления железа, причем ион двухвалентного железа регенерируется. Обрыв цепи вызывается превращением иона двухвалентного железа в ион трехвалентного железа, который не обладает способностью передавать кислород, что усугубляет ишемическое повреждение клеток [17].
Zhou H., Ding L., Wu Z., Cao X., Zhang Q., Lin L., Bian J.S. (2017) считают, как и многие другие авторы, что вырабатываемая клетками Н2О2 оказывает токсический эффект [25].
Sutariya S., Patel H. (2017), наоборот, пришли к положительным результатам, воздействуя на изолят сывороточного белка (WPI) растворами различных концентраций H2O2 в диапазоне концентраций 0–0.144 в деионизированной воде. Образцы анализировали на термостабильность, реологические свойства, уровень денатурации -лактоглобулин (β-LG) и альфа-лактальбумина (α-LA) [22]. Образцы, обработанные концентрации H2O2, превышающей 0,072, показали значительное улучшение в термостабильности, и снижение сывороточного белка к денатурации и агрегации. После обработки H2O2 (> 0,072 HTPR) раствор оставался в жидком состоянии после термической обработки при 120°С, в то время как контрольные образцы перешли в гель после термической обработки. Детальный анализ этих образцов позволил предположить, что улучшение тепловой стабильности после обработки раствора H2O2 было связано со значительным сокращением сульфгидрильной-дисульфид реакции обмена в процессе денатурации бета-LG и альфа-LA [16].
He Y., Del Valle A., Qian Y., Huang Y.F. (2017) предложили метод нанотерапии рака с помощью реакции Фентона на основе облучения светом тканей, что способствует переносу электронов к Fe (III) из FeOxH и ускоряет их реакцию с О2, образуя супероксидные анион-радикалы, которые затем подвергаются реакции диспропорционирования для производства Н2О2. Н2О2 затем реагирует с Fe (II) образуя FeOxH, как посредник в реакции Фентона, производя гидроксильные радикалы. Авторы показали, что GO-FeOxH может быть использован в качестве активируемого наноагента, обеспечивающего эффективную терапию рака [4, 7].
Hydrogen peroxide открыт Луи Тенаром в 1818 г. Разлагается с выделением О2, поэтому высокие концентрации при наружном применении обеспечивают противомикробный антисептический эффект, при этом удлиняются сроки заживления из-за повреждения прилегающих к ране клеток, но при этом происходит образование рубцов из-за разрушения клеток кожи. При приёме внутрь летальная доза 30 % раствора пероксида водорода – 50–100 мл. При соприкосновении с тканями под влиянием содержащихся ферментов каталазы, раствор перекиси разлагается и выделяет молекулярный кислород, который окисляет органические вещества различных клеток [14]. По данным исследований, период полураспада Н2О2 в крови человека – меньше одной десятой секунды; однако по сведениям, полученным Макнофтоном, полураспад перекиси может длиться до двух секунд и зависит от скорости смешивания с кровью. Чарльз Фарр обнаружил, что повышение содержания кислорода в тканях происходит только через 40–45 минут после инъекции перекиси.
Известно, что для выполнения фагоцитарной функции эффекторными иммуноцитами необходим каскад реакций с выделением hydrogen peroxide [12, 24]. Макрофаги способствуют поддержанию гомеостаза, очищая организм от стареющих и апоптотических клеток, восстанавливая ткани после инфекции и травмы, выполняя ведущую роль в защите организма. Для реализации этой функции они имеют набор распознающих рецепторов, кислородозависимые и кислородонезависимые механизмы киллинга микроорганизмов. Существенную роль в защите организма от инфекции играют макрофаги альвеолярные и фагоциты слизистой оболочки кишечника. Первые «работают» в относительно бедной опсонинами среде, поэтому они экспрессируют большое количество паттерн распознающих рецепторов, включая скавенджер-рецепторы, маннозные рецепторы, β-глюкан специфические рецепторы, дектин-1 и др. При микробной инфекции в очаг проникновения микробов дополнительно мигрирует большое число воспалительных моноцитов, способных дифференцироваться в различные клеточные линии в зависимости от цитокинового окружения. Ферментные системы НАДФ-Н-оксидазы, супероксиддисмутазы, NO-синтазы, генерируют активные формы неорганических окислителей, участвующих в деструкции фагоцитированного объекта: пероксид водорода (Н2О2), супероксид анион (О2–), синглетный кислород (1O2), радикал гидроксила (OH-), гипохлорид (OCl-), оксид азота (NO). Активация НАДФ-Н-оксидазы приводит к формированию так называемого «кислодородного взрыва». Первичным продуктом «кислородного взрыва» является супероксидный анион О2–, который образуется при переносе НАДФ-H-оксидазой электрона на кислород [13]. Супероксидный анион обладает слабым бактерицидным эффектом и является недолговечным. В результате реакции, катализируемой ферментом супероксидисмутазой (СОД), из двух молекул супероксидного аниона формируется перекись водорода, обладающая сильным микробицидным эффектом. При окислении хлоридов перекисью водорода в присутствии миелопероксидазы (МПО) образуется мощный цитотоксический агент – гипохлорная кислота HOCl, при её окислении супероксидным радикалом – гидроксильный радикал ОН, при окислении гипохлорит-иона перекисью водорода формируется синглетный кислород 1О2, который является источником образования другого бактерицидного вещества – озона О3. При взаимодействии гипохлорной кислоты с аминогруппой формируется микробицидное производное монохлорамина – R-NHCl.
Заключение
Анализ собственных данных и данных литературы показал, что при поражениях мозга, когда повышается уровень «активной формы» железа, аскорбиновая кислота может стимулировать образование ОН радикала, выступая в роли прооксиданта. Тиолы в восстановленной форме в присутствии «активных форм» металлов переменной валентности могут образовывать реактивные соединения типа RS (тиоловый радикал) и ОН [5]. При этом в качестве вторичных посредников принимают активное участие АФК (О2, Н2О2, ОН и гидроперекиси липидов), осуществляя регулирующую роль в процессах роста клеток, апоптозе, клеточной адгезии, свертывания крови и т.д. [1, 23].
Имеются прямые доказательства того, что низкие (микромолярные) нано- концентрации Н2О2 могут увеличивать рост или усиливать ответ на стимуляцию роста во многих типах клеток млекопитающих, а антиоксиданты подавляют нормальную клеточную пролиферацию. Так низкие концентрации Н2О2 (100 мкМ) стимулируют рост фибробластов легких хомяков [2]. Ингибирование СОД или глутатион пероксидазы увеличивает клеточную пролиферацию. Возможно, что ОН, генерируемый в реакции Фентона, может являться фактором, усиливающим клеточную пролиферацию и активность митоген-активируемой протеинкиназы (МАР-киназа). Это основано на том, что ловушки ОН (маннитол, диметилсульфоксид) и хелаторы железа тормозят стимулируемую Н2О2 пролиферацию клеток [3].
С АФК связана передача сигнала от тромбоцитарного фактора роста, эпидермального фактора роста, трансформирующего фактора роста Р-1, фактора некроза опухолей (ФНО-а) [1]. Участие интерлейкина-1 и интерферона в сигнальной транедукции вязывают с образованием О2, а фактора некроза опухолей (ФНО-а) – с Н2О2. В астроцитах интерлейкин-lfl повышает генерацию Н2О2, что приводит к снижению фосфатазной активности и активации МАР-киназы. ФНО-а через повышение образования АФК активирует факторы транскрипции NF-kp и АР-1, процессы апоптоза [11, 23].
Известно, что вазоактивный пептид (ангиотензин II) проявляет свое действие на процессы мышечного сокращения и клеточный рост гладких мышц сосудов через генерацию внутриклеточного О2 [8]. Мнение об источниках О2 НАДН и НАДФН-оксидазы, активируемых ангиотензином, опровергается данными, что именно Н2О2 ответственна за рост клеток гладкой мускулатуры сосудов. Получены данные об участии Н2О2 в сигнальной трансдукции тромбоцитарного фактора роста (PQGF) и трансформирующего фактора роста TGF-*pi. Предполагают, что Н2О2 действует через инактивацию протеинтирозинфосфатаз, как и эпидермальный фактор роста.
Тем не менее, вопрос о значении роли Н2О2 в процессах внутриклеточной сигнализации далек от разрешения. Полученные данные противоречивы и неоднозначны [18]. Только комплексный подход с учетом специфики и особенности функционирования конкретных клеток, исследования на уровне генома позволят с новых позиций оценить роль Н2О2 в механизмах регуляции функции клеток.
Учитывая то, что перекись водорода является недорогим веществом, которое не может быть запатентовано и не имеет никакой коммерческой стоимости, можно считать его наиболее перспективным для исследований механизмов его воздействия на гистофизиологию клеток с целью дальнейших стратегических решений в профилактике, лечении и реабилитации нейродегеративных повреждений мозга.
Работа выполнена при поддержке научного фонда ДВФУ, в рамках государственного задания 2014/36 от 03.02.2014 г.
Библиографическая ссылка
Рева И.В., Ямамото Т., Гульков А.Н., Такафуджи Я., Балдаев С.Н., Пикула К.С., Индык М.В., Лемешко Т.Н., Багрянцев В.Н., Рева Г.В. БИОЛОГИЧЕСКИЕ И ХИМИЧЕСКИЕ ЭФФЕКТЫ ЭНДО- И ЭКЗОГЕННОГО HYDROGEN PEROXIDE НА КЛЕТОЧНЫЕ СТРУКТУРЫ ОРГАНИЗМА ЧЕЛОВЕКА. // Международный журнал прикладных и фундаментальных исследований. 2017. № 4-2. С. 361-367;URL: https://applied-research.ru/ru/article/view?id=11473 (дата обращения: 16.05.2026).
DOI: https://doi.org/10.17513/mjpfi.11473

