По данным Всемирной организации здравоохранения до 50 % речной воды каждый год подвергается техногенному воздействию, в том числе и в результате сброса сточных вод. Поэтому при сбросе сточных вод в водоемы следует осуществлять их очистку от вредных примесей и добиваться соответствия стоков установленным показателям качества (предельно допустимым концентрациям) [1, 2]. Основными технологическими приемами удаления из воды грубодисперсных примесей и коллоидных загрязнений являются процессы коагуляции и флокуляции, позволяющие не только осветлить воду, но и в значительной степени освободить ее от таких вредных примесей, как бактерии и вирусы, соединения тяжелых металлов [3].
В результате анализа литературных данных по свойствам и сфере применения коагулянтов и флокулянтов и характеристики сточных вод аккумуляторного завода были выбраны для исследования следующие коагулянты: хлорид железа FeCl3·6H2O, сульфат алюминия Al2(SO4)3·18H2O и флокулянт – полиакриламид (ПАА).
Цель исследования: подбор оптимальных доз коагулянтов и флокулянтов с последующими рекомендациями, базируясь на исходных данных АО «Тюменский аккумуляторный завод».
Задачи исследования: приготовление модельных сточных вод аккумуляторного завода; выбор наиболее эффективных реагентов для обработки приготовленных сточных вод; определение оптимальных доз реагентов; определение остаточного содержания свинца в сточных водах.
Материалы и методы исследования
В ходе работы были разработаны методики приготовления модельных сточных вод АО «Тюменский аккумуляторный завод», проведения процесса коагулирования и флокулирования, использованы методы определения мутности (фотоколориметрический метод), кислотности (титриметрический анализ), содержания свинца (фотоколориметрический метод).
Методика приготовления модельных сточных вод: в 10 мерных цилиндров вместимостью 500 мл вносили навески свинцовой пасты массой 500, 550 и 600 мг (максимально растворимые). В соответствии с технологической инструкцией очистки сточных вод на АО «Тюменский аккумуляторный завод» доводили рН приготовленной сточной воды до 7–8 с помощью 10 %-ного раствора Na2CO3. Методом титрования 0,1 н раствором NaOH в присутствии индикатора фенолфталеина определяли кислотность сточных вод в ммоль/л, затем пересчитывали в мг/л. Таким образом, кислотность модельных сточных вод равнялась 12 мг/л, что соответствует кислотности сточных вод на АО «Тюменский аккумуляторный завод».
Методика расчёта доз коагулянтов и флокулянта: выбрали диапазон доз коагулянтов от 50 до 200 мг, поскольку оптимальной дозой коагулянта на АО «Тюменский аккумуляторный завод» является 200 мг/л, исходя из технологической инструкции, предназначенной для описания технологии очистки сточных вод на АО «Тюменский аккумуляторный завод». Дозы коагулянтов готовили из 5 %-х растворов коагулянтов, произведя перерасчет из единиц массы в единицы объема, что составило от 1,0 до 4,0 мл.
На основании литературных данных выбрали дозы флокулянта ПАА – 1,25 мг с коагулянтом FeCl3·6H2O и 0,75 мг с коагулянтом Al2(SO4)3·18H2O на 1 литр сточной воды. Дозы флокулянта готовили из 0,05 %-ного раствора полиакриламида, что составило соответственно для коагулянтов: 5 мл для FeCl3·6H2O, и 3 мл для Al2(SO4)3·18H2O [4].
Методика исследования процесса коагулирования с использованием флокулянта: в 10 мерных цилиндров вместимостью 500 мл с приготовленными сточными водами последовательно с помощью мерной пипетки добавляли коагулянт и с помощью мерной пробирки флокулянт. После 30-минутного отстаивания в течение часа через каждые 10 минут во все цилиндры погружали мерную пипетку на глубину ниже уровня жидкости на 10 см для забора пробы. Для определения мутности, как показателя качества воды, использовали нефелометрический метод. Во всех взятых пробах определяли оптическую плотность на фотометре КФК-3-01. По калибровочному графику, построенному по стандартному образцу (СО) мутности (формазиновой суспензии), рассчитывали мутность приготовленных сточных вод [5].
Методика определения концентрации свинца в модельных сточных водах: анализируя литературные данные по определению концентрации свинца в природных и сточных водах, остановились на фотометрическом методе ГОСТ 18293-72, ПНД Ф 14.1: 2.54-96 [6].
Приготовление пробы: 100 мл сточной воды перенесли в коническую колбу на 500 мл, добавили 5 мл азотной кислоты 1:1, поставили на плитку и нагрели. Затем колбу сняли, остудили, перенесли в мерную колбу на 250 мл, дистиллированной водой довели до метки.
Ход анализа: 10 мл пробы вылили в делительную воронку, затем приготовили холостую пробу; после чего налили 20 мл дистиллированной воды в делительную воронку и прибавили 5 мл приготовленной холостой пробы; добавили по 15 мл дистиллированной воды в каждую из делительных воронок; затем по 10 капель фенолового красного; нейтрализовали раствор гидроксидом натрия 0,05 н до оранжево-красного цвета; в раствор с помощью мерной пипетки добавили по 2 мл железосинеродистого калия 10 % раствора (свежеприготовленного); затем с помощью мерной пипетки добавили по 3 мл 1 %-ного раствора солянокислого гидроксиламина; после этого по 3 мл 10 %-ного раствора лимонной кислоты; нейтрализовали 20 %-ным раствором карбоната натрия до светло-малинового цвета; далее добавили по 10 мл 0,01 %-ного раствора дитизона; затем встряхивали растворы в делительных воронках в течение одной минуты, цвет дитизона должен смениться с зелёного на красный; во вторые делительные воронки залили по 15 мл 0,025 н соляной кислоты; из первых воронок слили осадок с дитизоном во вторые воронки; после расслоения дитизона слили его, из оставшегося водного слоя взяли элеквот по 10 мл и перенесли в мерные колбы на 25 мл; в мерные колбы с элеквотом мерной пипеткой добавили по 0,3 мл 5 %-ного раствора щавелевокислого аммония, по 0,2 мл 10 %-ного раствора тиомочевины; далее добавили по 0,4 мл 1 %-го раствоа железосинеродистого калия (свежеприготовленного), по 0,25 мл 0,05 %-ного раствора сульфарсозена; довели получившийся раствор до метки бурой; на ФЭК 3-01 при длине волны 520 нм, в кюветах на 10 мл, определяли оптическую плотность. Построив калибровочный график по стандартному образцу (СО) состава водных растворов ионов свинца, определили массовую концентрацию ионов свинца в пробах модельных сточных вод.
Результаты исследования и их обсуждение
Процесс коагуляции состоит из нескольких этапов. В начале происходит гидролиз соли (коагулянта), при котором образуются малорастворимые соединения (оксигидраты). При внесении Al2(SO4)3 в воду происходит гидролиз по катиону:
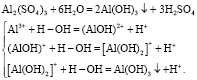
Аналогично для хлорида железа FeCl3. Продукты гидролиза поглощаются примесями воды, окружая их рыхлыми влагонасыщенными оболочками (мундирами). Оказавшись в таких мундирах, дисперсные загрязнения утрачивают индивидуальные свойства и приобретают свойства оксигидратов. Следующий этап коагуляции состоит в объединении частиц, постепенным образованием скоплений в виде хлопьев коагулированной взвеси. Они обладают достаточной массой, чтобы отделиться в осадок под действием силы тяжести. Оптимальная доза коагулянта – это такая его наименьшая доза, при которой после отделения в осадок коагулированной взвеси (в течение заданного промежутка времени) достигается требуемая степень очистки воды. При внесении флокулянта ПАА, содержащего в макромолекуле 3–8 % карбоксилатных звеньев, обычно используемого как неионогенный флокулянт, в дополнении к непосредственному контакту частиц происходит их взаимодействие через молекулы адсорбированного флокулянта, что способствует увеличению размеров образовавшихся хлопьев и их дальнейшего удаления. На графиках (рис. 1, 2) продемонстрированы зависимости изменения оптической плотности сточных вод в процессе отстаивания при различных дозах коагулянтов и флокулянта и содержания свинцовой пасты.
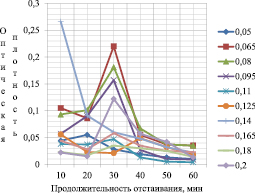
Рис. 1. Зависимость оптической плотности от продолжительности отстаивания: FeCl3•6H2O + ПАА 5 мл при содержании свинцовой пасты 500 мг/л
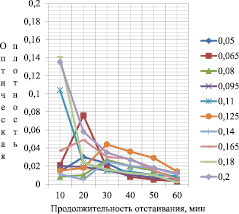
Рис. 2. Зависимость оптической плотности от продолжительности отстаивания: Al2(SO4)3•18H2O + ПАА 3 мл при содержании свинцовой пасты 550 мг/л
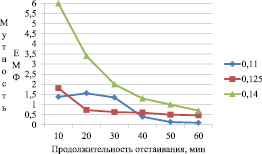
Рис. 3. Зависимость мутности от продолжительности отстаивания: FeCl3•6H2O + ПАА 5 мл при содержании свинцовой пасты 500 мг/л
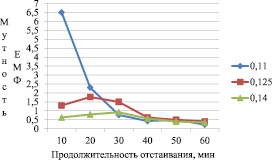
Рис. 4. Зависимость мутности от продолжительности отстаивания: Al2(SO4)3•18H2O + ПАА 3 мл при содержании свинцовой пасты 550 мг/л
В процессе эксперимента выяснили, что в первые 30 минут идет возрастание оптической плотности, это можно объяснить тем, что происходит образование крупных хлопьев, в результате повышается мутность и, следовательно, оптическая плотность. Поэтому решили измерять оптическую плотность сточных вод через 30 минут, чтобы дать время на структурирование. Через последующие 20–30 минут после начала измерений наблюдался резкий скачок оптической плотности воды. Это явление объясняется тем, что при добавлении флокулянта начинается формирование макроструктур, состоящих из коллоидных частиц с адсорбированными на них труднорастворимыми хлопьями гидроксида, связанными макромолекулами флокулянта. Далее происходит осаждение крупных хлопьев под действием силы тяжести и, как следствие, понижение оптической плотности.
Исходя из минимальных значений оптической плотности приготовленных сточных вод, при разных дозах коагулянта, после 60-минутного отстаивания, выбрали оптимальный диапазон доз коагулянтов, 110–140 мг/л. После чего для выбранных доз коагулянтов по калибровочному графику, построенному по стандартному образцу (СО) мутности, определили мутность сточных вод. На графиках (рис. 3, 4) продемонстрированы зависимости изменения мутности воды в процессе отстаивания при различных дозах коагулянтов и флокулянта и содержания свинцовой пасты.
Оценка достоверности полученных результатов: определяли функцию изменения мутности сточной воды в течение некоторого промежутка времени, применив метод регрессионного анализа. Описали регрессионный анализ на примере полученных значений мутности при добавлении 140 мг/л сульфата алюминия и 1,25 мг/л полиакриламида. Аналогично было получено уравнение регрессии при дозе коагулянта 140 мг/л хлорида железа и 1,25 мг/л полиакриламида. Полученные результаты представлены на рис. 5.
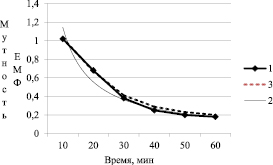
Рис. 5. Кинетика отстаивания сточных вод при добавлении 140 мг/л коагулянта Al2(SO4)3 и 0,75 мг/л флокулянта ПАА. 1 – экспериментальные данные, 2 – линия тренда, 3 – полученные данные
Анализ опытных данных показал, что функция изменения мутности в конкретные промежутки времени при разных дозах коагулянта и флокулянта является убывающей степенной функцией 3-го порядка и адекватно описывает кинетику отстаивания сточных вод.
Заключение
1. В процессе проведения исследований приготовлены модельные сточные воды, приближенные к реальным на АО «Тюменский аккумуляторный завод», их рН соответствовала 8, кислотность равнялась 12 мг/л.
2. В качестве коагулянтов выбраны хлорид железа (FeCl3) и сульфат алюминия (Al2(SO4)3) в диапазоне доз от 50 до 200 мг/л.
3. Коагулянт FeCl3 в сочетании с флокулянтом ПАА – 1,25 мг/л.
4. Коагулянт Al2(SO4)3 в сочетании с ПАА – 0,75 мг/л.
5. Определены оптимальные дозы коагулянтов: для хлорида железа – 110 мг/л, для сульфата алюминия – 140 мг/л.
6. Фотометрическим методом определены концентрации свинца в модельных сточных водах до и после коагулирования в исследуемых диапазонах.
7. Содержание свинца после процесса очистки сточных вод не превышало допустимые нормы, н/б 0,25 мг/л.
Библиографическая ссылка
Качалова Г.С. ИСПОЛЬЗОВАНИЕ СОВРЕМЕННЫХ КОАГУЛЯНТОВ И ФЛОКУЛЯНТОВ В ПРОЦЕССЕ КОАГУЛИРОВАНИЯ СТОЧНЫХ ВОД // Международный журнал прикладных и фундаментальных исследований. 2018. № 2. С. 23-27;URL: https://applied-research.ru/ru/article/view?id=12101 (дата обращения: 15.02.2026).

