Хронический виллит (ВХ) диагностируется по наличию смешанной лимфоидной инфильтрации стромы промежуточных и терминальных ворсин (могут присутствовать гистиоциты, плазмоциты), а также иногда вовлекаются стволовые ворсины и хориальная пластинка, в то время как при острых виллитах присутствует преимущественно инфильтрация полиморфноядерными лейкоцитами (ПЯЛ). ВХ диагностируются от 5 до 10 % от общего числа плацент [1, 2]. Хотя среди хронических виллитов в США и странах Западной Европы инфекционная природа выявлена приблизительно в 1–4/1000 случаев [3], но только в небольшом проценте наблюдений удаётся выявить инфекционный агент. В большинстве наблюдений возбудитель не обнаруживается, и для обозначения указанного состояния применяется термин «идиопатический хронический виллит» или «виллит неизвестной этиологии» (ВХНЭ) (англ. villitis of unknown etiology – VUE), который включает все случаи хронического виллита с неидентифицированной флорой (согласно Амстердамской классификации, 2104 (the Amsterdam Placenta Working Group) [1]. ВХ может быть как инфекционной, так и неинфекционной этиологии, и связан с аутоиммунными заболеваниями, проявляющейся инфильтрацией лимфоцитов матери стромы ворсин [4–6]. Морфологическая картина этих состояний во многом сходна, и вызывает затруднения при диагностике из-за недостатка выявления микроорганизмов в плаценте, при отсутствии признаков инфекции у матери и плода.
Считается, что ВХ, вызванный инфекционным фактором, отличается от неинфекционного по ряду признаков:
1) более часто встречается при недоношенных сроках гестации;
2) более выраженные и обширные поражения ворсинчатого дерева, хориоамниона, пуповины, а также базальной и децидуальной пластинок;
3) при гистологическом исследовании присутствие фиброза ворсин стромы и микрокальцинатов;
4) в дифференциальной диагностике следует учитывать наличие инфекции матери или инфекции плода.
Возбудителями ВХ часто являются вирусы Сytomegalovirus, Herpes simplex virus, Varicella-zoster virus, Rubella virus, Poxviruses (вирусы краснухи и оспы, в том числе связанные с вакцинацией), а также простейшие Toxoplasma gondi, Trypanosoma cruzi (Болезнь Шагаси), спирохеты Treponema pallidum (сифилис), Borrelia burgdorferi (Болезнь Лайма).
Хронический интервиллузит (интервиллит) (очаговое поражение части ворсин с наличием клеток воспалительного ряда в межворсинчатом пространстве), ассоциировано с вирусом кори, простейшими малярийным плазмодиумом, Plasmodium spp. (malaria), Schistosoma mansoni (шистосоматоз), грибами рода Coccidiodes immitis, Cryptococcus neoformans, хламидиозом Chlamydia psittaci (пситаккоз), риккетсиями Coxiella brunetti (Ку-лихорадка), бактериями Campylobacter fetus, риккетсиями – Francisella tularensis (тулерямия), Brucella abortus (бруцеллез), вирусом Эпштейна – Барр. К врожденным инфекциям, вызывающих ВХ, ограниченные синцитиотрофобластом и межворсинчатым пространством без признаков виллита, относятся микозы (кокцидиоидомикоз, криптококкоз), вирусами (корь), простейшими (малярия, шистосоматоз), риккетсиозами (Q-лихорадка), хламидиозами (пситтакоз) и (Francisella tularensis, Brucella abortus, Campylobacter fetus). Все эти инфекции, как полагают, распространяются на плаценту гематогенным путём. Наиболее часто встречаются на ранних сроках беременности в отсутствии защитных антител [6, 7].
Хронический воспалительный клеточный ответ, обусловленный вирусами и простейшими, обычно выявляется как в строме ворсин, так и в межворсинчатом пространстве [3]. Наиболее распространённые инфекции TORCH (токсоплазмоз, гепатит В, вирус краснухи, цитомегаловирус и вирус простого герпеса), эти микроорганизмы, как и цитомегаловирус, могут вызывать диффузный виллит, с отёком, фиброзом и выраженной инфильтрацией плазмоцитами. Наименее распространенное поражение малярией связана с выраженным интервиллузитом, но строма ворсин плаценты при этом не вовлечена [1, 8, 9]. При некоторых инфекциях, таких как листериоз, в одной плаценте может быть сочетание гистологических признаков хориоамнионита, виллита, интервиллузита [10].
Патологические данные, которые позволяют патоморфологам заподозрить ВХ инфекционной этиологии, следующие: инфекция, обусловленная цитомегаловирусом, обычно сопровождается небольшим фиброзированием ворсин плаценты с отложением микрокальцинатов [11]. В противовес этому, при инфицировании вирусом Zika (передающегося различными путями: гематогенным, половым, а также трансплацентарно, являющейся причиной врожденных пороков развития центральной нервной системы, прежде всего микроцефалии у плода, и имеющего нередко стертую клиническую картину [12], ворсины плаценты крупные с гиперклеточной стромой, повышенным количеством клеток Гофбауэра, однако некрозы и дистрофические нарушения в ворсинчатом дереве отсутствуют [12]. Наряду с этим для вируса Zika на поздних сроках гестации характерны хориоамниониты, фунизиты с вовлечением пупочных сосудов, децидуиты (воспаление децидуальной оболочки) [12]. При инфицировании вирусом Zika хориоамниониты могут быть связаны также и с коинфекцией, включающей стрептококки группы B, E. coli, Ureaplasma, Chlamydia, Mycoplasma, и другую вагинальную флору, попадающей в плодные оболочки гематогенным путём [12].
Гистологические изменения в виде ВХ также характерны для вируса гриппа, в том числе высокопатогенного штамма гриппа A/H1N1 [13]. В случаях, осложненных врожденным гепатитом, гипопротеинемия нередко может приводить к развитию выраженного отёка ворсин, за счёт чего плацента будет увеличена.
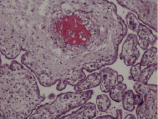
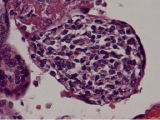
А Б
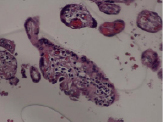
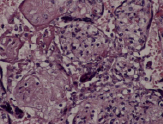
В Г
Д Е
Ж З
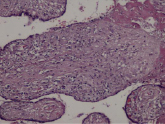
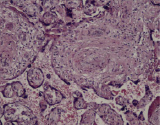
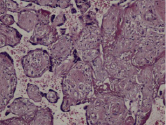
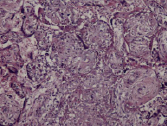
Воспалительные изменения ворсинчатого дерева плаценты (окраска гем-эозин) A–Г – Хронический виллит неустановленной этиологии (инфильтрация стромы лимфоцитами, макрофагами, единичными плазмоцитами с примесью ПЯЛ), А – х200, Б – х400, В – х200, Г – х200. Д–З – Обструктивная фетальная васкулопатия (облитерация просвета сосудов, присутствие бессосудистых ворсин; отмечается также периворсинчатое отложение фибриноида, склеивание ворсин, формирование афункциональных зон), Д–З – х200
Обнаружение в строме ворсин плазмоцитов часто свидетельствует о цитомегаловирусной инфекции. Важными гистологическими данными при цитомегаловирусной инфекции являются обнаружение в строме ворсин плазмоцитов, а также нарушение васкуляризации ворсин, появление бессосудистых ворсин, окклюзия просвета сосудов ворсин, отложение в строме ворсин гемосидерина. При сифилисе имеет место умеренно выраженная лимфоидная инфильтрация в сочетании с фиброзом стромы ворсин плаценты. Врожденный сифилис также нередко ассоциируется с патологической незрелостью плаценты, значительным отставанием её от сроков гестации, но отёчные ворсины единичны, преобладает выраженная диффузная гистиоцитарная инфильтрация с примесью лимфоцитов [1, 11], фиброз стромы ворсин и очаги периваскулитов стволовых ворсин могут помочь в диагнозе. Почти всегда патогномонично присутствие в пуповине вытянутых полос, обусловленных некрозом и воспалением, особенно при вовлечении стенки пупочной вены и с распространением на вартонов студень (некротический перифлебит). Как правило, только в этом месте, спирохеты могут быть выявлены посредством специальной окраски.
При врожденном токсоплазмозе (Toxoplasma gondii) плацента увеличена в размере, ворсины незрелые, но не отёчные [1], инфильтрация ворсинчатого дерева плаценты имеет тенденцию к очаговой локализации и часто ассоциируется с некротическими изменениями ворсин или инфильтрацией многоядерными гигантскими клетками гистиоцитарного происхождения, нередко выявляется диффузный хронический децидуит. Определяющим в диагностике плацентарного токсоплазмоза является обнаружение инкапсулированных псевдокист в вартоновом студне, псевдокисты визуализируются при рутинном окрашивании гематоксилином и эозином. Неблагоприятные исходы, такие как привычное невынашивание беременности, антенатальная гибель плода, водянка плода, преждевременные роды, внутриутробная задержка развития плода, нарушение формирования внутренних органов, особенно центральной нервной системы, обычно наблюдаются при виллитах, обусловленных инфекционным агентом.
Наряду с этим периферический фунизит с микроабсцессами часто связан с поражением грибами рода Candida. Однако грибы редко вызывают гранулематозное воспаление. Для выявления гранулем необходимы специальные окраски (по Steiner, Dieterle или Warthin-Starry), для дифференциального диагноза имеет значение анализ данных истории болезни.
ВХНЭ не имеет характерной клинической картины и не ассоциирован с какими-то конкретными заболеваниями, однако пациентки с наличием аутоиммунных заболеваний, повышенной массой тела, при использовании донорской яйцеклетки, привычным выкидышем, а также внутриутробной задержкой развития плода, ВХНЭ выявляется достоверно чаще [14]. ВХНЭ может быть ассоциирован с хроническим децидуитом, лимфоплазмоцитоидным децидуитом и эозинофильным Т-клеточным фетальным васкулитом, однако каждое из них может быть независимым [3].
Хронический гистиоцитарный интервиллит (массивный хронический интервиллит) – редкое воспалительное идиопатическое заболевание, характеризующееся мономорфными материнским гистиоцитарными инфильтратами в межворсинчатом пространстве с наличием CD68+ макрофагов, часто в сочетании с межворсинчатым отложением плодного фибриноида, кроме того, нередко имеют место инфаркты материнской части плаценты. Поражение стромы ворсинчатого дерева нередко отсутствует [14–18]. Хронический гистиоцитарный интервиллит может быть причиной потери беременности, преждевременных родов, внутриутробной задержки развития и антенатальной гибели плода [16–18]. Это состояние имеет самый высокий риск повторных осложнений, что удается проследить в анамнезе на протяжении 10 беременностей и более. Некоторые авторы считают, что данная категория пациентов отвечает на аспирин, гепарин и иммуносупрессивную терапию [16–18].
Несмотря на это, патогенез ВХНЭ остаётся неясным. Существуют две теории ВХНЭ. Одна из предложенных гипотез связывает ВХНЭ с нераспознанным инфекционным агентом, в ткани плаценты без проникновения в кровь плода Подтверждением этого явилось обнаружение вирусоподобных частиц, выявляемых посредством электронной микроскопии [16–18]. Согласно другой теории ВХНЭ является результатом проникновения материнских лимфоцитов через гемо-плацентарный барьер: лимфоциты, проникая через барьер синцитиотрофобласта, инфильтрируют строму ворсин. Однако данные изменения отмечены и в ворсинах плаценты при врожденных пороках развития плода [19, 20]. ВХ в данном случае является дискуссионным вопросом, что в ряде наблюдений можно объяснить тератогенным действием вирусов на плод, и формирование порока за счёт влияния вируса, с другой стороны, реакцией организма матери на плод с пороком развития и с генетическими нарушениями. Реакции материнского организма по типу отторжения трансплантата при акушерской патологии, была подтверждена обнаружением CD8+ Т-лимфоцитов матери [4, 5, 16] в строме ворсин плаценты [17]. Известно, что материнские Т-лимфоциты могут напрямую контактировать с фетальными антиген-презентирующими клетками, несущими антигены гистосовместимости II класса отцовского происхождения. Результатом этого процесса является иммунный ответ по типу реакции отторжения трансплантата, что приводит к увеличению активации антиген-специфических Т-лимфоцитов как фетальных, так и антиген-специфических CD8+ позитивных клеток у матери [16, 21], активации антиген-специфического ответа. Этот процесс также может усиливать инфекция урогенитального тракта, увеличение концентрации цитокинов, локальное воспаление. Механизм нарушения иммунологической толерантности описан также при увеличении провоспалительных хемокинов CXCL и их рецепторов CXCR, связанных с системным материнским воспалительным ответом [4, 5]. Важным патогенетическим звеном является вероятность цитокинового повреждения синцитиотрофобласта, что может благоприятствовать дополнительному проникновению инфекции [22]. Вероятно, этому также могут способствовать десиалирование синцитиотрофобласта [2, 21, 22], в том числе нельзя исключить воздействие сиалидаз микроорганизмов.
Антенатальные сопоставления с ВХНЭ включают повышенный уровень уровня α-фетопротеина в сыворотке материнской крови, отягощенный акушерский анамнез по предыдущим беременностям, включая случаи невынашивания беременности, внутриутробную задержку развития плода, а также внутриутробную гибель плода [16].
Гистологические критерии хронических виллитов основываются на наличии воспалительной инфильтрации в различных структурах плаценты [3].
Патологические изменения плаценты, ассоциированные с повышенным риском при последующих беременностях [3]
|
Редкие |
Частота осложнений |
|
Хронический гистиоцитарный виллузит |
75–90 % |
|
Массивное периворсинчатое отложение плодного фибриноида |
40–60 % |
|
Более распространенные |
|
|
Виллит неустановленной этиологии |
25–50 % |
|
Плацента accreta |
25–30 % |
|
Тяжелая тотальная/частичная материнская мальперфузия (нарушение кровообращения) |
10–25 % |
|
Самопроизвольные преждевременные роды с гистологически подтверждённым хориоамнионитом |
10–25 % |
- Базальный – инфильтрация базальной пластинки клетками воспалительного ряда (наличие децидуита) и небольшой части ворсин (крупные стволовые ворсины), прилегающие к базальной пластинке.
- Очаговый (фокальный) – поражение < 10 ворсин в поле зрения и/или в 2–3 полях зрения.
- Мультиочаговый (мультифокальный) – поражение > 10 ворсин в поле зрения и/или < в 3 полях зрения.
- Крупноочаговый – поражение > 10 ворсин в поле зрения и/или <5 % от всего объёма ворсинчатого дерева.
- Диффузный – поражение > 10 ворсин в поле зрения и/или > 5 % от всего объёма ворсинчатого дерева.
Фокальный и мультифокальный ВХ относят к низкой степени активности воспалительного процесса. Крупноочаговый и диффузный ВХ – к высокой активности воспалительного процесса.
В строме ворсин могут присутствовать также многоядерные гигантские клетки (вариант гранулематозного воспаления) и примесь нейтрофилов (ВХ высокой степени активности). В отличии от базального хронического виллита, воспалительная инфильтрация при других формах характеризуется более выраженной инфильтрацией Т- и В-лимфоцитами (рисунок, А–Г).
Для диффузного ВХ характерно увеличение количества плодного фибриноида с периворсинчатым его расположением, а также межворсинчатая инфильтрация мононуклеарами (интервиллит), нередко сочетающееся наличием плазматических клеток в базальной пластике. Воспалительная инфильтрация обнаруживается преимущественно в промежуточных и терминальных ворсинах. Кроме того, для диффузного ВХНЭ характерна и воспалительная инфильтрация стромы крупных стволовых ворсин с развитием периваскулита и васкулита сосудов стволовых ворсин, что в свою очередь часто приводит к окклюзии просвета сосудов и формированию бессосудистых ворсин (обусловливая развитие фетальной облитерирующей васкулопатии) (рисунок, Д–З), нередко с наличием тромбов в просвете сосудов (фетальная тромботическая васкулопатия) [3], может опосредовать развитие гипоксии, повреждение центральной нервной системы, а также приводя к задержке внутриутробного развития плода (таблица) [1, 3, 23].
Исходы хронического виллита
Базальный ВХ, в том числе низкой степени активности, часто протекают, бессимптомно, редко вызывая задержку развития плода и преждевременные роды. В то же время ВХ высокой степени активности, особенно диффузный ВХНЭ вариант часто ассоциированы с задержкой развития плода, являясь причиной антенатальной гибели плода, а также в 10–25 % может быть рецидивирующим при последующих беременностях, являясь причиной невынашивания беременности. ВХНЭ в сочетании с фетальной облитерирующей васкулопатией, так и с фетальной тромботической васкулопатией может обусловить гипоксию плода и развитие ишемических повреждений головного мозга [23–25].
Библиографическая ссылка
Низяева Н.В. ГИСТОЛОГИЧЕСКИЕ КРИТЕРИИ ВОСПАЛИТЕЛЬНЫХ ИЗМЕНЕНИЙ ВОРСИНЧАТОГО ДЕРЕВА ПЛАЦЕНТЫ // Международный журнал прикладных и фундаментальных исследований. 2018. № 2. С. 202-207;URL: https://applied-research.ru/ru/article/view?id=12136 (дата обращения: 05.02.2026).

