Рак слизистой оболочки полости носа и придаточных пазух (ПНПП) составляет 3 % всех случаев опухолей головы и шеи [1]. В настоящее время продолжаются поиски альтернативных вариантов лечения, которые позволили бы решить сразу несколько задач: улучшить выживаемость, снизить токсичность химиолучевого лечения, обеспечить возможность применения высокоактивного лечения у пациентов с соматическими заболеваниями [2]. Современная стратегия лечения основана на междисциплинарном подходе, который включает в различной последовательности лучевую терапию (ЛТ) в сочетании или без применения различных радиомодификаторов и расширенно-комбинированное хирургическое вмешательство [3, 4]. Особенности течения раневого процесса у больных, оперированных по поводу опухолей челюстно-лицевой области, а именно: первичная инфицированность, снижение местного и общего иммунитета, нарушение микроциркуляции и реологических свойств крови как реакция на операционную травму, способствуют увеличению длительности процессов репарации и эпителизации стенок послеоперационной полости, развитию воспаления в области эндопротеза и, как следствие, отторжению последнего в зонах с недостаточностью процессов интеграции имплантатов с окружающими тканями. Хирургическая травма в значительной степени угнетает и без того нарушенный местный защитный барьер [5]. Иммунный ответ организма играет важную роль в купировании воспалительного процесса в послеоперационном периоде. Специфический иммунный ответ сопряжен с продукцией цитокинов, которые влияют на течение и исход иммунного ответа, осуществляют взаимосвязь между неспецифическими защитными реакциями и клеточным иммунитетом, определяют преимущественную его направленность по гуморальному или клеточному типу. Многочисленные факты указывают на наличие тесной взаимосвязи между уровнем продукции этих молекул и клиническими характеристиками инфекционного процесса [6].
Таким образом, представляется необходимой разработка методики способной стимулировать защитный барьер у пациентов в послеоперационном периоде с раком слизистой оболочки полости носа и придаточных пазух для купирования воспалительного процесса и сокращения сроков заживления раневой поверхности.
В последние годы широко используются методы физиотерапевтического лечения, которые способны благоприятно влиять на воспалительный и восстановительный процесс. Особая роль отводится магнитолазерной терапии, при которой проводится одновременное воздействие сочетанием магнитного поля и лазера. При данном виде лечения осуществляется воздействие лазером инфракрасного спектра 0,8–1,3 мкм, который может проникать на глубину до 4–8 см, максимально пропускается кожными покровами, ориентирует диполи в одну линию вдоль световой волны за счет постоянного магнитного поля, что способствует резонансному взаимодействию биологических структур, усиливая светопоглощение [7]. Механизм магнитолазерного воздействия обладает выраженным противовоспалительным эффектом за счет улучшения микроциркуляции крови, купирования спастических реакций микрососудов. Происходит уменьшение интерстициального отека, активации макрофагальной реакции на экссудативной стадии воспаления. Стимулируется рост эпителиальных клеток, усиливаются процессы регенерации тканей, стимулируется иммунная система. Фотобиологический процесс протекает по механизму срочной адаптации, т.е. повышаются защитные механизмы кожи, слизистых оболочек и всего организма в целом [8]. Процесс заживления раневой поверхности происходит быстрее и в более ранние сроки без наличия осложнений.
Цель исследования: изучение влияния магнитолазера на показатели иммунного ответа у пациентов с опухолями полости носа и придаточных пазух после расширенных хирургических вмешательств с реконструктивно-восстановительным компонентом.
Материалы и методы исследования
Исследования проводились на базе клиник Томского НИИ онкологии НИМЦ с 2002 по 2018 г. у 60 пациентов, которым было проведено комбинированное лечение на фоне новообразований полости носа и придаточных пазух Т3-4N0-1M0. В основную группу (первая группа) вошли 30 пациентов с местнораспространенными злокачественными опухолевыми процессами, получавшие комбинированное лечение с предоперационной лучевой терапией и эндопротезированием костных структур субкраниальной области и стенок орбиты имплантатами из никелида титана. В данной группе для улучшения процессов репарации в послеоперационном периоде применялось физиотерапевтическое лечение с использованием магнитолазера. Контрольная группа (вторая группа) состояла из 30 пациентов, которым выполнялось только хирургическое вмешательство без восстановительного лечения с помощью методов физиотерапии. В обе группы были отобраны пациенты одинаковые по полу, возрасту, морфологическому строению опухолей и распространенности процесса.
Всем пациентам проводился курс стандартной предоперационной дистанционной гамма-терапии в режиме фракционирования дозы: РОД – 3 Гр., 5 фракций в неделю, СОД составляла – 44 изо Гр. Через 3–5 дней выполнялось оперативное вмешательство в объеме комбинированной электрорезекции верхней челюсти.
С целью исследования местного иммунитета в области раневой поверхности и влияния на его показатели магнитолазерной терапии было проведено определение уровней фактора некроза опухолей и γ-интерферона; интерлейкинов 1, 4, 8 (ИЛ-1, ИЛ-4, ИЛ-8). Проведено также исследование по выявлению зависимости уровня цитокинов от злокачественности опухолевого процесса в смывах из послеоперационной раны.
Изменение клеточного и гуморального иммунитета основывалось на определении уровня Т, В-лимфоцитов, иммуноглобулинов класса А, М, G в крови.
Магнитолазеротерапия проводилась с 8–10 суток после операции с помощью аппарата «Милта-Ф» по разработанной нами методике (патент № 2216302 от 2002 г.) ежедневно. Курс лечения зависел от состояния послеоперационной раны и выполнялся от 5 до 12 сеансов. Выраженная воспалительная реакция послеоперационной раневой поверхности требовала увеличения продолжительности воздействия от 30 с до 2 минут.
Обработка результатов исследования проводилась на персональном компьютере в среде Windows 7 с использованием статистической программы SPSS Statistica версия 21.
Результаты исследования и их обсуждение
Исследование содержания интерферона-g в смывах из послеоперационной полости показало, что цифровые значения у пациентов обеих групп оставались на одном уровне.
Результаты определения противовоспалительного ИЛ-4 не выявили статистически значимых различий между показателями в группах, но применение магнитолазерной терапии в послеоперационном периоде поддерживало ровный уровень цитокина (рис. 1), тогда как у пациентов контрольной группы снижение ИЛ-4 отмечено на 15 сутки после операции (р = 0,08) (рис. 2).
Уровень ИЛ-1 у больных обеих групп в послеоперационном периоде незначительно повышался на 10-е сутки, постепенно снижаясь к 15 суткам у пациентов контрольной группы и повышаясь у больных основной группы. Результаты исследования оказались статистически недостоверны, но с тенденцией (р = 0,07).
При определении содержания ИЛ-8 цифровые значения имели схожую динамику у пациентов обеих групп. Однако у больных основной группы уровень этого цитокина на 10-е и 25-е сутки после операции был значительно выше соответствующего показателя в контрольной группе. Данный факт констатирует положительное влияние магнитолазера на ИЛ-8, который в свою очередь негативно влияет на клеточное окружение опухоли и клетки в зоне воспаления (рис. 3–4).
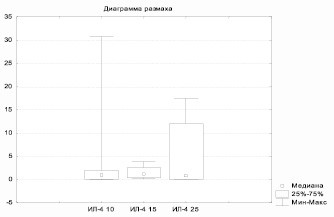
Рис. 1. Динамика ИЛ-4 у пациентов основной группы (использование магнитолазерной терапии)
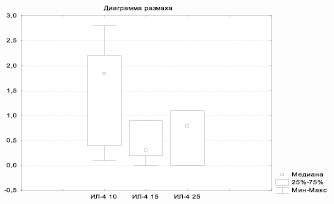
Рис. 2. Динамика ИЛ-4 у пациентов контрольной группы
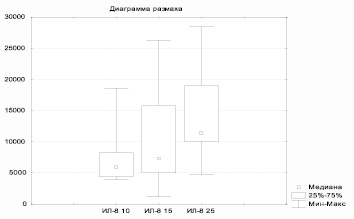
Рис. 3. Динамика ИЛ-8 у пациентов основной группы (использование магнитолазерной терапии)
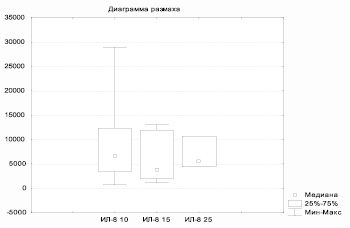
Рис. 4. Динамика ИЛ-8 – у пациентов контрольной группы
Определение такого важного медиатора процесса воспаления, как фактор некроза опухоли, является важным, так как обладает прямым действием на опухолевые клетки, выступает регулятором Тh1 иммунного ответа, ускоряя созревание и дифференцировку Т-лимфоцитов. Исследование показало, что высокий уровень у пациентов в контрольной группе, имеющий место на 10 сутки, снижался до нулевых значений к 25-м суткам. В основной группе пациентов после применения магнитолазера уровень повышался и был наиболее высок к 25-м суткам.
После применения магнитолазера отмечался рост показателей клеточного иммунитета, в частности уровень Т-лимфоцитов возрос с 29 % до 44 %, В-лимфоцитов с 4,8 % до 28 %. Наблюдалось восстановление иммуноглобулинов класса А до нормальных показателей в 58 % случаев, иммуноглобулинов G у 78 %, количество иммуноглобулинов М возрасло у 49 % больных. Полученные данные позволили нам сделать вывод об эффекте стимулирования исходно сниженного иммунитета.
По результатам наших исследований магнитолазер положительно влияет на продукцию провоспалительных цитокинов, стимулируя их выработку и поддерживая высокий уровень в очаге воспаления. Уровень интерлейкина-8 статистически значимо возрастал у пациентов основной группы к 25-м суткам послеоперационного периода, что явилось сигналом запуска механизма хемотаксиса, повышения активности хемоаттрактанта для нейтрофилов, базофилов и Т-лимфоцитов и включения местных защитных реакций слизистой оболочки в зоне раневой поверхности. Так как данный цитокин является одним из стимуляторов ангиогенеза, повышение его уровня в зоне оперативного вмешательства после обработки магнитолазером, ускоряло репаративные процессы.
Предотвращение развития иммунодепрессии и нормализация процессов репарации происходит за счет блокирования ФНО-α моноцитами и макрофагами спонтанной и индуцированной продукции провоспалительных цитокинов (ИЛ-1, ИЛ-8) выработкой противовоспалительных цитокинов и растворимых ингибиторов провоспалительных цитокинов, которым и является цитокин ИЛ-4.
По данным наших исследований у пациентов основной группы уровень противовоспалительного цитокина ИЛ-4 оставался стабильным во все сроки послеоперационного периода в отличие от значений у пациентов контрольной группы. Применение магнитолазера, по-видимому, запускало механизм цитокинового каскада, поддерживая баланс между провоспалительными цитокинами и противовоспалительными медиаторами, тем самым купируя воспалительный процесс в послеоперационной полости и ускоряя репаративные процессы.
Заключение
Результаты нашего исследования показали активизацию иммунного статуса, факторов неспецифической защиты в области раневой поверхности в послеоперационном периоде у пациентов с опухолями полости носа и придаточных пазух после расширенных хирургических вмешательств и использования магнитолазера. Усиление репаративных процессов, ранняя эпителизация позволяет предотвратить гнойно-септические осложнения, сократить сроки госпитализации. Кроме того, полученные результаты использования магнитолазера выявили стимулирование исходно сниженного иммунитета за счет роста и нормализации показателей клеточного иммунитета, что приводит к сокращению сроков лечения и улучшению качества жизни пациентов. Представленные данные свидетельствуют о том, что у больных с опухолями головы и шеи методы физиотерапии обладают достаточным уровнем эффективности. Результаты научных исследований в данном направлении представлены как обнадеживающими, так и перспективными для дальнейшего их применения. Они открывают в будущем возможность более широкого их внедрения в онкологическую практику.
Библиографическая ссылка
Кучерова Т.Я., Штин В.И., Вусик М.В., Стахеева М.Н., Черемисина О.В. ВЛИЯНИЕ МАГНИТОЛАЗЕРА НА ПОКАЗАТЕЛИ ИММУННОЙ ЗАЩИТЫ У БОЛЬНЫХ С ОПУХОЛЯМИ НОСА И ПРИДАТОЧНЫХ ПАЗУХ // Международный журнал прикладных и фундаментальных исследований. 2019. № 8. С. 71-75;URL: https://applied-research.ru/ru/article/view?id=12828 (дата обращения: 15.05.2026).

