Гексаметилфосфортриамид (ГМФТА) представляет собой высокополярный апротонный органический растворитель, характеризующийся высокой сольватирующей способностью по отношению к неорганическим катионам и многим комплексам металлов.
Гексаметилфосфортриамид используется для растворения полимеров; как избирательный растворитель газов; как катализатор в процессах полимеризации и для стабилизации полистирола к термической деструкции, а также в качестве растворителя в органическом и неорганическом синтезе и для обработки растворов в синтезе ароматических полиамидных волокон.
Известен способ получения ГМФТА [1], который заключается в осуществлении реакции хлорокиси фосфора и диметиламина в среде ГМФТА, где он используется в качестве органического растворителя. В этом способе диметиламин смешивают с ГМФТА, в смесь постепенно добавляют хлорокись фосфора. В результате около 95 % оксихлорида фосфора превращается в ГМФТА. Реакцию проводят в основном при 0 – 40 °С, предпочтительно при температуре около 20 °С. Диметиламин, который имеет низкую температуру кипения при атмосферном давлении (7,4 °С), возвращается в реакционную систему с помощью обратного холодильника или за счет проведения реакции при повышенном давлении. Влажный осадок диметиламина гидрохлорида после фильтрования или центрифугирования содержит большое количество гексаметилфосфортриамида. Его растворяют в воде, подщелачивают, а освободившийся диметиламин отгоняют. В водном растворе содержится 10–20 % мас. ГМФТА, 10–20 % мас. неорганической соли, небольшое количество диметиламина и органических побочных продуктов реакции. Из водного раствора ГМФТА может быть выделен экстракцией эфиром с последующим разделением перегонкой. Влажный осадок также можно промывать диметиламином. Метод синтеза представляет замкнутый либо полузамкнутый процесс Достоинствами этого метода являются осуществление синтеза при температурах близких к комнатным и высокий выход продукта. При этом существенным недостатком является то, что можно получить только 4 % ГМФТА в чистом виде, остальная часть содержится в водном растворе, где присутствуют неорганические соли, диметиламин и органические побочные продукты реакции. Выделение абсолютного ГМФТА из такой смеси является сложным, многостадийным процессом и элиминирует преимущества использования ГМФТА в качестве растворителя.
Известен способ получения ГМФТА, заключающийся в обработке хлорокиси фосфора PОCl3 в толуоле избытком диметиламина [2]. Сухой диметиламин охлаждают до –60 °С и постепенно вводят в толуол. Затем по каплям в течение трех часов добавляют смесь POCl3 и толуола при перемешивании. После выпадения в осадок соли диметиламина NH(CH3)2∙HCl температуру повышают до комнатной и затем до 100 °С. Соль отфильтровывают на воронке Бюхнера, а толуол отгоняют от фильтрата под вакуумом на водоструйном насосе. Оставшееся масло очищают нагреванием с NaOH, затем экстрагируют смесь хлороформом, отделяют слой хлороформа и перегоняют гексаметилфосфортриамид при 120 °С (11 мм. рт. ст.). Выход ГМФТА составляет 60 %
Недостатком способа является то, что для проведения основного процесса необходимо поддерживать температуру –60 °С в течение трех часов, что требует дополнительных затрат энергии. Кроме того, выход продукта составляет только 60 %.
Также известны способы, где в качестве среды основной реакции используются диизопропиловый, дибутиловый эфир или хлороформ [3].
Технический результат предлагаемого изобретения заключается в увеличении выхода чистого целевого продукта реакции до 84–87 % и снижении энергозатратности производства.
Технический результат достигается тем, что в способе получения гексаметилфосфортриамида, предусматривающем обработку хлорокиси фосфора избытком диметиламина в среде толуола, добавление по каплям смеси хлорокиси фосфора и толуола, после выпадения в осадок соли хлористоводородного диметиламина повышение температуры реакции до комнатной и затем до 100 °С, отфильтровывание соли на воронке Бюхнера, отгонку толуола от фильтрата под вакуумом, выделение гексаметилфосфортриамида перегонкой при давлении 1,0–1,5 мм рт. ст., обработку хлорокиси фосфора избытком диметиламина в среде толуола проводят в присутствии катализатора – безводного хлорида алюминия при температуре -5…+5 °С.
Отличительными признаками предлагаемого способа получения гексаметилфосфортриамида являются: применение более высокой температуры в процессе основной реакции –5…+5 °С, что снижает затраты энергии на охлаждение реакционной смеси; применение безводного хлорида алюминия в качестве катализатора, что повышает выход целевого продукта реакции до 84–87 %.
Механизм действия катализатора – безводного хлорида алюминия, вероятно, аналогичен механизму каталитического алкилирования по Фриделю-Крафтсу. В качестве нуклеофила в данной реакции может выступать диметиламин. Хлорид алюминия (кислота Льюиса) способствует повышению электрофильности хлорокиси фосфора. Возможно, реакция протекает по следующему механизму:
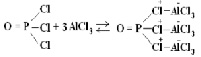
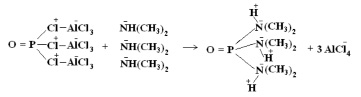
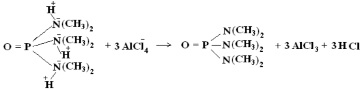
Известно, что присутствие аминов в субстрате вызывает затруднение протекания реакции по Фриделю-Крафтсу, так как амины обладают относительно высокой основностью и координируются с кислотами Льюиса, что выводит катализатор из системы. В случае реакции хлорокиси фосфора с диметиламином, диметиламин вводится в систему последним, и его добавление происходит медленно и постепенно. Таким образом, высвобождающийся катализатор – безводный хлорид алюминия взаимодействует с хлорокисью фосфора.
Экспериментальными исследованиями установлено, что проведение основной реакции при температурах –60 … –6 °С дает выход целевого продукта реакции только 60–75 %, то есть требует больших затрат энергии по охлаждению и обеспечивает меньший выход гексаметилфосфортриамида, а реализация способа получения гексаметилфосфортриамида при температурах выше +5…+10 °С осложнена летучестью диметиламина, что приводит к понижению выхода целевого продукта реакции.
Повышение температуры основной реакции до –5…+5 °С в присутствии катализатора – безводного хлорида алюминия позволяет повысить выход чистого целевого продукта реакции до 84–87 % и понизить энергозатратность производства.
Предлагаемый способ получения ГМФТА [4] поясняется чертежами, где на рис. 1 изображена схема установки для проведения основной реакции синтеза гексаметилфосфортриамида, на рис. 2 – схема установки для вакуумной перегонки.
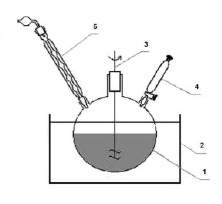
Рис. 1. Схема установки для проведения реакции синтеза ГМФТА
Установка для проведения основной реакции синтеза ГМФТА (см. рис. 1) включает трехгорлую колбу 1, которая помещена в теплообменнике или криостате 2. Приводная мешалка 3 установлена в горловине трехгорлой колбы 1. Капельная воронка 4 установлена в боковой горловине трехгорлой колбы 1. В другой горловине трехгорлой колбы 1 установлен обратный холодильник 5, который снабжен хлоркальциевой трубкой.
Схема установки для вакуумной перегонки (см. рис. 2) включает колбу 6 для вакуумной перегонки, в горловине которой установлен капилляр 7 для поступления воздуха. В боковой горловине колбы 6 для вакуумной перегонки установлен термометр 8. Сама колба 6 для вакуумной перегонки помещена в воздушную баню 9, под которой расположен нагревательный элемент 10. Разряжение в установке для вакуумной перегонки создается вакуумным насосом 11, контроль давления в системе осуществляется с помощью манометра 12. Через прямой холодильник 13 колба 6 для вакуумной перегонки соединена с алонж-пауком 14, имеющим приемные колбы 15.
Способ получения гексаметилфосфортриамида осуществляется следующим образом. В трехгорлую колбу 1 емкостью 1500 см3 (см. рис. 1) загружают 900 см3 абсолютного толуола, после чего трехгорлую колбу 1 охлаждают до температуры –5…+5 °С. Для поддержания заданной температуры используют теплообменник или криостат 2. Далее в трехгорлую колбу 1 доливают 250 см3 абсолютного диметиламина и добавляют катализатор – 0,2 г безводного хлорида алюминия (AlCl3).
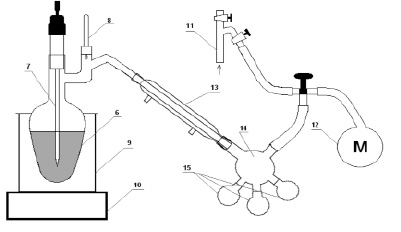
Рис. 2. Схема установки для вакуумной перегонки
В полученную смесь в течение 4 часов при постоянном перемешивании с помощью приводной мешалки 3 по каплям через капельную воронку 4 добавляют 66 г хлорокиси фосфора PОCl3, растворенной в 100 см3 толуола. По мере добавления образуется осадок хлористоводородного диметиламина. Температуру реакции доводят до комнатной и оставляют стоять в течение 6-7 часов. После этого температуру поднимают до 100 °С, нагревание продолжают в течение 2 часов, при этом пары улавливаются обратным холодильником 5, снабженным хлоркальциевой трубкой, а конденсат возвращается в реакционную смесь в трехгорлой колбе 1.
Образующийся осадок соли диметиламина NH(CH3)2∙HCl отделяют через воронку Бюхнера. Толуол отгоняют под вакуумом водоструйного насоса. Оставшийся гексаметилфосфортриамид отгоняют при вакууме 1,0–1,5 мм. рт. столба. Схема установки для перегонки представлена на рис. 2. Смесь помещают в колбу 6 для вакуумной перегонки, оснащенную капилляром 7 для поступления воздуха и термометром 8. Колбу 6 для вакуумной перегонки нагревают до температуры 69–77 °С на воздушной бане 9 при помощи нагревательного элемента 10. Разряжение создают вакуумным насосом 11 и фиксируют манометром 12. Пары гексаметилфосфортиамида конденсируются в прямом холодильнике 13, а конденсат поступает от алонжа-паука 14 в приемные колбы 15.
Отогнанный продукт представляет собой бесцветную жидкость, т. кип. 232–234 °С /760 мм рт. ст. или 70–76 °С /1,0–1,5 мм. рт. ст.; ηD20 = 1,4572; проба Бельштейна на хлорид отрицательна. Масса полученного гексаметилфосфортриамида 67 г. Выход продукта 87 %.
Вычислено, %: С 40,21; Н 10,12; N 23,45; P 17,28. C6H18N3OP
Найдено, %: С 40,45; Н 10,17; N 23,28; P 17,00.
Положение пиков спектра поглощения, см-1: 1430 – 1470 C–N
1150 – 1350 P=O
700 – 730 P–N.
Таким образом, рассматриваемый способ позволяет получить продукт реакции – ГМФТА, который представляет собой бесцветную жидкость, характеризующуюся температурой кипения 232–234 °С при давлении 760 мм. рт. ст. или 70–76 °С при 1,0 – 1,5 мм. рт. ст. и коэффициентом преломления при 20 °С ηD20 = 1,4572, проба Бельштейна на хлорид отрицательна. Элементный состав полученного продукта соответствует элементному составу гексаметилфосфортриамида. Положение пиков спектра поглощения подтверждает наличие характерных атомных групп гексаметилфосфортриамида.
Описанная методика по сравнению с известными в литературе позволяет:
- проводить основную реакцию при более высоких температурах, что обеспечивает снижение энергозатратности производства и упрощение аппаратного оформления;
- повысить выход целевого продукта реакции – гексаметилфосфортриамида до 84–87 %.
Библиографическая ссылка
Танганов Б.Б. СИНТЕЗ ДИПОЛЯРНОГО АПРОТОННОГО РАСТВОРИТЕЛЯ ГЕКСАМЕТИЛФОСФОРТРИАМИДА // Международный журнал прикладных и фундаментальных исследований. – 2013. – № 8-3. – С. 151-154;URL: https://applied-research.ru/ru/article/view?id=3941 (дата обращения: 20.04.2024).

