Тканевая инженерия является общепризнанной альтернативой аллотрансплантации при хронических заболеваниях в терминальной стадии. Возрастающая потребность в донорских органах заставляет обратить внимание на децеллюляризацию, как на перспективный метод получения биологических каркасов [3, 4]. Рецеллюляризация каркасов собственными стволовыми клетками реципиента позволит реализовать персонифицированный подход к проведению трансплантации и снизить потребность в длительной иммуносупрессивной терапии в послеоперационном периоде. Для достижения вышеупомянутых задач децеллюляризированные каркасы должны полностью воспроизводить морфологическую структуру нативных органов и обеспечивать воссоздание микроокружения для прикрепления, роста и дифференцировки стволовых клеток [2]. Децеллюляризация легких успешно проводится на моделях низших лабораторных животных с использованием различных протоколов. Наиболее перспективным считается метод перфузии легочной артерии растворами ферментов и детергентов различной концентрации. В результате применения данного метода был создан биологический каркас легких, не обладающий цитотоксическими свойствами, но с сохранением основных структурных белков внеклеточного матрикса [1]. Трансляция методов децеллюляризации в клинику требует проведения исследований на моделях крупных лабораторных животных. Наиболее перспективным является использование модели низших приматов, анатомическое строение легких которых обладает наибольшим сходством с человеческими [3].
Целью нашего исследования явилась разработка оптимального протокола децеллюляризации легких низших приматов на основе детергентно-энзиматического способа получения каркаса легких крысы.
Материалы и методы исследования
Подготовка органокомплексов к децеллюляризации
В работе было использовано 3 органокомплекса «сердце – легкие», выделенных единым блоком во время аутопсии у макак – резус (Macaca mulatta). Средний возраст животных составил 6,4 ± 2,3 года. Эксплантацию органов производили на базе НИИ медицинской приматологии РАМН. Качественная и количественная оценка нативных и децеллюляризированных каркасов легких была проведена в лаборатории международного научно-исследовательского клинико-образовательного центра регенеративной медицины на базе Кубанского государственного медицинского университета. Все исследования выполняли после одобрения протоколов исследования локальным этическим комитетом. Сразу после эксплантации органокомплексы были промыты физиологическим раствором и помещены в фосфатный буфер, содержащий 1 % раствор пенициллина-стрептомицина для транспортировки при постоянной температуре + 4 °С. После доставки в лабораторию произведено выделение легких из единого блока «сердце – легкие» хирургическим путем и промывание фосфатным буфером с добавлением раствора антибиотика – антимикотика и 5 mM этилендиаминтетрауксусной кислоты (ЭДТА). Трахея была каннюлирована на расстоянии 7 см от устья для фиксации в биореакторе, сконструированном для децеллюляризации органов крупных лабораторных животных ORCA Вioreactor (Harvard Apparatus, Массачусетс, США). От проведения вентилируемой децеллюляризации решено было отказаться в виду большого веса животного, что не позволило использовать систему Harvard Inspira Advanced Safety Ventilator (Harvard Apparatus, Массачусетс, США).
Протоколы децеллюляризации легких
Децеллюляризацию легких низших приматов проводили с использованием модификации разработанного нами детергентно-энзиматического метода [1]. Перфузия осуществлялась через трахею с последующим естественным оттоком через легочную паренхиму. Разработано три протокола получения биологических каркасов легких: (1) перфузионная децеллюляризация с использованием 2 % водного раствора дезоксихолата натрия с добавлением 0,002М натриевой соли ЭДТА; (2) перфузионная децеллюляризация легких 2 % водным раствором дезоксихолата натрия в сочетании с 0,1 % раствором Тритона Х-100; (3) последовательная децеллюляризация перфузией 2 % водного раствора дезоксихолата натрия и 0,1 % раствора Тритона Х-100 после цикла замораживания / размораживания органокомплекса при – 80 °С. Состав и последовательность воздействия ферментных растворов и буферов изменены не были. Для протоколов 1 и 2 перфузия растворов производилась в течение 4 часов с последующей паузой в перфузии на 1 час для естественного оттока децеллюляризирующих растворов. В протоколе 3 время воздействия детергентов было снижено до 2 часов, пауза в подаче растворов составила 30 минут. После завершения децеллюляризации легкие хранили в растворе фосфатного буфера с добавлением раствора антибиотика – антимикотика при температуре + 4 °С не более 1 недели для изучения качества и особенностей морфологической структуры полученных каркасов.
Морфологическая характеристика нативного и децеллюляризированного матрикса
После фиксации в 10 % нейтральном забуференном формалине образцы нативных и децеллюляризированных по трем протоколам легких дегидратировали и заключали в парафин по стандартной методике с использованием автоматического гистопроцессора Leica TP1020 (Германия) и модульной установки Leica EG1150H (Германия). Срезы толщиной 5 мкм, полученные при помощи ротационного микротома Leica RM2235 (Германия), депарафинизировали и гидратировали с последующим окрашиванием гематоксилином и эозином и флуорофором (4’,6-диамидино-2-фенилиндола) DAPI. Качественную оценку содержания гликозаминогликанов проводили после окрашивания срезов альциановым синим. Содержание коллагеновых и эластиновых волокон оценивали после окрашивания трихромом Массону.
Наряду с качественной оценкой децеллюляризации проводили количественное определение содержания ДНК в образцах легких на спектрофотометре NanoDrop ND-1000 (Thermo Fisher Scientific Inc., США) с использованием набора реагентов (Dneasy Blood and Tissue Kit, Qiagen, Швеция) по стандартному протоколу фирмы – изготовителя.
Результаты исследования и их обсуждение
В зависимости от выбранного протокола децеллюляризации время выполнения варьировало от 4 суток (протоколы 1 и 2) до 2 суток (протокол 3). После воздействия децеллюляризирующих агентов и интенсивного промывания растворами деионизированной воды и фосфатного буфера легкие сохранили форму и структуру нативных органов при изменении окраски на молочно-белую (рис. 1).
Рутинные методы гистологической окраски выявили полное отсутствие клеточных ядер и компонентов в образцах, полученных по протоколам 1–3. Незначительные повреждения альвеолярной структуры в образцах, полученных по протоколу 3, связывали с температурным воздействием на первом этапе децеллюляризации (рис. 2).
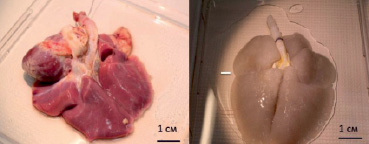
Рис. 1. Макроскопический вид нативных легких и легких после проведения децеллюляризации
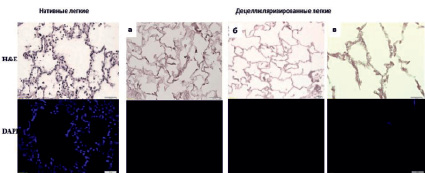
Рис. 2. Морфологическая характеристика легких низших приматов до и после децеллюляризации: (а) протокол 1; (б) протокол 2; (в) протокол 3. Окрашивание гематоксилином и эозином и DAPI. Увеличение: об х40; ок. х10
Окрашивание DAPI (рис. 2) подтверждает высокое качество проведенной децеллюляризации по протоколам 1 и 2. Следовые количества разрушенных клеточных структур после децеллюляризации по протоколу 3 позволяет рекомендовать увеличение времени промывания каркаса фосфатным буфером с 4 по 6 часов.

Рис. 3. Количественно определение уровня ДНК в легких низших приматов до и после децеллюляризации
Окрашивание трихромом по Массону позволило визуализировать сохранность коллагеновых и эластиновых волокон внеклеточного матрикса легких после децеллюляризации по всем трем протоколам, слабокислые сульфатированные гликозаминогликаны были выявлены по положительному окрашиванию срезов альциановым синим также во всех полученных образцах (данные не представлены). Большая сохранность структурных компонентов отмечена при децеллюляризации легких по протоколу 2.
Количественное определение уровня ДНК в нативных и децеллюляризированных образцах легких позволило оценить качество проведенной децеллюляризации. Около 89 % ядерного материала было удалено при обработке нативных легких растворами детергентов по протоколу 1, в то время как при использовании протоколов 2 и 3 – 82 и 66 % соответственно, р = 0,0001 (рис. 3). Количество резидуальной ДНК после децеллюляризации по протоколам 1 и 2 позволяет говорить о высоком качестве проведения процедуры.
Заключение
Перфузионная децеллюляризации легких низших приматов по протоколу 2 в наибольшей степени позволяет сохранить архитектонику получаемого каркаса при удалении большее количества чужеродного ядерного материала. Это позволяет считать указанный протокол наиболее оптимальным для получения биологических каркасов и последующего создания тканеинженерных легких.
Благодарности
Работа выполнена при поддержке государственного задания Министерства здравоохранения Российской Федерации (от 28.01.2015 г. ч. 1, раздел 1) «Разработка экспериментальных образцов тканеинженерных конструкций на основе децеллюляризированных матриксов для применения в регенеративной медицине».
Библиографическая ссылка
Куевда Е.В., Губарева Е.А., Сотниченко А.С., Гилевич И.В., Гуменюк И.С., Шаркова Т.В., Карал-оглы Д.Д., Орлов С.В., Маккиарини П., Маккиарини П. ДЕЦЕЛЛЮЛЯРИЗАЦИЯ ЛЕГКИХ НИЗШИХ ПРИМАТОВ: ОПТИМИЗАЦИЯ ПРОТОКОЛА // Международный журнал прикладных и фундаментальных исследований. 2015. № 8-2. С. 244-247;URL: https://applied-research.ru/ru/article/view?id=7076 (дата обращения: 14.01.2026).

