Арилметилиденовые производные 3Н-фуран-2-онов представляют интерес, главным образом, как промежуточные продукты способные участвовать в различных химических превращениях, приводящих к синтезу разнообразных гетероциклов [1-5]. Реакция Фриделя-Крафтса является перспективным методом синтеза соединений ароматического и неароматического ряда, способствует образованию новых С-С связей, введению различных дополнительных функций. Реакция Фриделя-Крафтса в ряду арилметилиденовых производных фуран-2-онов была изучена ранее [6-7], однако, во всех случаях авторы указывали на образование соединений, не содержащих в своем составе хлор – производных нафтойных кислот.
Нагревание 5-арил-3-арилметилиден-3Н-фуран-2-онов (Iа-в) с хлоридом алюминия в среде абсолютного бензола при постоянном перемешивании в течение часа приводит к образованию 3-(2-хлор-2-фенилвинил)-7,6R-1H-инден-1-онов (IIа-в).
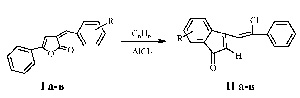
R=OH-4, OCH3-3 (Iа) R=OH-6, OCH3-7 (IIа); R=NO2-3, (Iб) R= NO2-7 (IIб); R=N(CH3)2-4, (Iв) R= N(CH3)2-6 (IIв)
Наличие хлора в данных элементного анализа, а также количество, расположение и мультиплетность сигналов в спектрах ЯМР1Н и 13С полностью соответствуют структуре соединений IIа-в.
Под действием кислоты Льюиса происходит расщепление связи С5 – О фуранонового кольца, с образованием интермедиата, стабилизация которого происходит за счёт реакции ацилирования в орто-положение активированного бензольного кольца, с образованием бициклической структуры II. Не исключалась стабилизация интермедиата за счёт внутримолекулярного алкилирования, либо реализация атаки в орто-положение активированного фенильного заместителя, что приводило бы к образованию замещенной нафтойной кислоты, однако данные направления реакции не реализуются.
Вероятно, образование иона Cl-, который далее реагирует с карбкатионом, происходит по следующей схеме:
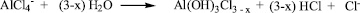
Таким образом изучена реакция Фриделя – Крафтса в ряду арилметилиденовых производных 3Н-фуран-2-онов. В результате реакции выделены продукты, отличные от описанных в литературных источниках и содержащие в своем составе хлор.
Экспериментальная часть
Спектры ЯМР1Н получены на спектрометре Varian-400 при 20-25°С в CDCl3, внутренний стандарт ТМС. Рабочая частота 400 МГц. ТСХ проводили на пластинах Silufol UV-254, элюент – гексан-этилацетат-хлороформ, 2:2:1, проявитель – пары иода.
3-(2-Хлор-2-фенилвинил)-7,6R-1H-инден-1-оны (II a-в). Смесь 0.01 моль 5-R-3-арилметилиден-3Н-фуран-2-она (I а-в), 0.01 моль хлорида алюминия нагревают при постоянном перемешивании в 15 мл абсолютного бензола в течение 1 часа. Образующуюся смесь обрабатывают разбавленной соляной кислотой. Выпавшие кристаллы отфильтровывают, промывают подкисленным раствором воды и перекристаллизовывают из бензола.
3-(2-хлор-2-фенилвинил)-6-гидрокси-7-метокси-1H-инден-1-он (II a). Выход 86 %, т. пл.155-157 ºС. Спектр ЯМР 1Н, δ, м.д.: 3.65 с (3Н, OCH3), 5.15 c (1H, OH), 6.95 с (1Н, C-2), 7.28 с (1Н, Cэкзо -2), 7.35-7.57 м (7Н, Ar), 6.95 с (1Н, C-2). ЯМР13С, δ, м.д.: 54.3, 114.1, 115.8, 119.3, 121.9, 123.3, 125.7, 127.3, 129.1, 130.9, 132.6, 133.5, 145.2, 147.3, 156.3, 197.4. Найдено, % С 68.76; Н 3.81; Cl 10.97. C18H13ClO3 Вычислено, % С 69.13; Н 4.19; Cl 11.34.
3-(2-хлор-2-фенилвинил)-7-нитро-1H-инден-1-он (II б) Выход: 79 %, т. пл. 207-209ºС. Спектр ЯМР 1Н, δ, м.д.: 6.93 с (1Н, C-2), 7.25 с (1Н, Cэкзо -2), 7.25-7.67 м (8Н, Ar), 6.95 с (1Н, C-2). ЯМР13С, δ, м.д.: 114.1, 115.8, 119.3, 121.9, 123.3, 125.7, 127.3, 129.1, 130.9, 132.6, 133.5, 145.2, 147.3, 156.3, 197.4. Найдено, % С 65.14; Н 3.66; Cl 11.07; N 4.75. C17H10ClNO3 Вычислено, % С 65.50; Н 3.23; Cl 11.37; N 4.49.
3-(2-хлор-2-фенилвинил)-6-(диметиламино)-1H-инден-1-он (II в). Выход: 83 %, т. пл. 179-181ºС. Спектр ЯМР 1Н, δ, м.д.: 6.98 с (1Н, C-2), 7.22 с (1Н, Cэкзо -2), 7.21-7.42 м (8Н, Ar), 7.05 с (1Н, C-2). ЯМР13С, δ, м.д.: 114.1, 115.8, 119.3, 121.9, 123.3, 125.7, 127.3, 129.1, 130.9, 132.6, 133.5, 145.2, 147.3, 156.3, 197.4. Найдено, % С 73.15; Н 5.76; Cl 11.75; N 4.32. C19H16ClNO Вычислено, % С 73.66; Н 5.21; Cl 11.44; N 4.52.
Исследование выполнено за счет гранта Российского Научного Фонда ( проект № 15-13-10007).
Библиографическая ссылка
Аниськова Т.В., Веревочкин А.А., Леденева И.В., Егорова А.Ю. 3-АРИЛМЕТИЛИДЕН-3Н-ФУРАН-2-ОНЫ В РЕАКЦИИ ФРИДЕЛЯ-КРАФТСА // Международный журнал прикладных и фундаментальных исследований. 2015. № 11-4. С. 543-544;URL: https://applied-research.ru/ru/article/view?id=7779 (дата обращения: 16.01.2026).

