Scientific journal
International Journal of Applied and fundamental research
ISSN 1996-3955
ИФ РИНЦ = 0,556
OBTAINING OF COPPER NANOPARTICLES BY THERMAL DECOMPOSITION OF THE FORMATE COMPLEX OF COPPER WITH TRIETHYLAMINE
В последнее время большой интерес проявляется к разработке методов синтеза и изучению свойств наночастиц меди. Связано это с тем, что наночастицы меди находят применение в катализе, оптических, сенсорных и электронных устройствах, они способны также повысить не только прочность лакокрасочных покрытий, но и увеличить их электро- и теплопроводность [1-3]. В работе [4] изучены процессы получения полимерных композиционных материалов (ПКМ), наполненных наночастицами меди, железа, кобальта и никеля, путем термического разложения соответствующих формиатов или ацетилацетонатов в эпоксидной смоле ЭД-20. Однако получить наполнение металлов в эпоксидной смоле более 1% не удавалось, так как при температуре разложения указанных выше соединений-предшественников (200-250оС) происходит термическая полимеризация и частичная деструкция эпоксидной смолы. Для наполнения ПКМ начочастицами меди можно использовать также комплекс из сульфата меди и моноэтаноламина [5]. Однако синтез этого комплекса требует высоких температур и длительного времени.
Важно получить такой медьсодержащий прекурсор, чтобы при температуре его разложения полимерная матрица не подвергалась деструкции.
Цель работы – получение наночастиц меди в среде полимера путем разложения комплекса формиата меди с триэтиламином при сравнительно низких температурах.
Материалы и методы исследования
Для получения наночастиц меди был выбран метод термического разложения формиата меди и его комплекса с триэтиламином. В качестве исходных материалов использовали:
– кристаллогидрат сульфата меди CuSO4•5H2O марки «х.ч.» по ГОСТ 4165–78;
– карбонат натрия Na2CO3 марки А по ГОСТ 5100–85;
– муравьиная кислота HCOOH марки «ч.д.а.» по ГОСТ 5848–73;
– триэтиламин (С2Н5)3N технический по ГОСТ 9966–88.
Для синтеза формиата меди использовали 1М раствор кристаллогидрата сульфата меди CuSO4•5H2O и 1М раствор карбоната натрия Na2CO3. Приготовленные растворы объёмом 50 мл смешивали для получения карбоната меди:
CuSO4•5H2O + Na2CO3 > Na2SO4 + +CuCO3v + 5H2O.
Для отделения осадка раствор фильтровали под вакуумом, используя установку, состоящую из воронки Бюхнера, колбы Бунзена и вакуум-насоса системы Комовского. Осадок карбоната меди переносили в колбу для промывания с применением декантации: заливали дистиллированной водой и взбалтывали его при помощи стеклянной палочки. После отстаивания жидкость осторожно сливали, но так, чтобы осадок оставался в колбе. К оставшемуся в колбе осадку снова приливали промывную воду и повторяли сливание жидкости. Полноту отмывки на содержание сульфат-ионов SO42– проверяли раствором хлорида бария.
К карбонату меди порционно добавляли концентрированную муравьиную кислоту при тщательном перемешивании. В результате реакции образовывается формиат меди синего цвета:
CuCO3v + 2HCOOH + Н2О > >Cu(HCOO)2•2H2O + CO2.
С целью получения аминного комплекса синтезированный формиат меди смешивали с триэтиламином. Образование комплекса идет по следующему уравнению
Cu(HCOO)2•2Н2О + 3(С2Н5)3N > >Cu(HCOO)2•3(С2Н5)3N + 2Н2О.
Триэтиламин прибавляли при комнатной температуре к формиату меди порционно, непрерывно перемешивая, до образования между ними комплекса ярко-зеленого цвета.
Полученный комплекс формиата меди с триэтиламином сушили в эксикаторе над концентрированной серной кислотой.
Идентификацию фаз, образующихся при разложении формиата меди и его комплекса с триэтиламином, проводили рентгенофазовым анализом (РФА) на порошковом дифрактометре ARL X TRA (ThermoFisher Scientific, Швейцария).
Термический анализ синтезированного формиата меди проводили в атмосфере воздуха в условиях неизотермического нагрева с эталоном a-Al2O3 при скорости нагрева 10 град/мин в интервале температур 25–800оС (дериватограф Perking Elmer Diamond TG/DTA).
Результаты исследования и их обсуждение
Образование формиата меди было подтверждено РФА (рис. 1).
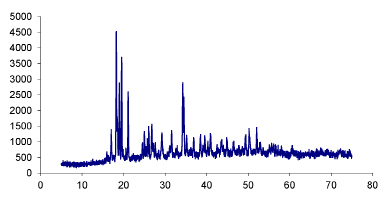
Рис. 1. Рентгенограмма формиата меди Cu(HCOO)2•2H2O
Для идентификации исследуемого образца на рентгенограмме фиксировали наиболее интенсивные пики, для которых отмечали углы 2θ и интенсивности. Значения этих параметров сравнивали c табличными данными в базе картотеки PDF-2 (табл. 1).
Таблица 1
Значения угла 2θ для формиата меди Cu(HCOO)2•2Н2О
|
Значение угла 2θ |
Относительная интенсивность |
№ картотеки |
|
18,16 |
100 |
16–9–54 |
|
18,94 |
65 |
|
|
19,45 |
85 |
Из данных табл. 1 видно, что синтезированный образец соли отвечает составу формиата меди Cu(HCOO)2•2Н2О. РФА показал, что в полученном образце формиата меди присутствует незначительная примесь сульфата натрия и муравьиной кислоты.
Результаты дифференциальной сканирующей калориметрии и термогравиметрии разложения формиата меди представлены на рис. 2.
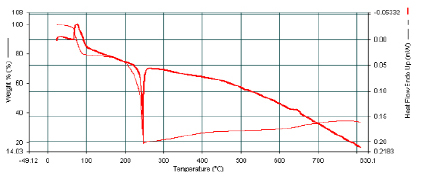
Рис. 2. Кривые ДСК и ТГ формиата меди Cu(HCOO)2•2H2O
Из кривых ТГ и ДСК видно, что процесс термического разложения формиата меди характеризуется эндотермическим эффектом. Температура начала разложения – 200 оС, а конец разложения – 250оС. В этом температурном интервале процесс разложения формиата меди протекает с очень большой скоростью с потерей массы до 55%.
Формиат меди в температурном интервале от 200 до 250оС разлагается с образованием наночастиц меди по следующему уравнению:
Cu(HCOO)2 > Cuv + H2O + CO + CO2.
В условиях нагрева образовавшиеся в результате реакции частицы меди окисляются кислородом воздуха до оксида меди (I), который с поверхности переходит в оксид меди (II) черного цвета. На эти процессы указывает ход кривой ТГ: в интервале температур 250–750оС идет постепенное увеличение массы образца от 20 до 38%. Из хода кривой ТГ видно также, что интенсивное образование оксида меди (II) начинается с 600оС.
Получение ПКМ, наполненных наночастицами меди в результате термического разложения формиата Cu(HCOO)2 при температуре от 200 до 250оС, проблематично. При такой температуре многие полимеры претерпевают частичную деструкцию.
Поэтому следующим этапом исследований было получение комплекса формиата меди с триэтиламином Cu(HCOO)2•3(С2Н5)3N. Данные РФА подтверждают получение аминного комплекса (рис. 3).
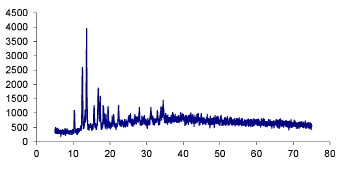
Рис. 3. Рентгенограмма комплекса формиата меди с триэтиламином
По данным [1] синтезированный комплекс формиата меди с тириэтиламином разлагается при температуре 120 оС. Эта температура является комфортной для многих полимеров и их олигомеров. Его разложение протекает по следующему возможному уравнению:
Cu(HCOO)2•3(С2Н5)3N > Cuv + H2O + +CO + CO2 + 3NH3 + 9C2H4.
Образование наночастиц меди с примесями оксидов меди (I) и (II) было также подтверждено РФА (рис. 4).
Результаты измерений рентгенограммы образца, полученного в результате разложения комплекса формиата меди с триэтиламином, приведены в табл. 2.
При расшифровке рентгенограммы образца было обнаружено две фазы: медь и небольшая примесь оксида меди (II).
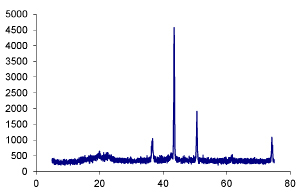
Рис. 4. Рентгенограмма меди, полученной в результате разложения комплеса формиата меди с триэтиламином Cu(HCOO)2•3(С2Н5)3N
Таблица 2
Значения угла 2θ для меди, полученной из комплекса Cu(HCOO)2•3(С2Н5)3N
|
Значение угла 2θ |
Относительная интенсивность |
|
43,50 |
100 |
|
50,64 |
40 |
|
74,26 |
20 |
Для стабилизации наночастиц меди, образующихся в результате термического разложения комплекса формиата меди с триэтиламином, этот процесс необходимо проводить в среде полимера, устойчивого до 150оС. Таким полимером может служить поливиниловый спирт (ПВС), деструкция которого начинается при температуре 200оС [6].
Для стабилизации наночастиц меди применяли водный раствор ПВС, который готовили в дистиллированной воде на водяной бане при температуре 60–70оС. В среде раствора ПВС проводили термическое разложение комплекса Cu(HCO)2•3(С2Н5)3N до полного испарения воды. Наночастицы меди обволакиваются полимером и стабилизируются.
Аналогичным образом могут быть получены и другие полимерные композиционные материалы, содержащие высокодисперсную медь.
Выводы
1. Показано, что формиат меди не может быть использован как прекурсор для наполнения высокодисперсной медью ПКМ, так как при температуре его разложения большинство полимеров подвергаются деструкции.
2. Установлено, что комплекс формиата меди с триэтиламином разлагается при сравнительно низкой температуре и поэтому может служить прекурсором для наполнения большинства полимеров высокодисперсной медью.
Библиографическая ссылка
Евстифеев Е.Н., Новикова А.А. ПОЛУЧЕНИЕ НАНОЧАСТИЦ МЕДИ ТЕРМИЧЕСКИМ РАЗЛОЖЕНИЕМ КОМПЛЕКСА ФОРМИАТА МЕДИ С ТРИЭТИЛАМИНОМ // Международный журнал прикладных и фундаментальных исследований. 2017. № 9. С. 135-139;URL: https://applied-research.ru/en/article/view?id=11842 (дата обращения: 11.05.2026).

