Scientific journal
International Journal of Applied and fundamental research
ISSN 1996-3955
ИФ РИНЦ = 0,556
SUNFLOWER AND RAPE LETSITINA AS INHIBITORS OF CORROSION STEEL
Лецитины или фосфатидилхолины – соединения общей формулы ROCH2-CH(OR’)CH2OP(O)(O’)O(CH2)2N(CH3)3, где R-обычно ацил насыщенной, R’-ненасыщенной кислоты с 16-24 атомами С в цепи (преобладают кислоты С16 и С18) [4,1]. Состав и свойства сырых лецитинов зависят от источника, условий получения и исходного спектра составляющих их фосфолипидов. Основными фосфолипидами, содержащимися в рапсовых лецитинах в отличие от подсолнечных, являются фосфатидилхолины и фосфатидил-этаноламины. Кроме этого в рапсовом лецитине больше олеиновой кислоты, но меньше высших насыщенных кислот, чем в подсолнечном [4, 1].
Рапсовое масло, отстои подсолнечного масла и фосфолипиды исследовались как ингибиторы атмосферной коррозии и коррозии ряда металлов в нейтральных средах [2-3]. Поскольку в сырых лецитинах одновременно содержатся масла, фосфолипиды, насыщенные и ненасыщенные жирные кислоты, представлялось целесообразным рассмотреть их в качестве ингибиторов коррозии низкоуглеродистой стали [6-8]. Несомненным достоинством данных реагентов является экологическая безопасность, доступность и дешевизна.
Материалы и методы исследования
В качестве ингибиторов коррозии исследовали растворы подсолнечного (ПЛ) и рапсового (РЛ) в дизельном топливе. Массовая доля лецитинов составляла 10 %. Коррозионное поведение стали 3 изучали в 3 %-ном растворе хлорида натрия без и в присутствии лецитинов с концентрацией С = 25-150 мг/л. Коррозионные измерения проведены в статическом и динамическом режиме, методика и оценка эффективности ингибиторов описаны ранее [9].
Электрохимические измерения проводили на неподвижном электроде (S = 1 см2) на потенциостате ПИ-50-1.1 в термостатируемой трехэлектродной ячейке с разделенными католитом и анолитом. Электрод сравнения – насыщенный хлорсеребряный, вспомогательный – платиновый. Потенциалы (Е) приведены относительно нас. х.с.э. Поляризационные кривые снимали ступенчато от меньшего Е к большему с выдержкой 1 минута при каждом значении потенциала. Интервал рабочих температур – 20-55 °С.
Результаты исследования и их обсуждение
Влияние растворов рапсового и подсолнечного лецитинов на коррозию стали 3 в нейтральных средах исследовали в двух режимах – статическом и динамическом. Скорости коррозии K стали 3 при различных концентрациях изученных лецитинов, коэффициенты торможения g и степень защиты Z представлены в табл. 1.
Таблица 1
Скорость коррозии стали 3, коэффициенты торможения и степень защиты в зависимости от режима коррозионных измерений и концентрации лецитинов
|
С, мг/л |
K,г/(м2час) |
g |
Z, % |
K,г/(м2час) |
g |
Z, % |
|
статика, j0 = 0,110 г/(м2час) |
динамика j0 = 0,063 г/(м2час) |
|||||
|
Рапсовый лецитин |
||||||
|
50 |
0,140 |
7,7 |
86,9 |
0,0770 |
0,8 |
- |
|
75 |
0,025 |
8,7 |
88,5 |
0,0660 |
1,0 |
- |
|
100 |
0,004 |
26,0 |
96,2 |
0,0300 |
2,1 |
52,6 |
|
125 |
0,004 |
26,0 |
96,2 |
0,0250 |
2,5 |
60,5 |
|
150 |
0,004 |
26,0 |
96,2 |
0,0200 |
3,2 |
68,5 |
|
Подсолнечный лецитин |
||||||
|
50 |
0,017 |
6,5 |
84,6 |
0,0230 |
2,6 |
61,1 |
|
75 |
0,010 |
10,4 |
90,4 |
0,0200 |
3,1 |
66,7 |
|
100 |
0,006 |
19,5 |
94,9 |
0,0030 |
18,0 |
94,4 |
|
125 |
0,004 |
26,0 |
96,2 |
0,0013 |
45,0 |
97,8 |
|
150 |
0,004 |
26,0 |
96,2 |
0,0013 |
45,0 |
97,8 |
Как видно из табличных данных оба лецитина могут быть рекомендованы как ингибиторы коррозии в нейтральных хлоридных средах, поскольку независимо от режима проведения коррозионных испытаний они обеспечивают высокую степень защиты низкоуглеродистой стали.
В статических условиях выход на предельную степень защиты реализуется при концентрации 100 мг/л. В динамическом режиме для рапсового лецитина в исследованном концентрационном диапазоне предельная степень защиты не реализуется. В случае же подсолнечного лецитина максимальная степень защиты наблюдается при С = 125 мг/л. Отсутствие предельной степени защиты или ее реализация при больших С по сравнению с статическим режимом связано с затруднением образования пленки ингибитора на поверхности стали. Исследованные лецитины проявляют защитные свойства за счет формирования на поверхности металла пленок фосфор- содержащих анионов ингибитора, а также радикалов ненасыщеных кислот, которые блокируют образование комплекса Fe(OH)адс
и затрудняют протекание коррозии стали.
Отличие коэффициентов торможения рапсового и подсолнечного лецитинов при динамических измерениях можно связать с разным их составом и, соответственно, разной способностью образовывать защитную пленку на стали. Известно, что масло и фосфолипиды, содержащиеся в рапсовых лецитинах, по степени ненасыщенности жирных кислот значительно отличаются от масла и фосфолипидов, содержащихся в подсолнечных лецитинах. Содержание мононенасыщенных жирных кислот, в том числе олеиновой кислоты, в масле и фосфолипидах, выделенных из рапсовых лецитинов, выше в 2,4 и 3,4 раза соответственно, по сравнению с содержанием указанных кислот в масле и фосфолипидах, выделенных из подсолнечных лецитинов. В тоже время содержание полиненасыщенных жирных кислот в масле и фосфолипидах, выделенных из рапсовых лецитинов, значительно ниже, чем в масле и фосфолипидах, выделенных из подсолнечных лецитинов. Отличительной особенностью жирнокислотного состава масла и фосфолипидов, содержащихся в рапсовых лецитинах, по сравнению с подсолнечными лецитинами, является присутствие незначительного количества эруковой (цис-13-докозеновой) кислоты [4].
Различие в химическом составе рапсового и подсолнечного лецитинов проявляется и в их влиянии на частные электродные реакции коррозионного процесса при изменении температуры.
В нейтральных неаэрированных хлоридных средах коррозия стали протекает со смешанной кислородно-водородной деполяризацией. Лецитины создают на поверхности стали собственную пленку, которая является дополнительным механическим барьером для восстановления водорода и диффузии растворенного кислорода к поверхности стали. Подсолнечный лецитин практически при всех исследованных концентрациях уменьшает потенциал коррозии стали 3 и снижает скорость катодной реакции, а рапсовый при больших С увеличивает Екор и поляризуемость анодной реакции, рис. 1.
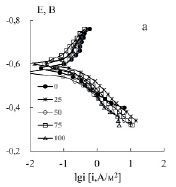
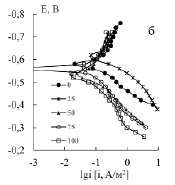
Рис. 1. Поляризационные кривые стали 3 в хлоридном растворе без (0) и в присутствии подсолнечного (а) и рапсового (б) лецитинов. Цифры на графиках – концентрация лецитинов
Таблица 2
Зависимость коэффициента торможения от потенциала, концентрации и природы лецитина, t = 20 °C
|
-Е, В |
Значения g для концентраций лецитинов, С (мг/л) |
|||||||
|
25 |
50 |
75 |
100 |
|||||
|
РЛ |
ПЛ |
РЛ |
ПЛ |
РЛ |
ПЛ |
РЛ |
ПЛ |
|
|
0,72 |
1,09 |
1,26 |
1,26 |
1,26 |
1,86 |
1,58 |
1,20 |
1,26 |
|
0,70 |
1,12 |
1,41 |
1,74 |
1,17 |
1,74 |
1,78 |
1,35 |
1,41 |
|
0,65 |
1,41 |
1,70 |
1,78 |
1,15 |
1,70 |
1,70 |
1,62 |
1,66 |
|
0,50 |
0,19 |
0,35 |
5,01 |
1,12 |
3,02 |
0,58 |
7,94 |
0,71 |
|
0,45 |
0,32 |
0,56 |
5,01 |
1,51 |
4,57 |
0,89 |
7,41 |
1,35 |
|
0,40 |
0,89 |
1,35 |
10,72 |
3,39 |
13,49 |
2,04 |
16,98 |
4,07 |
Таблица 3
Значения эффективной энергии активации коррозии, катодной (-0,64 В) и анодной (-0,36 В) реакции, Слец = 100 мг/л
|
Среда |
Значения Еак (кДж/моль) для потенциалов- Е,В |
||
|
Екор |
0,64 |
0,36 |
|
|
3 %-ный NaCl |
86,5 |
22,6 |
133,2 |
|
3 %-ный NaCl + РЛ |
101,3 |
34,1 |
189,0 |
|
3 %-ный NaCl + ПЛ |
92,5 |
37,2 |
115,9 |
Торможение подсолнечным лецитином катодной реакции и уменьшение Екор ведет к кажущемуся стимулированию анодной реакции в более электроотрицательной области потенциалов. При Е > -0,38В при большинстве С стимулирование сменяется торможением процесса, табл. 2.
Рапсовый лецитин в большей степени при С > 50 мг/л тормозит анодную реакцию.
Защитное действие лецитинов зависит от температуры t. Увеличение t по-разному влияет на коррозию стали, протекающую с чисто кислородной и чисто водородной деполяризацией. Известно, что увеличение скорости коррозии в два раза наблюдается при росте температуры на 30 и 10 °С если процесс протекает с кислородной и водородной деполяризацией соответственно [5]. Следует заметить, что скорость коррозии стали, определенная из поляризационных измерений, при повышении температуры на 30 °С не удваивается, как должно быть в случае только кислородной деполяризации, а растет практически в четыре с половиной раза. В случае, чисто водородной деполяризации она должна была увеличиться почти в шесть раз. Из вышеуказанного следует, что вклад водородной деполяризации достаточно большой. В согласии с этим находятся и расчетные значения эффективной энергии активации коррозии и частных электродных реакций, табл. 3.
Полученные значения Еак свидетельствуют о том, что катодная реакция протекает в условиях смешанного диффузионно-кинетического контроля, а коррозия и анодная реакция – кинетического. Исследованные лецитины увеличивают эффективную энергию активации коррозии и катодной реакции, подсолнечный лецитин уменьшает ее значение для анодной реакции, табл. 3. Практически при всех исследованных t лецитины тормозят анодный и катодный процессы на стали 3, рис. 2. Оба лецитина увеличивают потенциал коррозии стали, что может свидетельствовать о преимущественном торможении анодной реакции.
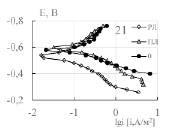
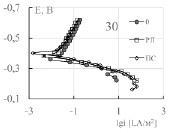
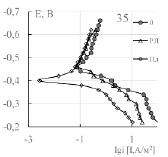
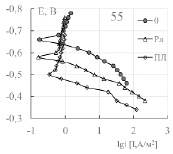
Рис. 2. Поляризационные кривые стали 3 в хлоридном растворе без (0) и при наличии лецитинов (РЛ,ПЛ) при разных температурах, С = 100 мг/л. Название диаграммы- температура, °С
Существенное изменение потенциала коррозии в присутствии лецитинов затрудняет расчет коэффициентов торможения при одинаковых потенциалах и зачастую вызывает кажущееся стимулирование процесса, рис. 2. При этом, следует отметить, что оба лецитина в большей части увеличивают поляризуемость ba анодной реакции в исследованном температурном интервале, табл. 4.
Таблица 4
Зависимость ba от температуры и природы лецитина
|
t, °C |
Значения ba (мВ) для лецитинов |
||
|
0 |
ПЛ |
РЛ |
|
|
30 |
55 |
56 |
55 |
|
35 |
50 |
100 |
75 |
|
40 |
55 |
125 |
133 |
|
45 |
71 |
125 |
120 |
|
50 |
67 |
57 |
125 |
|
55 |
63 |
63 |
67 |
Рост температуры не приводит к изменению механизма растворения стали в хлоридном растворе без лецитинов. В интервале температуры от 35 до 50 С рапсовый и подсолнечный лецитины меняют механизм растворения стали, о чем свидетельствуют повышенные значения тафелевого коэффициента.
Выводы
1. Растворы подсолнечного и рапсового лецитинов с массовой долей 10–25 % в дизельном топливе могут использоваться как ингибиторы коррозии стали в нейтральных хлоридных и высоко минерализованных средах.
2 При коррозии стали в обычных условиях предельная степень защиты реализуется при дозировке 10-ти процентных лецитиновых растворов 100 мг/л. Данная концентрация обеспечивает требуемую защиту стали в нейтральных средах как в статических, так и в динамических условиях.
3. Защитное действие лецитинов связано как с образованием пленки, так и изменением кажущейся энергии активации протекающих процессов.
Библиографическая ссылка
Бережная А.Г., Иващенко О.А., Чернявина В.В. ПОДСОЛНЕЧНЫЙ И РАПСОВЫЙ ЛЕЦИТИНЫ КАК ИНГИБИТОРЫ КОРРОЗИИ СТАЛИ // Международный журнал прикладных и фундаментальных исследований. 2016. № 8-3. С. 365-369;URL: https://applied-research.ru/en/article/view?id=10035 (дата обращения: 05.06.2026).

