Scientific journal
International Journal of Applied and fundamental research
ISSN 1996-3955
ИФ РИНЦ = 0,556
INFLUENCE OF TRANSAMINASES, EXCRETED BY PSEUDOMONAS AERUGINOSA, ON OXIDATIVE METABOLISM OF PERITONEAL CELLS OF GUINEA PIGS AND MOUSE IN VITRO
Pseudomonas aeruginosa обладает различными факторами вирулентности, одним из которых является липополисахарид (ЛПС). Он накапливается в организме при лизисе бактериальных клеток и вызывает разнообразные поражения организма. При этом в окружающую среду выделяются и разнообразные ферменты, в частности, ферменты энергетического обмена. Ранее для крыс было показано in vitro выделение гепатоцитами АСТ и АЛТ в ответ на ЛПС изолятов P. aeruginosa и влияние этих ферментов на дыхание активированных данными ЛПС перитонеальных клеток (ПК), при этом дыхание зависит от активности АЛТ и АСТ [1]. Также было показано, что дыхание перитонеальных клеток морской свинки при фагоцитозе клеток Mycobacterium bovis стимулируется АЛТ и АСТ in vitro [2].
Целью данной работы было обнаружение способности культур вирулентных и авирулентных изолятов P. aeruginosa выделять в среду ферментативные активности АСТ и АЛТ, и определение характера влияния указанных ферментов на дыхание перитонеальных клеток мыши и морской свинки в присутствии ЛПС указанных изолятов псевдомонад.
Материалы и методы исследования
В работе использовались изоляты P. aeruginosa 4, 8 (вирулентные), 11, 12, (авирулентные). Из суточных культур изолятов на жидкой среде № 8 (Оболенск) получали очищенные центрифугированием (20000g, 40 мин) культуральные жидкости (КЖ) и клетки бактерии. В полученных супернатантах определяли концентрацию белка, активность АСТ, АЛТ и рассчитывали отношение АСТ/АЛТ (коэффициент Де Ритиса) [3]. Из клеток изолятов получали ЛПС по Вестфалю [6].
Определяли дыхание перитонеальных клеток (ПК) в тесте восстановления нитросинего тетразолия (тест НСТ) [5, 7, 8] при ответе на ЛПС P. aeruginosa 8 в зависимости от концентрации пирувата и α-кетоглутарата. ПК мыши и морской свинки (от 10 животных каждого вида) суспендировали в среде ДМЕМ до концентраций 1 млн клеток/мл; в суспензии вносили нитросиний тетразолий (НСТ) до конечной концентрации 0,01 %. Суспензии ПК делили на ряд аликвот, в аликвоты, кроме контрольной, вносили ЛПС P. aeruginosa 8 до конечной концентрации 4 мкг/мл. В аликвоты суспензий ПК добавляли пируват в концентрациях 54 – 120 мкМ/л, α-кетоглутарат – от 23 до 51 мкМ/л и их сочетания. Суспензии ПК инкубировали 1 час при 37 °С, определяли накопление формазана спектрофотометрически.
Влияние культуральных жидкостей изолятов P. aeruginosa на дыхание ПК определяли аналогично описанному выше. ПК мыши и морской свинки суспендировали в среде 199, добавляли 1/10 объема КЖ, получая суспензии 1 млн клеток/мл, вносили ЛПС соответствующего изолята до 4 мкг/мл и определяли накопление формазана в тесте НСТ.
Определяли коэффициенты корреляции Пирсона и множественной корреляции между дыханием ПК в тесте НСТ и концентрациями пирувата и α-кетоглутарата, а также активностями АЛТ, АСТ и значениями коэффициента Де Ритиса [4].
Результаты исследования и их обсуждение
Накопление формазана в тесте НСТ ПК мыши и морской свинки, стимулированных ЛПС P. aeruginosa 8, в присутствии пирувата и α-кетоглутарата представлено на рисунке. ЛПС стимулирует дыхание, дыхание контрольных ПК мыши составляет 27 ± 6 нг/млн. клеток, контрольных ПК морской свинки – 34 ± 5 нг/млн. клеток. А-кетоглутарат и пируват стимулируют дыхание ПК, причем первый заметно сильнее при 37 мкМ, второй – при 94 мкМ. При этом максимум дыхания ПК как мыши, так и морской свинки достигается при сочетании пируват/αp>
Корреляционный анализ более отчетливо выявляет связь дыхания с пируватом и α-кетоглутаратом (табл. 1).
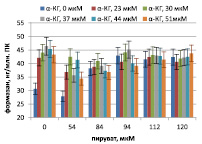
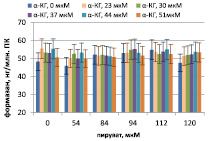
А Б
Дыхание перитонеальных клеток мышей (А) и морских свинок (Б), стимулированных ЛПС P. aeruginosa 8, в присутствии пирувата и α-кетоглутарата (α-КГ)
Таблица 1
Значения коэффициентов корреляции Пирсона (r) и множественной корреляции (R) дыхания перитонеальных клеток мыши и морской свинки с пируватом и α-кетоглутаратом в присутствии ЛПС P. Aeruginosa 8
|
НСТ ПК мыши |
НСТ ПК морской свинки |
||
|
Пируват, r |
С чистым пируватом |
+ 0,83 |
+ 0.46 |
|
В присутствии α-кетоглутарата |
+ 0,96 |
+ 0.89 |
|
|
α-кетоглутарат, r |
С чистым α-кетоглутаратом |
+ 0,86 |
+ 0.43 |
|
В присутствии пирувата |
+ 0,93 |
+ 0.87 |
|
|
Корреляция с парой пируват/α-кетоглутарат, R |
0,96 |
0.90 |
|
Примечание: жирным шрифтом выделены достоверные значения коэффициентов корреляции (p < 0.05).
Дыхание ПК мыши связано с обеими кетокислотами вместе и с каждой из них в отдельности, однако и дыхание ПК морской свинки в присутствии обеих кетокислот связано с каждой из них. Об этом же свидетельствуют высокие достоверные коэффициенты множественной корреляции дыхания ПК с парой пируват/α-кетоглутарат, т.е. обе кетокислоты стимулируют дыхание ПК обоих видов животных. Результат вполне объясним тем, что эти кетокислоты утилизируются в цикле Кребса, рост их концентрации в среде позволяет усилить дыхательный метаболизм ПК при ответе на антиген.
Изоляты P. aeruginosa выделяют в культуральную жидкость заметное количество белка и активности АСТ и АЛТ (табл. 2). Выделение ферментативных активностей соотносится с выделением белка и не имеет выраженной связи с вирулентностью изолята.
Таблица 2
Биохимические параметры культуральных жидкостей изолятов P. aeruginosa
|
изолят |
Белок, г/л |
АСТ, нкат/л |
АЛТ, нкат/л |
Коэффициент Де Ритиса |
|
|
вирулентные |
4 |
0,49 ± 0,1 |
0,47 ± 0,1 |
0,20 ± 0,1 |
2,31 ± 0,3 |
|
8 |
1,82 ± 0,3 |
3,92 ± 0,5 |
1,00 ± 0,2 |
3,91 ± 0,5 |
|
|
авирулентные |
11 |
0,99 ± 0,2 |
2,60 ± 0,4 |
0,45 ± 0,1 |
5,67 ± 0,6 |
|
12 |
1,53 ± 0,2 |
0,73 ± 0,2 |
0,33 ± 0,1 |
2,26 ± 0,3 |
Культуральные жидкости в сочетании с ЛПС изолятов P. aeruginosa оказывают стимулирующее влияние на дыхание ПК, причем это влияние мало зависит от вирулентности изолята (табл. 3).
Таблица 3
Накопление формазана перитонеальными клетками (ПК) морской свинки и мыши в присутствии культуральных жидкостей (КЖ) и липополисахарида (ЛПС) изолятов P. aeruginosa, нг формазана на млн. ПК
|
Вирулентные изоляты |
Авирулентные изоляты |
Среда ДМЕМ |
|||
|
КЖ + ЛПС изолята 4 |
КЖ + ЛПС изолята 8 |
КЖ + ЛПС изолята 11 |
КЖ + ЛПС изолята 12 |
||
|
ПК морской свинки |
14,1 ± 1,6 |
19,7 ± 6,1 |
20,6 ± 4,7 |
17,9 ± 2,6 |
11,9 ± 1,5 |
|
ПК мыши |
8,4 ± 0,6 |
8,9 ± 0,7 |
8,7 ± 0,9 |
8,4 ± 0,7 |
7,8 ± 0,5 |
Примечание: жирным шрифтом выделены значения, достоверно отличающиеся от контроля (p < 0.05).
Дыхание перитонеальных клеток положительно связано с активностями АЛТ и АСТ, а также с коэффициентом Де Ритиса, о чем свидетельствуют значения коэффициентов корреляции Пирсона между дыханием ПК и указанными биохимическими параметрами КЖ (табл. 4).
Таблица 4
Значения коэффициентов корреляции Пирсона дыхания перитонеальных клеток (ПК) мыши и морской свинки с активностью АЛТ, АСТ и коэффициентом Де Ритиса в присутствии ЛПС P. aeruginosa
|
ПК мыши |
ПК морской свинки |
|
|
Корреляция с АЛТ |
+ 0,69 |
+ 0,67 |
|
Корреляция с АСТ |
+ 0,65 |
+ 0,70 |
|
Корреляция с коэффициентом Де Ритиса |
+ 0,60 |
+ 0,42 |
Примечание: жирным шрифтом выделены достоверные значения коэффициентов корреляции (p < 0.05).
В среде ДМЕМ отсутствовали специфические факторы регуляции активности перитонеальных клеток со стороны макроорганизма (комплемент, интерлейкины и т.д.), это означает, что действие трансаминаз на дыхание связано именно с катализируемыми трансаминазами биохимическими реакциями.
АЛТ катализирует обратимое превращение L-аланина и α-кетоглутарата в пируват и L-глутматат, АСТ стимулирует обратимое превращение L-аспартата и α-кетоглутарата в оксалоацетат и L-глутматат. Сопряженные реакции, катализируемые АЛТ и АСТ, способны поддерживать равновесную концентрацию кетокислот, причем повышенная активность АЛТ ведет к накоплению в среде пирувата, АСТ – к накоплению α-кетоглутарата, т.е. кетокислот, стимулирующих дыхание перитонеальных клеток (табл. 1). Таким образом, положительная связь дыхания перитонеальных клеток с активностью трансаминаз АЛТ и АСТ может объясняться поддержанием оптимальных для дыхательного метаболизма ПК концентраций кетокислот, в частности – пирувата и α-кетоглутарата.
Заключение
Pseudomonas aeruginosa способен стимулировать ответ перитонеальных клеток не только за счет своего эндотоксина – ЛПС, но также выделяемых из клеток бактерии трансаминаз АЛТ и АСТ. В действии АЛТ и АСТ на дыхание перитонеальных клеток проявляется стимулирующее влияние непосредственно на метаболический статус через концентрацию субстратов цикла Кребса – пирувата и α-кетоглутарата.
Библиографическая ссылка
Тарасенко Т.Н., Габалов К.П., Рюмина М.В., Староверов С.А., Волков А.А. ВЛИЯНИЕ ТРАНСАМИНАЗ, ВЫДЕЛЯЕМЫХ PSEUDOMONAS AERUGINOSA, НА ОКИСЛИТЕЛЬНЫЙ МЕТАБОЛИЗМ ПЕРИТОНЕАЛЬНЫХ КЛЕТОК МОРСКОЙ СВИНКИ И МЫШИ IN VITRO // Международный журнал прикладных и фундаментальных исследований. 2016. № 8-5. С. 760-763;URL: https://applied-research.ru/en/article/view?id=10164 (дата обращения: 19.05.2026).

