Scientific journal
International Journal of Applied and fundamental research
ISSN 1996-3955
ИФ РИНЦ = 0,556
POSSIBILITY OF COMPLEX CORRECTION OF OBESITY IN MEN WITH HYPOTESTOSTERONEMIA
Согласно данным Всемирной организации здравоохранения, в современном мире избыточную массу тела имеют около 1,7 млрд человек, по оценкам ряда экспертов, к 2025 г. число лиц, страдающих избыточной массой тела, увеличится примерно в 2 раза. В настоящее время эксперты говорят об эпидемии ожирения во всем мире [3]. По данным ряда авторов, 30 % трудоспособного населения России имеют избыточную массу тела и 25 % – ожирение. Распространенность ожирения среди женщин составляет 30–40 %, мужчин – 10–20 %. Существует мнение, что распространенность ожирения среди мужчин гораздо выше, что связано с низкой обращаемостью [2; 3].
Абдоминальное ожирение, характерное для мужчин, сопровождается не только высоким риском развития сопутствующих заболеваний, но и нарушением метаболизма половых гормонов, влияющим на половую функцию [3; 8; 9]. Абдоминальное ожирение может приводить к гипогонадизму, с другой стороны гипогонадизм играет роль в развитии и прогрессировании ожирения и метаболическом синдроме [4]. Именно в жировой ткани при участии фермента ароматазы, изоформы цитохрома Р-450, происходит конверсия андрогенов в эстрогены. С увеличением массы жировой ткани концентрация эстрогенов увеличивается. Кроме того, при ожирении уменьшается продукция в печени глобулина, связывающего половые стероиды, что обусловливает повышение уровня активных свободных фракций эстрогенов [5; 6; 7]. Однако до сих пор актуален вопрос – первично или вторично нарушение секреции тестостерона при ожирении. Одни авторы относят гормональные нарушения к вторичным, доказывая, что при коррекции массы тела происходит нормализация уровня тестостерона. В других исследованиях показано, что при экзогенном введении тестостерона у мужчин снижается количество висцерального жира, уменьшается инсулинорезистентность, снижается диастолическое артериальное давление, улучшается липидный профиль [1; 3; 10].
Наряду с препаратами тестостерона и гонадотропинов потенциальными кандидатами на роль средств для устранения гипогонадизма и дефицита тестостерона являются антиэстрогены. Таким образом, актуален поиск механизмов коррекции гормональных нарушений у мужчин с ожирением и цель работы – оценка клинической эффективности комплексной коррекции ожирения и нарушения метаболизма половых гормонов у мужчин.
Материалы и методы исследования
Критерии включения: мужчины в возрасте от 25 и до 75 лет; наличие ожирения III степени; отсутствие гормональной замещающей терапии.
Все пациенты разделены на 2 группы по 20 человек: основная группа (ОГ) – больные со сниженным содержанием тестостерона и контрольная (КГ) – больные с нормальным уровнем тестостерона. Средний возраст мужчин в ОГ составил 47,8 ± 2,54 лет, кг – 53,7 ± 3,1 лет.
Все больные получали традиционный курс лечения, включавший стандартную лекарственную терапию и лечебную физкультуру. Все пациенты в течение 14 дней получали гипонатриевую антиатерогенную диету с энергетической ценностью 2200 ккал в сутки, содержавшую 98 г белка, 72 г жира и 306 г углеводов. Диета характеризовалась уменьшенным количеством рафинированных углеводов, холестеринсодержащих продуктов и экстрактивных веществ. После выписки из стационара больным выдавались на руки рекомендации по соблюдению диеты идентичного химического состава и калорийности. Пациенты ОГ на фоне диетотерапии дополнительно в течение всего периода исследования получали антиэстрогенный препарат (АэП) в суточной дозе 100 мг. Продолжительность наблюдения составила 5 недель. Комплексное обследование пациентов включало измерение в динамике антропометрических показателей (массы тела, окружности талии и бедер), жировой массы тела и определение общего и свободного тестостерона плазмы крови.
Результаты исследований обработаны с помощью пакета программ «STATISTICA 11.0». Сравнение количественных показателей проводили при помощи рангового U-образного критерия Манна-Уитни. При анализе повторных измерений применяли критерий Вилкоксона. Статистически значимыми считались различия при ρ < 0,05.
Результаты исследования и их обсуждение
Динамика массы тела больных
Результаты измерения массы тела больных в обеих группах представлены в табл. 1.
Таблица 1
Динамика массы тела у больных на фоне диетотерапии и приема АэП
|
Основная группа |
Контрольная группа |
||
|
Медиана значений [25 %;75 % перцентили] |
Медиана значений [25 %;75 % перцентили] |
||
|
Масса тела |
Исходно |
159,7 [142,0; 179,0] |
133,7 [124,6; 157,7] |
|
2 недели |
152,8* [133,2; 167,3] р = 0,00004 |
128,5* [119,3; 149,7] р = 0,0007 |
|
|
5 недель |
151,7* [129,3; 165,8] р = 0,00009 |
131,9* [116,2; 145,5] р = 0,0006 |
|
Примечание. *различия достоверны по сравнению с исходным значением.
Как видно из табл. 1, у больных ОГ редукция массы тела была выше по сравнению с больными кг. При этом показатели в ОГ достоверно отличались от исходных значений через 2 и 5 недель, а также между собой. К окончанию 2-й недели лечения редукция массы тела составила 6,9 кг, что на 4,3 % (р < 0,0001) ниже исходных значений, к 5-й неделе – 8,0 кг, что составило 5,0 % (р < 0,0001). Динамика массы тела в кг была менее убедительна: в первые 2 недели лечения редукция массы тела была сопоставима с больными ОГ и составила в среднем 5,2 кг (3,9 %, р = 0,0007); на втором этапе исследования масса тела начала возрастать и к 5-й неделе практически вернулась к исходным показателям. В итоге, масса тела больных за весь период наблюдения уменьшилась лишь на 1,8 кг (1,3 %), при этом различия между начальной и конечной точкой были достоверны р = 0,0006.
Таким образом, анализ массы тела больных в динамике показал, что добавление к диетотерапии АэП приводит к выраженной ее редукции в течение всего периода наблюдения, в то время как в кг выявляется обратная тенденция.
Исследование жировой массы как показателя состава тела у больных на фоне диетотерапии и приема АэП
Результаты исследования жировой массы у больных методом биоимпедансометрии представлены в табл. 2.
Таблица 2
Динамика изменения жировой массы тела у больных
|
Основная группа |
Контрольная группа |
||
|
Медиана значений [25 %;75 % перцентили] |
Медиана значений [25 %;75 % перцентили] |
||
|
Жировая масса |
Исходно |
79,4 [60,45; 90,1] |
58,9 [56,1; 77,7] |
|
2 недели |
74,4 [55,0; 86,1]* |
58,7 [53,3; 73,1] |
|
|
5 недель |
73,1 [51,8; 82,0]* |
56,4 [50,9; 68,5] * |
|
Примечание. *различия достоверны по критерию Wilcoxon при р < 0,05 по сравнению с исходным значением.
Пациенты ОГ исходно имели большие значения по жировой массе по сравнению с больными кг, при этом соотношения основных показателей (жировая и тощая масса, общая жидкость) в обеих группах были сопоставимы.
Динамика жировой массы тела у больных
Как следует из табл. 2, больные ОГ характеризовались существенной редукцией жировой массы по сравнению с пациентами кг: жировая масса к окончанию стационарного этапа лечения снизилась в ОГ на 5,0 кг (6,3 %, р < 0,05), в то время как в кг этот показатель статистически не отличался от исходного значения. В последующие 3 недели амбулаторной терапии интенсивность редукции жировой массы в ОГ составила еще 1,3 кг и в итоге за весь период лечения больные ОГ потеряли 6,3 кг или 7,9 % (р < 0,05). Амбулаторный этап лечения больных кг привел к снижению жировой массы на 2,3 кг, при этом общая потеря жировой массы за весь период лечения составила в среднем 2,5 кг или 4,2 % (р < 0,05). Анализируя редукцию жировой массы тела, очевидно, что добавление АэП к диетотерапии приводит к значимому «ускорению» потери жира больными. Через 5 недель терапии различия составили 3,7 % и были статистически достоверны при уровне значимости р = 0,044.
Таким образом, можно предполагать повышение интенсивности метаболизации жиров у больных ОГ на фоне приема АэП. Применение АэП на фоне диетотерапии, по сравнению с пациентами, получающими только диетотерапию, приводит к достоверно более быстрой и выраженной редукции жировой массы тела.
Исследование уровня тестостерона на фоне диетотерапии и приема АэП
Одним из критериев отбора больных в ОГ было наличие гипотестостеронемии, в связи с этим ОГ и кг исходно отличались по уровню общего и свободного тестостерона (см. табл. 3).
Таблица 3
Содержание общего и свободного тестостерона в плазме крови больных на фоне диетотерапии и приема АэП
|
Основная группа |
Контрольная группа |
||
|
М ± SD |
М ± SD |
||
|
Общий тестостерон |
Исходно |
8,9 ± 2,8 |
19,4 ± 14,6 |
|
5 недель |
21,3 ± 8,7* (р = 0,000004) |
13,5 ± 6,9 (р = 0,11) |
|
|
Свободный тестостерон |
Исходно |
4,9 ± 2,4 |
8,6 ± 3,2 |
|
5 недель |
15,7 ± 8,1* (р = 0,000011) |
7,7 ± 3,8 (р = 0,45) |
|
Примечание. *различия достоверны при р < 0,0001 по сравнению с исходным значением в той же группе.
На фоне диетотерапии наблюдается отчетливая тенденция к снижению общего и свободного тестостерона в кг. В ОГ выявлено высоко достоверное, более чем двукратное, повышение уровня общего тестостерона (см. рисунок, а) и более чем трехкратное повышение свободного тестостерона (см. рисунок, б). Для анализа выраженности изменений сравнивались относительные величины – отклонение значений общего и свободного тестостерона от исходного значения в %.
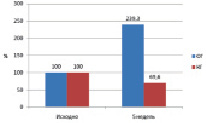
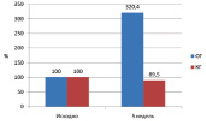
a б
Динамика содержания общего тестостерона (а) и свободного тестостерона (б) у больных на фоне диетотерапии и приема АэП
Выводы
1. Выявлено, что прием антиэстрогенного препарата в течение 5 недель на фоне диетотерапии приводит к достоверному преимуществу в редукции общей массы тела у больных с ожирением III степени.
2. Установлено, что прием антиэстрогенного препарата приводит к достоверно быстрой и выраженной редукции жировой массы тела у больных с ожирением III степени.
3. Доказано, что на фоне диетотерапии и приема антиэстрогенного препарата происходит достоверное увеличение уровня общего тестостерона и свободного тестостерона, при этом, пациенты, не принимающие препарат, характеризуются тенденцией к снижению данных биомаркеров на фоне диетотерапии.
Представленные данным свидетельствуют о безусловной целесообразности продолжения исследований влияния антиэстрогенного препарата на показатели композиционного состава тела и метаболического статуса больных с ожирением.
Библиографическая ссылка
Феофанова Т.Б., Богданов А.Р., Залетова Т.С. ВОЗМОЖНОСТИ КОМПЛЕКСНОЙ КОРРЕКЦИИ ОЖИРЕНИЯ У МУЖЧИН С ГИПОТЕСТОСТЕРОНЕМИЕЙ // Международный журнал прикладных и фундаментальных исследований. 2016. № 9-1. С. 97-100;URL: https://applied-research.ru/en/article/view?id=10198 (дата обращения: 14.05.2026).

