Scientific journal
International Journal of Applied and fundamental research
ISSN 1996-3955
ИФ РИНЦ = 0,556
THE ACTUAL QUESCHENS OF ANTHRACENCONTAINING PLANT MEDICINAL DRUGS, INCLUDING IN THE STATE PHARMACOPOEIA OF RUSSIAN FEDERATION
В медицинской практике широко применяются лекарственные препараты на основе лекарственного растительного сырья (ЛРС), содержащего антраценпроизводные [4, 5], а именно: листья и плоды кассии остролистной (Сassia acutifolia Del.), или сенны александрийской (Senna alexandrina Mill.), листья и плоды кассии узколистной (Cassia angustifolia Vahl.), трава зверобоя продырявленного (Hypericum perforatum L.) и трава зверобоя пятнистого (Hypericum maculatum Grantz.).
Одной из актуальных проблем в фармации является совершенствование методов анализа ЛРС и фитопрепаратов, причем одной из противоречивых проблем с точки зрения фармакопейного анализа является стандартизация ЛРС, содержащего антраценпроизводные. Внедрение методов тонкослойной хроматографии (ТСХ) и высокоэффективной жидкостной хроматографии (ВЭЖХ) открыло новые возможности для целей стандартизации ЛРС и фитопрепаратов, что нашло отражение в вышедшей в свет Государственной фармакопее Российской Федерации XIII издания [2]. в Государственную фармакопею Российской Федерации XIII издания включены виды сырья вышеперечисленных лекарственных растений: ФС.2.5.0038.15 «Сенны листья», ФС 2.5.0021.15 «Крушины ломкой кора», ФС 2.5.0014.15 «Жостера слабительного плоды», 2.5.0052.15 «Щавеля конского корни» и 2.5.0015.15 «Зверобоя трава», однако по-прежнему актуальной остается проблема совершенствования методов стандартизация ЛРС и фитопрепаратов,
Цель настоящих исследований – научное обоснование методологических подходов к стандартизации лекарственного растительного сырья, содержащих антраценпроизводные.
Материалы и методы исследования
В качестве объектов исследования служили кора крушины ломкой (Frangula alnus Mill.), плоды жостера слабительного (Rhamnus cathartica L.), корни щавеля конского (Rumex confertus Willd.), листья сенны александрийской (Cassia acutifolia Del.), трава зверобоя продырявленного (Hypericum perforatum L.) и трава зверобоя пятнистого (Hypericum maculatum Grantz.), а также антраценпроизводные и флавоноиды, выделенные из вышеперечисленного ЛРС. Выделение индивидуальных веществ из ЛРС осуществляли с использованием колоночной хроматографии. Контроль за разделением веществ осуществляли с помощью ТСХ-анализа на пластинках «Сорбфил ПТСХ-АФ-А-УФ». Cпектры ЯМР 1Н и ЯМР 13С получали на приборе «Bruker AM 300», масс-спектры снимали на масс-спектрометре «Kratos MS-30», регистрацию УФ-спектров проводили с помощью спектрофотометра «Specord 40» (Analytik Jena).
Результаты исследования и их обсуждение
В результате исследования компонентного состава коры крушины ломкой, плодов жостера слабительного, корней щавеля конского, листьев сенны александрийской, травы зверобоя продырявленного и травы зверобоя пятнистого выделены в индивидуальном виде доминирующие вещества, представленные антраценпроизводными (1–8) (рис. 1) и флавоноидами (9–14) (рис. 2).
В ходе научного обоснования подходов к стандартизации ЛРС, содержащего антраценпроизводные, нами принималось во внимание то обстоятельство, что наряду с антраценпроизводными в сырье содержатся и другие БАС, частности, флавоноиды и дубильные вещества [3], которые представляют интерес с точки зрения диагностики. Так, в листьях сенны александрийской и сенны узколистной флавоноид кемпферол-3–O-гентиобиозид (13) является доминирующим фенольным компонентом и во многом определяет УФ-спектр водно-спиртовых извлечений сырья данных растений. в плодах жостера слабительного доминирующим фенольным компонентом является 3–О-рутинозид рамнетина (14) (флавоноид). в корнях щавеля конского второй группой БАС являются дубильные вещества. Трава зверобоя продырявленного и трава зверобоя пятнистого с точки зрения химической классификации относятся к флавоноидам, однако очень важным является учет наличия в сырье данных растений антраценпроизводных, которые обусловливают антидепрессантное действие лекарственных препаратов на основе травы зверобоя и рассматриваются за рубежом как их критерии качества.
Следовательно, успешное решение проблемы стандартизации возможно лишь на основе учета совокупной значимости содержащихся в сырье различных групп БАС.
Качество сырья «Зверобоя трава» регламентирует ГФ РФ XIII издания (ФС.2.5.0015.15). Раздел «Подлинность» наряду с внешними и микроскопическими признаками включает определение основных групп биологически активных веществ с использованием ТСХ и стандартного образца рутина (10), являющегося 3–О-рутинозидом кверцетина (11). на наш взгляд, в данном методе целесообразно было бы использование ГСО гиперозида (9) – второго по значимости (после рутина) флавоноида для зверобоя продырявленного и доминирующего флавоноида в траве зверобоя пятнистого. Кроме того, использование второго стандарта в методиках – довольно часто применяемый методический подход, который соответствует современным тенденциям фармацевтического анализа.
Количественное определение суммы флавоноидов осуществляют методом дифференциальной спектрофотометрии при аналитической длине волны 415 нм с использованием ГСО рутина. на наш взгляд, было бы целесообразным определение в траве зверобоя не только суммы флавоноидов, но и суммы антраценпроизводных, принимая во внимание то обстоятельство, что данная группа веществ, во-первых, отвечает за антидепрессантный эффект, а, во-вторых, тот факт, что в Европейской фармакопее стандартизация данного сырья осуществляется по содержанию антраценпроизводных (в пересчете на гиперицин). Сравнительное исследование химического состава сырья фармакопейных видов зверобоя показало (метод ВЭЖХ), что в траве зверобоя продырявленного среди флавоноидов преобладает рутин [5], тогда как в траве зверобоя пятнистого доминирует гиперозид (9). Кроме того, в последнем виде не обнаружен 3,811–бисапигенин (12), содержащийся в траве зверобоя продырявленного и обладающий, по нашим данным, антидепрессантной активностью. Результаты данных исследований свидетельствуют о целесообразности стандартизации сырья и препаратов зверобоя не только по содержанию флавоноидов, но и антраценпроизводных.
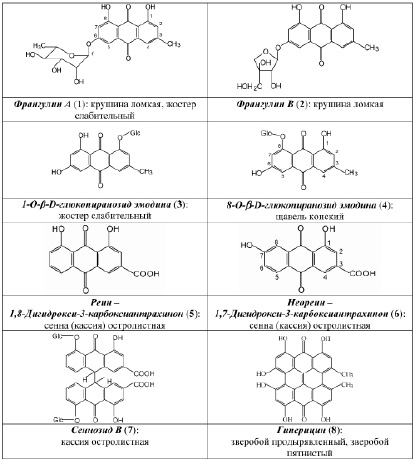
Рис. 1. Антраценпроизводные фармакопейных растений
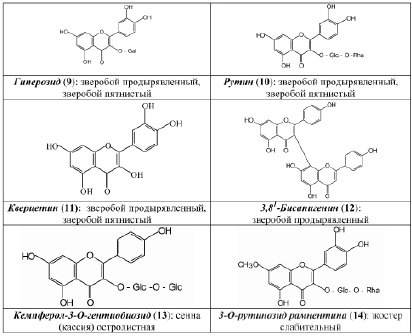
Рис. 2. Флавоноиды антраценсодержащих фармакопейных растений
Одной из нерешенных проблем с точки зрения фармакопейного анализа является стандартизация сырья видов кассии, или сенны. Целесообразность внедрения новых современных методов анализа связана с тем, что в существующих подходах к анализу не в полной мере используется все разнообразие химического состава сырья кассии [1, 2, 6–8]. на наш взгляд, актуальным является учет значимости флавоноидов, в частности, кемпферол-3–О-гентиобиозида (13), как по содержанию, так и по возможному вкладу в фармакологическое действие препаратов на основе кассии.
С использованием ТСХ обнаружено, что именно кемпферол-3–О-гентиобиозид является доминирующим компонентом листьев сенны. на наш взгляд, обнаружение методом ТСХ данного соединения, диагностически значимого для листьев сенны, является перспективным подходом в плане идентификации сырья данного растения. Это тем более важно, что в силу невысокого содержания сеннозида а и в в листьях кассии [6, 8] определение данных антрагликозидов методом ТСХ весьма проблематично. по нашим данным, доминирующим соединением листьев кассии является близкий к реину (5) по хроматографической подвижности и физико-химическим характеристикам 1,7–дигидрокси-3–карбоксиантрахинон (6), являющийся новым природным соединением.
Кроме того, методика количественного определения суммы антраценпроизводных, включенная в ФС.2.5.0038.15 «Сенны листья», на наш взгляд, имеет ряд недостатков: является многостадийной и небезопасной, включающей такие стадии, как кислотный гидролиз, многократную экстракцию сырья, обработку диэтиловым эфиром – легкокипящим огнеопасным растворителем. Методики количественного определения антраценпроизводных, включенные в зарубежные фармакопеи, с точки зрения пробоподготовки сопоставимы с ГФ СССР XI издания [1] и ГФ РФ XIII издания (ФС.2.5.0038.15 «Сенны листья») и отличаются только значением используемой аналитической длиной волны (515 нм вместо 523 нм), а также подходом [7], предусматривающим расчет содержания на сеннозид в (7).
В соответствии с Европейской фармакопеей для расчета содержания суммы антраценпроизводных целесообразно использовать теоретическое значение удельного показателя поглощения (240) стандартного образца сеннозида в [7]. Видимо, поэтому наблюдается расхождения в регламентируемых числовых показателях: содержание сырье суммы агликонов антраценового ряда в пересчете на хризофановую кислоту не менее 1,35 % и содержание суммы антрагликозидов не менее 2,5 % в пересчете на сеннозид B [7].
Аналогичные проблемы нами решены и при разработке методик качественного и количественного анализа плодов жостера слабительного, коры крушины ломкой и корней щавеля конского [4], в случае которых обосновано использование стандартных образцов франгулина а (1) и 8–О-b-D-глюкопиранозида эмодина (4). Так, в случае коры крушины ломкой ГФ РФ XIII издания раздел «Подлинность» включает определение основных групп биологически активных веществ с использованием ТСХ и стандартного образца барбалоина. Методический подход, предусматривающий определение подлинности по отсутствию барбалоина, который в отличие от франгулина а (1) и франшулина в (2) не содержится в коре крушины, представляется ошибочным решением. Что касается раздела «Количественное определение», то представляется нелогичным включение в ГФ РФ XIII издания (двух методик – из ГФ СССР XI издания (в пересчете на истизин) и Европейской фармакопеи (в пересчете на глюкофрангулин А). Видимо, поэтому числовой показатель «сумма антрагликозидов» в отечественной и европейской фармакопеях отличаются значительно – 4,5 % и 7 % соответственно. Нами на примере данного сырья показано, что определение содержания антраценпроизводных целесообразно определять без сочетания таких стадий или процессов, как кислотный гидролиз (ледяная уксусная кислота) и экстракция (диэтиловый эфир). при этом определение содержания суммы антраценпроизводных осуществляется методом спектрофотометрии при длине волны 524 нм в пересчете на франгулин А, являющийся доминирующим антрагликозидом коры крушины.
Выводы
Таким образом, результаты проведенных исследований позволили научно обосновать новые подходы к стандартизации фармакопейных видов ЛРС, содержащих антраценпроизводные. Доказано, что в сырье растений (виды зверобоя, виды кассии, жостер слабительный), содержащих одновременно антраценпроизводные и флавоноиды, стандартизацию целесообразно осуществлять с учетом обеих групп действующих веществ.
Библиографическая ссылка
Правдивцева О.Е., Куркин В.А., Авдеева Е.В., Куркина А.В., Шмыгарева А.А., Агапов А.И., Кулагин О.Л. АКТУАЛЬНЫЕ ВОПРОСЫ СТАНДАРТИЗАЦИИ АНТРАЦЕНСОДЕРЖАЩИХ ВИДОВ ЛЕКАРСТВЕННОГО РАСТИТЕЛЬНОГО СЫРЬЯ, ВКЛЮЧЕННЫХ В ГОСУДАРСТВЕННУЮ ФАРМАКОПЕЮ РОССИЙСКОЙ ФЕДЕРАЦИИ // Международный журнал прикладных и фундаментальных исследований. 2016. № 12-2. С. 272-276;URL: https://applied-research.ru/en/article/view?id=10822 (дата обращения: 16.05.2026).

