Не смотря на огромны научный вклад и внушительный практический опыт, проблема распространенного гнойного перитонита (РГП) не теряет своей актуальности. По данным различных авторов, летальность при этом грозном осложнении воспалительных заболеваний органов брюшной полости сохраняется на уровне 20-30%, достигая наиболее высоких цифр при развитии полиорганной недостаточности (ПОН), абдоминального сепсиса (АС) и септического шока (СШ) [1, 2, 3, 4, 5].
По данным Красноярского краевого гнойно-септического центра (ККГСЦ), от острых хирургических заболеваний в 2015 году погибло 350 человек, из них 18 пациентов от кровотечений, 105 пациентов от острого панкреатита, большая часть - 227 пациентов - от перитонита и абдоминального сепсиса. Исходя из выше изложенного очевидно, что проблема лечения распространенного гнойного перитонита остаётся злободневной на сегодняшний момент, представляя собой непростую задачу, требующую комплексного подхода к лечению на всех этапах ведения пациента, а так же усовершенствования имеющихся хирургических методик.
Пациенты с распространенным гнойным перитонитом, как правило, нуждаются в проведении нескольких санирующих операций на брюшной полости, направленных на устранение источника перитонита. На сегодняшнем этапе развития абдоминальной хирургии для лечения РГП принят метод программированных релапаротомий, позволяющий осуществлять контроль за источником внутрибрюшной инфекции. Однако, стоит отметить, что дополнительное оперативное вмешательство и санация брюшной полости у таких пациентов приводит к усилению системного воспалительного ответа, который вносит большой вклад в развитие и прогрессированию ПОН. Учитывая этот факт, следует стремиться к снижению количества необходимых санирующих операций путём усовершенствования методики лапаростомии.
Немаловажное значение в комплексе лечебных мероприятий при распространённых формах перитонита отводится ведению периоперационного периода: ранней и адекватной антибактериальной терапии (АБТ), коррекции эндотоксикоза, базисной и адьювантной терапии, иммунокоррекции. [5, 6, 7].
Адекватная санация брюшной полости и полнота проводимой интенсивной терапии не является единственными этапами на пути к успешному исходу лечения РГП. Немаловажную роль в течении РГП, развитии осложнений и исходе заболевания играют изменения иммунной системы пациента. Тяжёлая дисфункция иммунной системы во многом обеспечивает возникновение ПОН с последующим прогрессированием и, как правило, неблагоприятным исходом заболевания [7, 8, 9, 10]. Оценка иммунного статуса пациента позволяет дать прогноз течения заболевания и правильно выбрать хирургическую тактику и объём интенсивной терапии у больных с РГП [7, 10].
Цель исследования
Анализ особенностей течения и исхода РГП в зависимости от способа оперативного лечения: использование традиционной лапаростомы (ТЛ) и вакуум-ассистированной лапаростомы (ВАК). Оценка состояния иммунной системы пациентов в зависимости от характера течения и исхода заболевания с выявлением характерных особенностей реагирования иммунной системы пациентов с РГП.
Материалы и методы исследования
В исследование вошли 56 пациентов с диагнозом РГП, средний возраст которых составил 47,5± 7,8 лет. В первую группу вошли 30 пациентов, которым применялась лапаростома по традиционной методике. Вторую группу составили 26 пациентов, которым применялась ВАЛ при помощи аппарата VivanoTec® S 042 NPWT фирмы Hartmann в режиме постоянного вакуумирования 145 мм рт.ст. При поступлении, всем пациентам проводилась оценка тяжести состояния и степени полиорганной недостаточности при помощи интегральных шкал SAPS и SOFA соответственно, состояние брюшной полости оценивалось при помощи Мангеймского индекса перитонита (МИП) и индекса брюшной полости (ИБП).
Для оценки иммунного статуса, проводился забор крови для исследования хемилюминесцентной активности нейтрофильных гранулоцитов. Нейтрофильные гранулоциты выделяли из цельной гепаринизированной крови центрифугированием в двойном градиенте плотности фиколлурографина: ρ = 1,077 г/см3 – для отделения лимфоцитов, ρ = 1,119 г/см3 – для выделения нейтрофилов. Оценку спонтанной и зимозан-индуцированной хемилюминесценции осуществляли в течение 90 мин на 36-канальном хемилюминесцентном анализаторе CL3606 (СКТБ «Наука», Красноярск).
Статистический анализ осуществляли при помощи пакета прикладных программ Statistica 8.0 (StatSoft Inc., 2007).
Достоверность различий между показателями независимых выборок оценивали по непараметрическому критерию Манна– Уитни, достоверность различий в динамике лечения определяли по критерию Вилкоксона.
Результаты исследования и их обсуждения
Для оценки эффективности лечения проводился сравнительный анализ количества необходимых санаций в зависимости от варианта хирургического лечения РГП, динамика изменения ИБП после проведения санирующих операций, а так же динамическая оценка степени тяжести и развития полиорганной недостаточности при помощи интегральных шкал SAPS и SOFA.
При поступлении у всех исследуемых пациентов были признаки SIRS. В группе пациентов с применением ТЛ сепсис диагностирован у 14 пациентов (46,7%), тяжелый сепсис у 10 пациентов (33,3%), в состоянии септического шока прибывали 6 пациентов (20%). В группе с применением ВАК сепсис наблюдался у 6 пациентов (23%), тяжелый сепсис у 12 пациентов (46,2), в состоянии септического шока находилось 8 пациентов (30,8%).
Величина МИП у всех пациентов обеих групп превышала 25 баллов.
При сравнительной оценке показателя среднего количества санирующих операций на одного пациента, отмечено существенное уменьшение количества необходимых санаций при применении ВАК в группах с тяжелым и крайне тяжелым течением перитонита.
При оценке динамики изменения ИБП после первой санирующей операции также отмечается более значительное снижение ИБП при применении ВАК в обеих группах (рис.2).
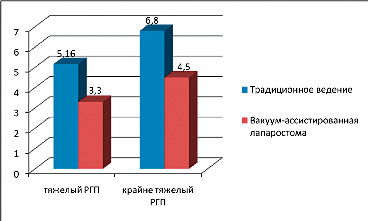
Рис. 1. Среднее количество санаций на одного больного.
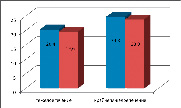
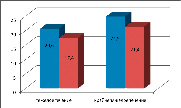
Традиционная лапаростома Вакуум-ассистированная лапаростома
Рис.2. Динамика ИБП после первой санирующей операции
В группе с применением ВАК отмечалась стойкая тенденция к улучшению состояния пациента и купированию SIRS, закрытие брюшной полости при тяжелом течении происходило на 3 санацию, при крайне тяжелом на 4 санацию, тогда как при традиционном ведении отмечалось ухудшение показателей состояния пациента с прогрессисрованием SIRS после 3 и четвёртой санации в группах с тяжелым и крайне тяжелым течением соответственно (рис. 3, 4).
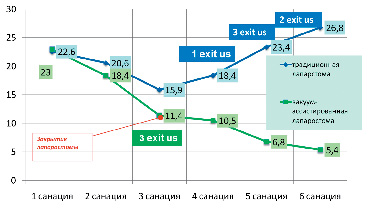
Рис. 3. Динамическая оценка тяжести состояния в группе пациентов с тяжелым перитонитом (SAPS )
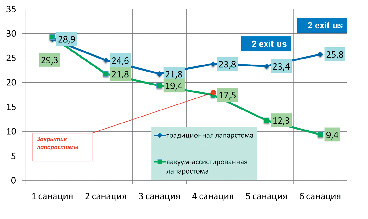
Рис. 4. Динамическая оценка тяжести состояния в группе пациентов с крайне-тяжелым перитонитом (SAPS )
Применение ВАК позволило значительно снизить летальность во всех группах. Так, в группе со средней тяжестью течения перитонита, летальность при применении ВАК составила 0%, что на 10% меньше, в сравнении с ТЛ. В группе с тяжелым течением, летальность с применением ВАК снизилась на 8,5%. Показатели летальности при применении ВАК при крайне тяжелом течении снизились на 5,2 % (рис.5).
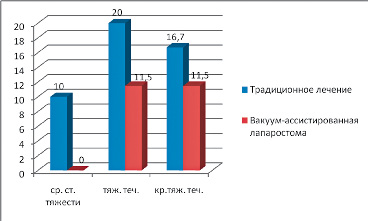
Рис. 5. Показатели летальности
При оценке иммунного статуса пациентов с РГП отмечалось, что у больных с благоприятным исходом, а так же средней тяжестью количество Т-хелперов и регуляторных Т-лимфоцитов в периферической крови в начале лечения было значительно повышено после чего постепенно снижалось, что указывает на массовый выход нового клона клеток и их активную миграцию, необходимую для реализации иммунного ответа, а так же об активной миграции Т-лимфоцитов говорит повышение количества клеток несущих на своей поверхности CD62l.
В группе с благоприятным исходом, а так же средней степенью тяжести отмечалось постепенное снижение количества В-лимфоцитов в русле крови, что может указывать на реализацию поздних этапов В-клеточного иммунного ответа, связанного с миграцией клеток и активной продукцией иммуноглобулинов, а так же на это указывает снижение процента В-лимфоцитов несущих CD23.
Таким образом, увеличение количества наивных В2-лимфоцитов, на фоне нормальных показателей Т-хелперов и регуляторных Т-лимфоцитов, а так же явно низкий пул активированных клеток, могут выступать в роли маркера применимого для прогнозирования неблагоприятного исхода распространенного гнойного перитонита (рис 6).
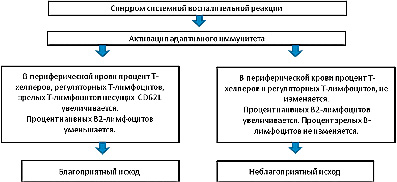
Рис. 6. Схема прогнозирования исхода РГП на основе фенотипического состава Т- и В-лимфоцитов периферической крови.
Выводы
Применение вакуум-ассистированной лапаростомы позволяет в более короткие сроки улучшить интраабдоминальную ситуацию, сокращая количество необходимых санирующих операций и увеличивая срок между санирующими операциями. Более быстрое купирование воспалительных явлений брюшины и сокращение количества санирующих операций, по-видимому, способствуют уменьшению количества системных и местных осложнений и улучшению результатов лечения больных с тяжелым абдоминальным сепсисом, что позволяет рассматривать предложенную методику лечения как перспективную и рекомендовать её к более широкому применению.
Иммунный статус пациента играет немаловажную роль в исходе перитонита. Основываясь на данных иммуннограммы пациента, возможно с высокой долей вероятности предположить исход заболевания, а так же выбрать верную тактику ведения пациента с РГП индивидуально, что поможет снизить показатели летальности и улучшить результаты лечения пациентов с РГП

