Scientific journal
International Journal of Applied and fundamental research
ISSN 1996-3955
ИФ РИНЦ = 0,556
FACTOR ANALYSIS OF THE PROCESS OF ELECTRODEPOSITION OF METAL CATIONS FROM AQUEOUS SOLUTIONS
В работе процесс электроосаждения катионов металлов рассматривался на модельных растворах с различным содержанием ионов Mn2+ .
В зависимости от типа электрода, материала и условий работы электролизера при электролизе марганецсодержащих растворов на аноде могут выделяться [1–6]:
– молекулярный кислород – в результате разложения гидроксид-ионов и молекул воды:
4ОН- – 4e → 2H2O + О2↑
4 H2O – 4e → 4H+ + О2↑
– молекулярный хлор – при разряде хлорид-ионов, который затем в слабокислой и нейтральной среде гидролизуется, образуя хлорид-ионы и кислородсодержащие соединения хлора – «активный хлор»:
2Cl- – 2e → Cl2↑
Cl2 + H2O → H+ + Cl- + HClO
На катоде в основном происходит образованию молекулярного водорода и гидроксид-ионов в результате разряжения молекул воды и восстановления катионов водорода:
2H2O + 2e → H2↑+ 2OH-
2H+ + 2e → H2↑
В слабокислой, кислой, нейтральной и слабощелочной среде (рН ≤ 10) ионы Mn2+ окисляются до соединений Mn3+ , Mn4+ [2, 10–12]. В общем случае процесс окисления ионов Mn2+ электролизными растворами «активного хлора» до соединений Mn3+ , Mn4+ протекает по схеме [8]:
Mn2+ + СlО- + 6ОН- → Сl- +2МnО(ОН)2↓ + Н2О
Mn2+ + НСlО + Н2О → Сl- +МnО(ОН)↓ + 2Н+
Согласно представленным уравнениям реакций, эффективность процесса окислительного осаждения Mn (II) из растворов напрямую зависит от окислительной активности образующихся в процессе электролиза кислородных соединений хлора.
При электрохимической обработке марганецсодержащих растворов, после образования нерастворимых соединений Mn3+ , Mn4+ , будет протекать процесс его коагуляции.
Известно, что электролизная обработка растворов способствует интенсификации процесса коагуляции: при наложении электрического поля на систему ускоряется процесс формирования и осаждения коагулированной взвеси. В процессе электрообработки системы происходит значительное увеличение удельного содержания твердого вещества в единице объемы раствора. Во всех опытах с электрическим полем происходит более быстрое осветление воды, образование осадка и стабилизация его уровня по сравнению с реагентной коагуляцией. При этом эффект осветления воды при электрокоагуляции увеличивался на 25–35 %. Доказано, что наибольший эффект коагуляции наблюдается при наложении электрического поля в течение всего процесса: коагулирование воды, осаждение взвеси, образования осадка и его уплотнения [7–9].
Таким образом, воздействие электрического поля на объем коагулированного раствора позволит повысить эффективность и ускорить процесс извлечения марганца (II) в виде нерастворимых соединений Mn3+ , Mn4+ .
При электрокоагуляционном извлечении металлов из вод в качестве материалов анода в основном используют либо сталь, либо алюминий.
В случае использовании стальных анодов, протекает процесс частичного растворения железа до ионов железа (II), c последующим его окислением кислород или «активным хлором» и осаждением в виде гидроокиси трехвалентного железа:
Fe0 – 2e → Fe2+
Fe2+ + О2 → Fe 3+
Fe3+ + 3ОН- → Fe(ОН)3
В случае использования алюминиевых анодов, будет протекать процесс частичного растворения алюминия до ионов Аl3+ c последующем осаждением в виде гидроокиси Аl(ОН)3:
Аl0 – 3e → Аl3+
Аl3++ 3ОН- → Аl (ОН)3.
В результате при электрохимической обработке марганецсодержащих растворов, после образования осадка в результате окисления, будет протекать процесс коагуляции, аналогичный обработке растворов соответствующими солями железа и алюминия. Однако по сравнению с реагентным коагулированием при электрохимическом растворении металлов не происходит дополнительного введения в систему хлоридов и сульфатов [8].
С целью определения оптимальных параметров работы электролизера при протекании окислительной электрокоагуляции марганца (II) из растворов в виде осадка нами были проведены исследования по изучению влияния различных факторов на эффективность протекания процесса.
Целью этих экспериментов является установление влияния исходной концентрации хлорид-ионов в исходных растворах, плотности тока на электродах и продолжительности электролиза, на эффективность протекания процесса.
В работе использовались стандартные модельные растворы хлорида натрия с исходной концентрацией: 0,01н., 0,5н. 0,1н. Согласно справочным, данным степени диссоциации хлорида натрия в растворе при указанных концентрациях равны: 0,94; 0,88; 0,85, следовательно исходная концентрации хлорид-ионов в указанных растворах буде равна: 0,549; 2,574 и 4,973 г/дм3.
Электролиз марганецсодержащих модельных растворов (СMn 2+ = 100 мг/дм3) проводили в присутствии хлорид-ионов на бездиафрагменном электролизере. Материал катода и анода сталь марки ШХ – 15 (ГОСТ 4986–90) толщиной 2 мм, соотношение площадей поверхности анодов к катодам – 1:2; расположение электродов монополярное. Соотношение катодов и анодов 1:2.
Электролиз модельных растворов проводился при плотностях тока на анодах 100, 200 и 300 А/м2 и времени обработки 30 секунд, 1 и 2 минуты.
Значения рН исходных необработанных модельных растворов колебались в пределах 3,0 – 4,5, после электрохимической обработки значения рН составляли 6,8 – 7,7.
Результаты влияние плотности тока на электродах и продолжительности электрообработки раствора на выход «активного хлора» представлены на рис. 1, 2, 3.
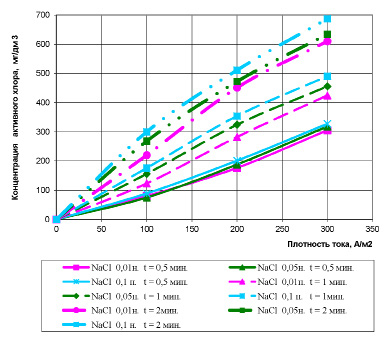
Рис. 1. Изменение концентрации «активного хлора» в растворах NaCl в зависимости от плотности тока при времени электрохимической обработке в течение 30 секунд
Графические зависимости, представленные на рис.1 показали, что образование концентрации «активного хлора» в системе необходимой для полного извлечения ионов марганца (II) (10 – 200 мг/дм3) в виде осадка наблюдается при:
– времени электролизной обработки раствора в течение 30 секунд и плотностях тока на анодах – 100, 200, 300 А/м2 (от 10 до 200 мг/дм3);
– времени электролизной обработки раствора в течение 1 минуты и плотностях тока на анодах – 100, 200 А/м2 (от 10 до 200 мг/дм3);
– времени электролизной обработки раствора в течение 2 минут и плотности тока на аноде – 100 А/м2 (от 10 до 200 мг/дм3);
После электролизной обработки модельных растворов при указанных режимах работы электролизера и удалении образовавшегося осадка путем фильтрации, остаточное содержаний ионов марганца (II) в фильтрате было меньше 0,05 мг/дм3.
С целью определения оптимального режима работы электролизера при получении необходимой концентрации «активного хлора» в системе были рассчитаны энергозатраты и выход по току «активного хлора» в исследуемых режимах. Результаты исследований представлены на рис. 2 и 3.
Полученные данные показывают, что максимальный выход по току «активного хлора» наблюдается при 30 секундной электролизной обработке раствора. В дальнейшем, при увеличении времени электролиза выход по току «активного хлора» существенно снижается. Также очевидно, что с увеличением плотности тока на электродах выход по току «активного хлора» повышается (рис. 2).
При рассмотрении зависимости между энергозатратами и максимальным выходом по току «активного хлора» при различных режимах работы электролизера, очевидно, что минимальные затраты получены при продолжительности электрообработки раствора в течение 30 секунд и плотности тока на электродах 100–300 А/м2, в зависимости от исходной концентрации ионов марганца (II) в растворе (табл. 1 и рис. 3).
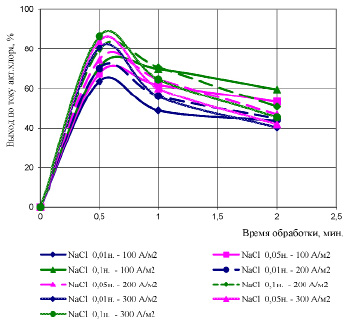
Рис. 2. Изменение ВТ ( %) «активного хлора» в растворах NaCl в зависимости от времени электрохимической обработки
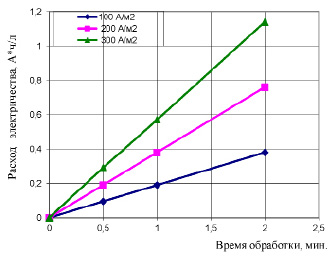
Рис. 3. Изменение расхода электричества при электролизной обработке растворов NaCl в зависимости от времени электрохимической обработки
Таблица 1
Изменение величины степени превращения хлорид-ионов в «активный хлор» при электролизной обработке растворов в течение 30 секунд и плотности тока на электродах 100 – 300 А/м2
|
Плотность тока, А/м2 |
Концентрация «активного хлора» в обработанных растворах, мг/дм3 |
С Сl- (исходная), мг/дм3 |
Степени превращения хлорид-ионов, λ, % |
||||||
|
NaCl 0,01н |
NaCl 0,05н |
NaCl 0,1н |
NaCl 0,01н |
NaCl 0,05н |
NaCl 0,1н |
NaCl 0,01н |
NaCl 0,05н |
NaCl 0,1н |
|
|
100 |
60,1 |
85,2 |
89,1 |
549,9 |
2574 |
4973 |
10,9 |
3,3 |
1,8 |
|
200 |
156,5 |
188,0 |
201,2 |
549,9 |
2574 |
4973 |
28,5 |
7,3 |
4,1 |
|
300 |
298,1 |
318,4 |
327,3 |
549,9 |
2574 |
4973 |
54,2 |
12,4 |
6,6 |
Таким образом, результаты проведенных исследований показали, что получение «активного хлора» в количестве необходимом для полного извлечения ионов марганца (II) (10 – 200 мг/дм3) из раствора в виде осадка рекомендуется проводить в течении 30 секунд при плотностях тока на анодах – 100, 200, 300 А/м2 (в зависимости от исходной концентрации марганца (II) в растворе).
Полученные результаты показали, что при равных параметрах режимах работы электролизера наибольшая степень превращения хлорид-ионов в «активный хлор» характерна для растворов с меньшей исходной концентрации хлорид-ионов т.е. для 0,01 н. раствора хлорида натрия (концентрация ионов Сl- = 549,9 мг/дм3). При увеличении концентрации хлорид-ионов в растворе данный показатель значительно снижается.
Поэтому, для определения оптимальной исходной концентрации хлорид-ионов в растворе, достаточной для получения заданной концентрации «активного хлора» в растворе необходимо учитывать соотношение двух параметров процесса: степени превращения хлорид-ионов в «активный хлор» и выхода по току «активного хлора» (табл. 2) при заданных режимах работы электролизера.
Таблица 2
Влияние продолжительности обработки раствора и плотности тока на электродах на выход «активного хлора»
|
t, мин |
Плотность тока, А/м2 |
Сила тока, А |
0,01 н раствор NaCl |
0,05 н раствор NaCl |
0,1 н раствор NaCl |
||||||
|
Напряжение, В |
ВТ, % |
Удельный расход электроэнергии, кВтч/кг |
Напряжение, В |
ВТ, % |
Удельный расход электроэнергии, кВтч/кг |
Напряжение, В |
ВТ, % |
Удельный расход электроэнергии, кВтч/кг |
|||
|
0,5 |
100 |
5,7 |
4,2 |
63,7 |
4,9 |
3,6 |
67,7 |
4,0 |
2,9 |
70,7 |
3,1 |
|
200 |
11,4 |
4,3 |
70,1 |
4,6 |
3,7 |
74,6 |
3,7 |
3,0 |
79,8 |
2,8 |
|
|
300 |
17,1 |
4,4 |
80,8 |
4,1 |
3,8 |
84,2 |
3,4 |
3,1 |
86,6 |
2,7 |
|
Представленные результаты показывают, что значительное увеличение концентрации хлорид-ионов в растворе проводит к весьма существенному снижению показателя степени превращения хлорид-ионов в «активный хлор» и не значительному при этом увеличению значений выхода по току «активного хлора». Поэтому, с целью снижения минерализации используемых растворов при получении заданного содержания «активного хлора» целесообразно рассчитывать исходную концентрацию хлорид-ионов в растворе по показателям выхода по току «активного хлора» (при заданных режимах работы электролизера). Так же не следует увеличивать исходную концентрацию хлорид-ионов в системе (свыше 550 мг/дм3), т.к. это приведет к увеличению общей минерализации используемых растворов, а так же увеличению удельного расхода NaCl на 1 кг получаемого «активного хлора».
Полученные результаты исследований позволяют утверждать, что при увеличении концентрации хлорид-ионов в растворе с 549,9 по 2574 мг/дм3 (в 5 раз) расход электроэнергии на получение 1 кг «активного хлора» в системе в среднем уменьшится на 0,9 кВтч/кг, что в пересчете на заданный интервал концентраций «активного хлора» (52,5 – 303,3 мг/дм3) является весьма незначительным. Особенно с учетом того, что затраты, связанные с вынужденным в этом случае процессом дехлорирования существенно превысят обозначенную разницу энергозатрат на получение на 1 кг «активного хлора» в растворе.
Выводы. Результаты проведенных исследований показали что:
– максимальные значения выхода по току «активного хлора» и минимальные значения энергозатраты получены при продолжительности электрообработки раствора в течение 30 секунд и плотности тока на электродах 100–300 А/м2. Поэтому получение «активного хлора» в количестве необходимом для полного извлечения ионов марганца (II) (10 – 200 мг/дм3) из раствора в виде осадка MnО2 рекомендуется проводить в течении 30 секунд при плотностях тока на электродах – 100, 200, 300 А/м2 (в зависимости от исходной концентрации марганца (II) в растворе);
– увеличение концентрации хлорид-ионов в исходном растворе при электролизной обработке проводит к весьма существенному снижению показателя степени превращения хлорид-ионов в «активный хлор» и не значительному при этом увеличению значений выхода по току «активного хлора». Поэтому, с целью снижения минерализации используемых растворов при получении заданного содержания «активного хлора» целесообразно рассчитывать исходную концентрацию хлорид-ионов в растворе по показателям выхода по току «активного хлора» (при заданных режимах работы электролизера);
– уменьшение исходной концентрации хлорид-ионов в растворе (в 5 раз) приводит к увеличению расхода электроэнергии на получение 1 кг «активного хлора» в системе в среднем на 0,9 кВтч/кг, но при этом, что введение избыточного количества хлорид-ионов в систему приведет к необходимости последующего дехлорирования стоков;
– для получения в системе концентраций «активного хлора» в интервале от 52,5 до 303,3 мг/дм3 целесообразно использовать растворы с исходным содержанием хлорид-ионов до 550 мг/дм3, при этом выход по току «активного хлора» составит от 63,7 % до 80,8 %, в зависимости от плотности тока на электродах.
Библиографическая ссылка
Муллина Э.Р. ФАКТОРНЫЙ АНАЛИЗ ПРОЦЕССА ЭЛЕКТРООСАЖДЕНИЯ КАТИОНОВ МЕТАЛЛОВ ИЗ ВОДНЫХ РАСТВОРОВ // Международный журнал прикладных и фундаментальных исследований. 2016. № 12-5. С. 864-869;URL: https://applied-research.ru/en/article/view?id=10944 (дата обращения: 03.05.2026).

