Scientific journal
International Journal of Applied and fundamental research
ISSN 1996-3955
ИФ РИНЦ = 0,556
INVESTIGATION OF SILVER-BASED DRUG ANTILEUCAEMIC ACTION ON THE MODEL OF VIRAL BOVINE LEUKEMIA
В настоящее время вопросам экологической и продовольственной безопасности уделяется большое значение, остро стоит проблема инфекционных и злокачественных заболеваний в животноводстве [4,7]. Необходимо особо отметить проблему вирусного лейкоза крупного рогатого скота [1]. Вирусный лейкоз в России является основной заразной болезнью КРС, достигая доли в 41,7 % от всех нозологий [3]. Лейкоз КРС характеризуется неопластической пролиферацией кроветворных клеток с появлением в крови малодифференцированных клеток лимфоидного или миелоидного ряда, наблюдается диффузная инфильтрация органов этими клетками и опухолевый рост. Несмотря на внедрение в практику усовершенствованных «Правил по профилактике и борьбе с лейкозом», процент инфицированности животных вирусом в разных регионах РФ достигает половины поголовья, при этом гематологические проявления лейкоза наблюдается в 10–15 % [3]. Лейкоз КРС наносит тяжелый ущерб животноводству вследствие выбраковки и утилизации больных животных, снижения продуктивности молочного стада, ограничения срока хозяйственного использования и т.п. [10, 8]. В настоящее время основным средством борьбы с лейкозом является выбраковка стада [9]. Омоложение оздоравливаемого стада за счет выведения из товарного производства полновозрастных коров и замены их нетелями, также снижает валовое производство молока. Отсутствие средств терапии и профилактики, определяют актуальность фундаментальных и прикладных исследований по данной проблеме [6]. Вместе с тем, вирусный лейкоз КРС можно рассматривать как оригинальную модель лимфопролиферативных заболеваний и разработки средств их лечения. В данной работе модель вирусного лейкоза КРС использована для оценки эффективности нового препарата «Сильверол» [5, 2]. Ранее была показана высокая антибактериальная активность данного препарата. Целью данной работы является изучение противолейкозной активности серебросодержащего препарата Сильверол в опытах in vivo на КРС с вирусным лейкозом.
Материалы и методы исследования
Препарат «Сильверол» разработан в соответствии с инновационной программой «Разработка технологии оздоровления сельскохозяйственных животных и птиц при инфекционных и опухолевых заболеваниях на основе металлопрепаратов новой генерации и доведение ее до стадии практического использования». Препарат представляет собой серебросодержащую фармацевтическую композицию на основе фармакопейных средств разрешенных к применению в Российской Федерации. Препарат использовался в виде 0,5 % и 1 % прозрачного водного раствора для инъекций (ОАО «ФИБР-Мед», ООО «Политек»). Проведение клинического тестирования препарата Сильверол разрешено Минсельхозом РФ и Россельхознадзором.
Эксперименты проведены на КРС с подтвержденным гематологическим диагнозом вирусного лейкоза (коровы черно-пестрой породы, возраст 2–6 лет, масса 450–670 кг, стандартный рацион) и РИД-положительной реакцией, разделенных в соответствии с задачами тестирования на две опытные группы (по 15–20 голов в каждой). Контролем служила группа здоровых КРС (15 голов).
Препарат вводился внутривенно в яремную вену однократно (1 группа) в дозе 1 мг/кг и трехкратно (2 группа) в дозе 1 мг/кг в виде курса с интервалом в 72 часа. Выбор экспериментальной дозы проведен с учетом данных по определению острой токсичности препарата на лабораторных животных. Характеристики острой токсичности определяли на неимбредных белых мышах при внутрибрюшинном введении 1 % водного раствора препарата. Установлены следующие токсикологические параметры стандартным методом пробит-анализа, LD50=112 мг/кг, LD16=94 мг/кг, LD84=129 мг/кг. В соответствии с этими данными, для тестирования выбрана токсикологически безопасная вышеуказанная доза в 1 мг/кг.
Испытания препарата на модели вирусного лейкоза КРС проводились при обязательном гематологическом контроле перед началом экспериментальной терапии, после завершения курса введений и, дополнительно, через 90 дней после введения. Полученные данные обрабатывались методом вариационной статистики.
Результаты исследования и их обсуждение
Однократная инъекция экспериментальной дозы препарата 1 мг/кг, приводило к снижению количества лейкоцитов (до 14,8 тыс/мкл) и абсолютного числа лимфоцитов (до 12,4 тыс/мкл). Исходные показатели лейкоцитов в среднем составляли 21,6±2,4 тыс/мкл, лимфоцитов – 18,2±1,9 тыс/мкл. Отмечена хорошая переносимость препарата и отсутствие токсических эффектов у всех подопытных животных.
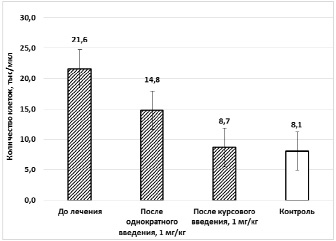
Рис. 1. Влияние внутривенных инъекций препарата «Сильверол» на общее количество лейкоцитов у животных с лейкозом
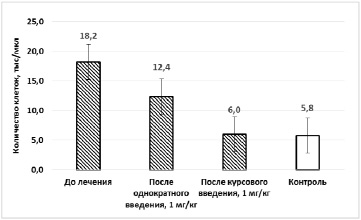
Рис. 2. Влияние внутривенных инъекций препарата «Сильверол» на абсолютное количество лимфоцитов у животных с лейкозом
Курсовое трехкратное введение препарата в дозе 1 мг/кг сопровождалась более выраженным воздействием на уровень гематологических показателей со снижением количества лейкоцитов (до 8,7±0,8 тыс/мкл), абсолютного числа лимфоцитов (до 6,0±0,7 тыс/мкл) и отсутствием незрелых лимфоидных клеток. Показатели существенно не отличались от таковых в группе контрольных животных, общее количество лейкоцитов у которых составляло 8,1±0,9 тыс/мкл, абсолютное количество лимфоцитов 5,8±0,6 тыс/мкл. Результаты эксперимента показаны на рис. 1, 2.
После применения препарата не выявлено побочного токсического эффекта на организм животных, в т.ч. воспалительных реакций, повышения температуры, снижения аппетита. Контроль динамики лейкоцитов через 3 месяца после курса введений препарата и их анализ показали сохранение их нормальных значений, подтверждая стабильную клинико-гематологическую ремиссию. Анализ полученных данных, показал наличие положительной динамики влияния препарата с нормализацией картины крови у подопытных животных.
Заключение
Эксперимент in vivo на модели вирусного лейкоза КРС показал, что изученный препарат обладает противолейкозной активностью, не оказывая при этом существенного токсического влияния на организм. Важно подчеркнуть, что работа в этом направлении представляет интерес с точки зрения, как ветеринарии, так и медицинской онкогематологии, позволяя рассматривать лейкоз КРС как перспективную модель для изучения эффективности препаратов и создания новых схем химиотерапии злокачественной патологии крови. Целесообразно продолжение исследования клеточных и молекулярных механизмов действия препарата.
Библиографическая ссылка
Плотников Е.В., Плотников В.М. ИССЛЕДОВАНИЕ ПРОТИВОЛЕЙКОЗНОЙ АКТИВНОСТИ НОВОГО СЕРЕБРОСОДЕРЖАЩЕГО ПРЕПАРАТА НА МОДЕЛИ ВИРУСНОГО ЛЕЙКОЗА КРС // Международный журнал прикладных и фундаментальных исследований. 2017. № 3-1. С. 89-91;URL: https://applied-research.ru/en/article/view?id=11406 (дата обращения: 17.05.2026).

