Scientific journal
International Journal of Applied and fundamental research
ISSN 1996-3955
ИФ РИНЦ = 0,556
PREPARATION OF COMPOUND OF AGASS2 AND AG3ASS3 BY HYDROTHERMAL METHOD
Тиоарсениты серебра (I) (AgAsS2 и Ag3AsS3) относятся к числу важных функциональных материалов современной техники. Большинство соединений этого класса широко используются или считаются перспективными материалами с ценными полупроводниковыми, фото-, сегнето- и термоэлектрическими свойствами [1, 3–12].
В системе Ag2S–As2S3 известны соединения составов AgAsS2 и Ag3AsS3. Эти соединения обладают уникальными полупроводниковыми свойствами [1, 2]. Соединение AgAsS2 плавится при 423°С, полиморфное превращение происходит при 321°С и согласно [1] низкотемпературная модификация (T<321°С) кристаллизуется в ромбический (Пр. гр. 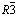 : а=1,398, с=0,912 nm), а высокотемпературная в гексагональной (Пр. гр.
: а=1,398, с=0,912 nm), а высокотемпературная в гексагональной (Пр. гр. 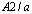 : a=1,723, b=0,778, c=1,519 nm; b=101,2o) структурах [1, 4, 6, 7]. Это соединение разлагается при температуре выше 500°С [1–6].
: a=1,723, b=0,778, c=1,519 nm; b=101,2o) структурах [1, 4, 6, 7]. Это соединение разлагается при температуре выше 500°С [1–6].
Соединение Ag3AsS3 плавится при 491°С, полиморфное превращение соединения Ag3AsS3 происходит при 195°С. Низкотемпературная модификация (T<195°С) кристаллизуется в ромбический (Пр. гр. 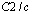 : a=1,200, b=0,626, c=1,708 nm; b=110o), а высокотемпературная в гексагональной (Пр. гр.
: a=1,200, b=0,626, c=1,708 nm; b=110o), а высокотемпературная в гексагональной (Пр. гр. 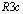 : a=1,083, c=0,865 nm; b=103,52o) структурах [8–12].
: a=1,083, c=0,865 nm; b=103,52o) структурах [8–12].
Из литературных данных [1–12] известно, что тиоарсениты серебра синтезируются при высоких температурах (450–500°С) в вакуумированных (∼10–2 Па) кварцевых ампулах путем сплавления элементных компонентов или сульфида серебра (I) с сульфидом мышьяка (III). Для гомогенизации этих соединений требуется высокая температура и слишком много времени. В связи с этим, получение тиоарсенитов серебра (I) в растворе при низких температурах является одним из наиболее актуальных вопросов.
В статье приведены результаты исследования условий получения соединений AgAsS2 и Ag3AsS3 в водных растворах гидротермальным методом.
Экспериментальная часть и результаты. В качестве исходных компонентов в синтезе соединений AgAsS2 и Ag3AsS3 были использованы как химически чистые соединения AgNO3, NaAsO2, Na3AsO3 и CH3–CS–NH2. Смеси исходных компонентов при их мольном соотношении AgNO3/NaAsO2=1:1 и AgNO3/Na3AsO3=3:1 (ммол) растворяют в 20 мл дистиллированной водs и к этому раствору приливают стехиометрического количество раствора тиоацетамида. Полученные растворы перемешивают при температуре 70°С в течении 15 минут, затем экспериментальный сосуды помещают в тефлонный автоклав (100 мл). Автоклав закрывают и помещают в микроволновый (Speedwave four BERGHOF – Германия) электрический нагреватель. Реакционную смеси нагревают до 180°С в течение 24 часов. После синтеза осадки фильтруют через стеклянный фильтр. Осадки промывают ультрачистой водой и в течение 1 часа высушивается при 80°С в вакууме.
Получение соединений AgAsS2 и Ag3AsS3 можно написать следующими уравнениями:
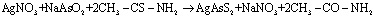
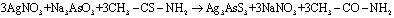 .
.
В этих условиях pH среды раствора меняется в интервале 4,6. Известно, что продукт реакции – ацетамид при слабо кислой среде гидролизуется:
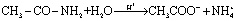
Присутствие ионов ацетата и аммония уменьшает поверхностное взаимодействие частиц и играет роль стабилизатора.
Индивидуальность синтезированных соединений контролировали методами РФА (2D PHASER “Bruker”, CuKa, 2q, 20–80 град.) и ДТА (пирометр НТР-70, прибор Термоскан-2, инертная атмосфера). По данным РФА (рис. 1) установлено, что пики соответствующие максимальной интенсивности соединений AgAsS2 и Ag3AsS3 согласуются с результатами других работ [1, 6–12]. В составе присутствует низкотемпературная модификация соединений AgAsS2 и Ag3AsS3. В параметрах решетки наблюдается частичное уменьшение: AgAsS2 (Пр. гр.: 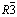 ) а=1,3781, с=0,8892 nm; Ag3AsS3 (Пр. гр.:
) а=1,3781, с=0,8892 nm; Ag3AsS3 (Пр. гр.:  ) a=1,1988, b=0,6021, c=1,6968 nm. Причиной этого является присутствие некомпенсированных связей между атомами мелких частиц соединений AgAsS2 и Ag3AsS3.
) a=1,1988, b=0,6021, c=1,6968 nm. Причиной этого является присутствие некомпенсированных связей между атомами мелких частиц соединений AgAsS2 и Ag3AsS3.
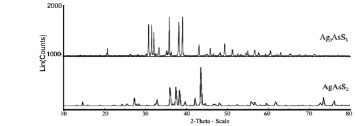
Рис. 1. Дифрактограмма соединений AgAsS2 и Ag3AsS3
По данным РФА установлено, что при синтезе соединения AgAsS2 при температуре 180°С, в кислой среде (pH=3, в присутствии H2SO4) основной состав полученного осадка составляет Ag3AsS3. Установлено, что соединение AgAsS2 устойчиво в интервале pH=4,8.
Методом ДТА исследована температура полиморфного превращения и температура плавления соединений. Установлено, что температуры полиморфных превращений полученных соединений AgAsS2 и Ag3AsS3 составляют 317°С и 191°С соответственно. Соединение AgAsS2 плавится при 416°С, а соединение Ag3AsS3 – 487°С. Низкое значение температуры плавления и полиморфного превращения можно объяснить тем, что эти соединения присутствуют в виде наночастиц. Известно, что температура плавления веществ в виде наночастиц несколько меньше температуры плавления монокристалла.
Микроморфология полученных соединений исследована на микроскопе марки HITACHI TM3000. Установлено, что состав полученных осадков состоит из наночастиц (рис. 2).
Из микрофотографии видно, что состав соединений состоит из несферических форм наночастиц и между ними наблюдается высокая адгезия. В больших агрегатах соединений AgAsS2 и Ag3AsS3 наблюдается высокая пористость.
Для уточнения стехиометрического состава соединений AgAsS2 и Ag3AsS3 проведен термогравиметрический анализ (прибор Fascinating Flexibility in thermal Analysis STA 449F3). По данным полученных термограмм определены весовое и атомное соотношение в составе соединений (табл. 1).
Из результатов показанных в табл. 1 были составлены простые формулы соединений. Установлено, что в составе соединений AgAsS2 и Ag3AsS3 присутствует излишнее количество серы (0,005–0,01 %). Это можно объяснить тем, что при гидролизе исходных компонентов – тиоацетамида в составе присутствует определенное количество свободной серы, что входит в состав полученных тиоарсенитов серебра.
В работе также было изучено влияние pH среды (pH METER-pH410 «АКВИЛОН») и температуры на полное осаждение соединений AgAsS2 и Ag3AsS3. Для получения в растворе кислой среды использовали 0,1 M серную кислоту и при различных значениях pH среды в температурном интервале 100–180°С контролировали выход продукта. Влияние pH среды и температуры на полное осаждение соединений AgAsS2 и Ag3AsS3 представлено в табл. 2.

Рис. 2. Микрофотография соединений AgAsS2 (a) и Ag3AsS3 (b)
Таблица 1
Результаты элементного анализа полученных соединений
|
Соединения |
Элементный состав, % |
|||||
|
Ag, вес. |
Ag, ат. |
As, вес. |
As, ат. |
S, вес. |
S, ат. |
|
|
AgAsS2 |
43,70 |
24,99 |
30,36 |
24,98 |
25,94 |
50,03 |
|
Ag3AsS3 |
65,45 |
42,91 |
15,15 |
14,16 |
19,40 |
42,93 |
Таблица 2
Результаты исследования влияния pH-среды и температуры на выход соединений AgAsS2 и Ag3AsS3
|
Температура, °С |
pH |
Выход соединений, % |
|
|
AgAsS2 |
Ag3AsS3 |
||
|
100 |
4 |
93,31 |
92,59 |
|
120 |
5 |
94,67 |
95,52 |
|
140 |
6 |
96,84 |
97,68 |
|
160 |
7 |
96,68 |
97,49 |
|
180 |
8 |
96,52 |
96,83 |
Установлено, что максимальный выход соединений AgAsS2 и Ag3AsS3 наблюдается при pH=6–8 и при температуре 140-180°C.
Вывод: на основе исходных соединений AgNO3, NaAsO2, Na3AsO3 CH3–CS–NH2 получены наноразмерные соединения AgAsS2 и Ag3AsS3 и доказана их индивидуальность. В параметрах решетки и в значении температуры плавление наноразмерных соединений AgAsS2 и Ag3AsS3 наблюдается частичное уменьшение.
Библиографическая ссылка
Гусейнов Г.М., Сулейманова Т.И. ПОЛУЧЕНИЕ СОЕДИНЕНИЙ AGASS2 И AG3ASS3 ГИДРОТЕРМАЛЬНЫМ МЕТОДОМ // Международный журнал прикладных и фундаментальных исследований. 2017. № 3-2. С. 228-231;URL: https://applied-research.ru/en/article/view?id=11432 (дата обращения: 24.05.2026).

