Scientific journal
International Journal of Applied and fundamental research
ISSN 1996-3955
ИФ РИНЦ = 0,556
THE ARCHITECTURE OF PHARMACEUTICAL BUILDINGS BASED ON THE DESIGN OF CLEAN ROOMS IS CONSIDERED IN THIS ARTICLE
Чистые помещения используются в различных отраслях промышленности, науке и медицине, в производственных и исследовательских проектах. В зданиях фармацевтического производства: «чистое помещение» – помещение-барьер, защищённое от проникновения всевозможных загрязнений, в котором проводятся действия и операции, требующие обязательной стерильности в целях получения безопасного продукта, по причине того, что строительные конструкции и отделочные материалы, технологическое оборудование и работающий персонал являются источниками различных загрязнений в виде миллионов частиц. Цель чистого помещения – контроль распространения частиц и обеспечение производства лекарственной продукции в чистой среде [1]. Стерильности производства способствует: принудительная вентиляция с фильтрацией поступающего воздуха; специальные материалы ограждающих конструкций стен и покрытий полов; требуемая организация тепло-, водо-, электроснабжения; а также, расположение зон основного «чистого» производства и вспомогательных помещений по принципу «матрёшки» (рис. 1). Пространства-оболочки помещений различных классов чистоты встраиваются друг в друга по мере с понижения класса чистоты, где «воздушный шлюз» – буферная зона между чистыми помещениями и ограждающими конструкциями здания или вспомогательными и административно-бытовыми помещениями.
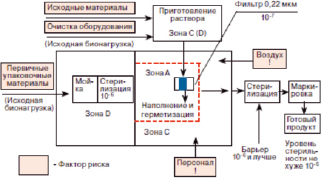
Рис. 1. Принципиальная схема производства с финишной стерилизацией [3]
Проектирование чистых помещений – очень ответственная задача, где нужно уделить особое внимание схемам потоков поступления исходного сырья, тщательно продуманному перемещению персонала, размещению оборудования и его дальнейшему перемещению и критическим производственным операциям. Так как производство стерильных лекарственных препаратов требует выполнения критических операций в чистой среде, где производимый продукт должен быть защищён от воздействий окружающей среды, персонала, отмечается ряд обязательных методов проектирования чистых помещений.
Согласно требованиям концепции стерильного производства, чистое помещение должно находиться в соответствующей окружающей среде, гарантирующей минимальный риск контаминации или перекрёстного загрязнения. Возможность возникновения перекрестной контаминации от производственных процессов, персонала и проникновения насекомых или животных максимально должна быть предотвращена путём правильной планировочной структуры помещений, соответствующей логической последовательности главных технологических операций. Путь персонала в чистое помещение должен следовать исключительно через воздушные шлюзы, спроектированные с учетом требований GMP (Надлежащей производственной практики – управления качеством, гарантирующей и контролирующей стандарты качества производства), перемещение – оптимальным, без перекрёстных встреч с потоками исходного сырья или готовой продукции [4].
Требуемому уровню чистоты способствует рациональное решение оптимальной объемно-планировочной структуры производственного здания, определяющее основные части в зависимости от класса чистоты: производственная зона и зона технической поддержки, вспомогательные помещения, зона складирования и административная зона (рис. 2). Планировочно-технологические требования к проекту фармацевтического предприятия подразделяются на требования к технологической схеме объекта и требования к планировке отдельных помещений, касающиеся взаимосвязей производственных помещений и организаций материальных потоков, персонала, различных грузов и пищи. Выбор планировочного решения помещений, строительных материалов, а также материалов и конструкций оборудований должен минимизировать риск ошибок во время работы, обслуживания и проведения эффективной уборки, т.е. устранять любой фактор, отрицательно влияющий на качество продукции.
Задача интегрированной схемы функциональной структуры производства состоит в организации потоков перемещения основного и вспомогательного сырья, персонала, готовой продукции, вспомогательных материалов и исключении нежелательных пересечений между ними. Она включает в себя определение основных входов и выходов для каждого из потоков в отдельности, размещение инженерно-технической оснастки и инженерно-технологического оборудования, трубопроводов [5]. При этом основным технологическим принципом является организация кратчайшей связи между функциональными зонами при условии их максимальной изоляции.
Так как все гигиенические зоны для критических и других технологических операций делятся по классам чистоты на зоны А, В, С и D, в зависимости от допустимого содержания аэрозольных частиц, основу архитектурно-планировочного решения фармацевтического производства составляют специфические особенности проектирования, которые зависят от технологии производства лекарственных препаратов, базирующейся на соответствующих регламентах и стандартах надлежащего производства в целях получения качественной готовой продукции. Например, в помещении класса D проводятся операции с материалами после мойки, в зоне класса С – приготовление растворов, подлежащих фильтрации, а в зоне класса А – приготовление раствора в асептических условиях и наполнение ампул при необычайно высоком риске [1, 2]. Эксплуатация этих помещений предусматривает постоянный контроль над воздушной средой, кондиционированием и вентиляцией, что в свою очередь, классифицирует чистые помещения на турбулентно вентилируемые и помещения с однонаправленным воздушным потоком.
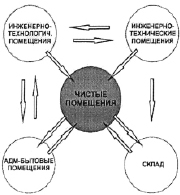
Рис. 2. Схема функциональной зависимости зон фармацевтических предприятий [5]
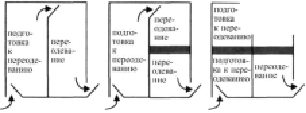
Рис. 3. Схема зоны переодевания с двумя комнатами с поперечной скамьёй и без неё [1]
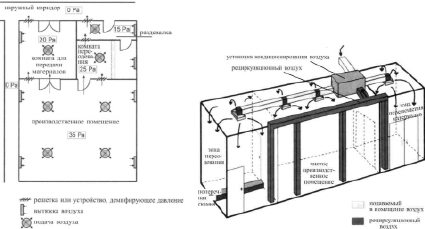
Рис. 4. Схемы несложных комплексов чистых помещений [1]
Рядом с основными чистыми помещениями с производством необходимо расположить чистые помещения вспомогательного назначения, в зависимости от вида производимого продукта и от сложности поставленных задач и целей. На рис. 4 демонстрируется комплекс чистых помещений с комнатой переодевания для персонала (с поперечной скамьёй или без неё, делящей комнату на две зоны различной чистоты (рис. 3)) и комнатой для передачи сырья из которой перемещается в производственное чистое помещение или в которую поступает готовая продукция. Эти мероприятия способствуют предотвращению перекрестных встреч потоков исходного сырья и материалов и путей персонала в целях минимизации риска контаминаций согласно требованиям GMP. В этих же комплексах чистых помещений могут проектироваться дополнительные чистые помещения для хранения и подготовки материалов, дополнительные раздевалки, промежуточные склады и передаточные шлюзы.
Касаемо материалов, используемых в строительстве чистых помещений, можно утверждать следующее: по сравнению со строительством обычных помещений, к качеству чистых помещений предъявляются более высокие требования. К ним относятся: герметичность; гладкость отделки, обеспечивающая легкую очистку; прочность и износостойкость материалов; стойкость к воздействию агрессивных сред в процессе производства; отсутствие ненужных выступов, отверстий и углублений на внутренних поверхностях в целях минимизации загрязнений.
Таким образом, в основе проектирования зданий фармацевтического производства лежит необходимость повышения качества выпускаемой лекарственной продукции путём следования всем требованиям и нормам, предъявляемым к проектированию чистых помещений для критических операций. Конкурентоспособность фармацевтической продукции, производимой в Казахстане, зависит от слаженного взаимодействия специалистов фармацевтического производства с архитекторами, которым необходимо изучить требуемые стандарты проектирования объектов фармацевтической промышленности для интеграции фармацевтической отрасли Казахстана в мировую систему.
Библиографическая ссылка
Баракова А.Ш., Мурзагалиева Э.Т., Остапенко И.И. ОСОБЕННОСТИ ПРИ ПРОЕКТИРОВАНИИ ЧИСТЫХ ПОМЕЩЕНИЙ НА ПРИМЕРЕ ФАРМАЦЕВТИЧЕСКИХ ПРЕДПРИЯТИЙ // Международный журнал прикладных и фундаментальных исследований. 2017. № 7-1. С. 7-10;URL: https://applied-research.ru/en/article/view?id=11681 (дата обращения: 17.05.2026).

