Scientific journal
International Journal of Applied and fundamental research
ISSN 1996-3955
ИФ РИНЦ = 0,556
VIBRATIONAL SPECTRA OF THE UNCHARGED CONFORMERS OF CYSTEINE AND SELENOCYSTEINE
Цистеин (Cys) играет особую, неповторимую роль в формировании структуры белков, поскольку именно с его участием образуются поперечные сшивки между полимерными белковыми молекулами. Молекулы Cys содержат реакционно-способные сульфгидридные группы –SH, которые взаимодействуют между собой, образуя дисульфидные мостики –S-S-. Во многих случаях свойства Cys зависят не только от фазового состояния, но и от его конформации [1, 2]. При этом идентификация и исследование различных конформеров Cys, как и его структурного аналога селеноцистеина (Sec), затруднено из-за небольшой величины энергетического барьера.
Цель работы – выполнить интерпретацию колебательных спектров двух незаряженных конформеров Cys, как и Sec, в газовой фазе и определить характерные спектральные особенности каждого конформера.
Расчёт был выполнен методом DFT (базис 6-311++G(d,p)) с использованием программного продукта Gaussian-09 [3].
Цистеин
Молекулярные диаграммы двух конформеров Cys1 и Cys2, полученных в результате вращения связи SH вокруг связи SC, приведены на рис. 1. Согласно результатам расчёта, значение полной энергии Cys1 всего на 0,48 ккал/моль меньше полной энергии Cys2, что, как отмечалось выше, затрудняет экспериментальное исследование свойств Cys определённой конформации.
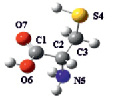
а б
Рис. 1. Молекулярные диаграммы Cys1 (a) и Cys2 (б) с обозначением и нумерацией атомов
В ИК спектрах конформеров Cys1 и Cys2 (табл. 1) наибольшую интенсивность имеют полосы поглощения, отвечающие деформационным колебаниям 11, 15, 20 и 29, формы которых содержат изменения углов СОН, NH2 и валентной связи С=О. В спектрах КР наиболее интенсивными для обоих конформеров являются линии, отвечающие колебаниям 12, 29. Кроме этого, для Cys2 имеется ещё одна линия сильной интенсивности, отвечающая колебанию с частотой 730 см-1, т.е. в спектре данного соединения проявляются две близлежащие линии сильной интенсивности.
Таблица 1
Экспериментальные [4] (nэксп) и вычисленные значения частот колебаний в гармоническом и ангармоническом приближениях (nг, nанг, cм-1)
и интенсивностей спектров ИК (IИК, км/моль) и КР (IКР, Å4/а.е.м.) Cys1 и Cys2
|
№ |
νэксп (Iотн ) |
Cys1 |
Cys2 |
Отнесение |
||||||
|
νг |
νанг |
IИК |
IКР |
νг |
νанг |
IИК |
IКР |
|||
|
9 |
484 |
477 |
34,2 |
1,7 |
478 |
472 |
25,8 |
3 |
γ (SCN), γ (OCN) |
|
|
10 |
596 |
577 |
32,9 |
2,7 |
614 |
597 |
42,3 |
2,1 |
β(OH), β(CH2) |
|
|
11 |
626 |
590 |
89,4 |
2,4 |
638 |
630 |
78,3 |
3,3 |
β(OH), β(CH2) |
|
|
12 |
715 |
693 |
11,9 |
15,3 |
730 |
719 |
9,5 |
12,1 |
Q(CS) |
|
|
13 |
770 |
749 |
46,8 |
3,5 |
745 |
735 |
19,5 |
12,4 |
γ (CCN) |
|
|
14 |
781 |
762 |
8,9 |
5,2 |
800 |
781 |
37,2 |
1,9 |
β(SH), γ (CCO) |
|
|
15 |
821 |
878 |
117,1 |
1,5 |
827 |
789 |
102,3 |
0,7 |
β(NH2) |
|
|
16 |
867 |
824 |
37,8 |
6,5 |
870 |
829 |
58,2 |
4,6 |
β(SH), β(NH2,CH2) |
|
|
17 |
991 |
959 |
13,9 |
2,7 |
1007 |
991 |
13,5 |
3,4 |
β(NH2), β(CH2) |
|
|
18 |
1039 |
1006 |
18,6 |
3,5 |
1014 |
989 |
22,6 |
4,1 |
β(SH), β(NH2) |
|
|
19 |
1097 |
1059 |
56,4 |
9,2 |
1101 |
1068 |
18,5 |
6,6 |
Q(C-N) |
|
|
20 |
1118 (0,74) |
1147 |
1110 |
249,7 |
1,2 |
1144 |
1111 |
262,4 |
1,4 |
Q(C-O) |
|
21 |
1160 |
1134 |
6,5 |
1,6 |
1182 |
1159 |
3,2 |
2,8 |
β(NH2), β(CH2,CH) |
|
|
22 |
1248 |
1216 |
10,6 |
5,6 |
1236 |
1204 |
12 |
3,8 |
β(NH2), β(CH2,CH) |
|
|
23 |
1293 |
1255 |
4,8 |
4,1 |
1292 |
1270 |
4,8 |
6,3 |
β(OH) |
|
|
24 |
1316 |
1279 |
16,1 |
3,1 |
1321 |
1289 |
14,9 |
2,9 |
β(CH2) |
|
|
25 |
1394 |
1352 |
3,3 |
4,2 |
1388 |
1352 |
19,7 |
4,0 |
Q(C2C3) |
|
|
26 |
1364 (0,28) |
1400 |
1372 |
23,7 |
4,1 |
1410 |
1386 |
11,8 |
5,2 |
β(CH) |
|
27 |
1462 |
1431 |
11,7 |
6,6 |
1466 |
1445 |
12,3 |
6,8 |
β(CH2) |
|
|
28 |
1627 (0,16) |
1658 |
1628 |
33,8 |
2,2 |
1660 |
1660 |
32,4 |
2,2 |
β(NH2) |
|
29 |
1782 (1,0) |
1799 |
1766 |
275,7 |
10,9 |
1806 |
1774 |
275,3 |
8,8 |
Q(C=O) |
|
30 |
2676 |
2508 |
0,5 |
93,1 |
2661 |
2501 |
5,3 |
118,6 |
Q(SH) |
|
|
31 |
3075 |
2960 |
5,6 |
133,5 |
3071 |
2965 |
4,2 |
125,2 |
Q(CH2) sym, q(CH) |
|
|
32 |
2952 (0,1) |
3086 |
2948 |
7,6 |
30,9 |
3085 |
2951 |
12,2 |
29,5 |
Q(CH2) sym, q(CH) |
|
33 |
3133 |
2981 |
2,9 |
46,7 |
3132 |
2983 |
2,7 |
53,6 |
q(CH2) asym |
|
|
34 |
3500 |
3333 |
2,4 |
122,4 |
3497 |
3369 |
2,2 |
126,9 |
q(NH2) sym |
|
|
35 |
3587 |
3423 |
7,0 |
64,5 |
3581 |
3408 |
7,2 |
67,9 |
q(NH2) asym |
|
|
36 |
3572 (0,32) |
3749 |
3548 |
69,3 |
141,3 |
3741 |
3540 |
62,5 |
152,9 |
q(OH) |
Максимальные отличия частотных смещений в спектрах Cys 1 и Cys 2 наблюдаются для колебаний 13, 14 (DCys1 = 9, DCys2 = 56 см-1);
20, 21 (DCys1 = 13, DCys2 = 37 см-1) и 25, 26 (DCys1 = 6, DCys2 = 23 см-1). Это приводит к тому, что в спектрах (ИК и КР) Cys 1 и Cys 2 слабые по интенсивности полосы поглощения проявляются как плечи на близлежащих более интенсивных полосах поглощения, что наблюдается для колебаний с частотами 781, 1160, 1394 см-1 в ИК спектре Cys 1.
Учёт механического ангармонизма привёл к существенному улучшению согласия между экспериментальными и вычисленными частотами по сравнению с отнесением, выполненным в работе [4]. Если расхождение между вычисленными и экспериментальными частотами колебаний (табл. 1) составляет для средней и высокочастотной области 6 и 14 см-1 соответственно, то, например, в работе [5] расхождение между аналогичными частотами составляет 140 см-1. Одной из основных причин такого существенного отличия теоретических и экспериментальных частот, имеющих место в работе [5], является сравнение авторами частот колебаний, вычисленных для незаряженной молекулярной структуры Cys, с экспериментальными частотами, измеренными для Cys в твёрдом состоянии, где, как известно, аминокислоты существуют в цвиттер-ионной форме.
Согласно выполненному расчёту в колебательном спектре Cys2, одно из низкочастотных колебаний имеет отрицательное значение. Как известно, седловая точка первого порядка характеризуется одним мнимым колебанием и имеет более низкое значение энергии, чем текущее, т.е. является переходным состоянием. Смещения атомов (или формы колебаний) изображают деформацию молекулы при колебаниях в переходном состоянии. Так как состояние, характеризуемое наличием седловой точки, неустойчиво, то анализ деформаций, отвечающих мнимым колебаниям, позволяет выявить структурные изменения, приводящие к перестройке молекулярной структуры при её дальнейшем переходе в состояние с минимумом потенциальной энергии. Форма данного колебания характеризуется смещением атома Н относительно атома S с одновременным вращением связи SH относительно связи CS, что может привести к конформерному превращению Cys1 в Cys2, что вполне возможно, учитывая, что отличие полных энергий этих конформеров меньше 0,5 ккал/моль.
Выполненный расчёт колебательных спектров изолированных конформеров Cys1 и Cys2 показал, что каждый из них имеет характерные полосы поглощения и линии КР, позволяющие однозначно выполнять их идентификацию и определять присутствие в смеси.
Селеноцистеин
На рис. 2 приведены молекулярные диаграммы двух конформеров Sec, а в табл. 2 – результаты расчёта колебательных спектров.
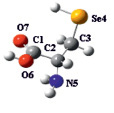
Sec1 Sec2
Рис. 2. Молекулярные диаграммы конформеров цистеина с обозначением и нумерацией атомов
Таблица 2
Вычисленные значения частот колебаний в гармоническом и ангармоническом приближениях (nг, nанг, cм-1) и интенсивностей спектров ИК (IИК, км/моль)
и КР (IКР, Å4/а.е.м.) Sec1 и Sec2
|
№ кол. |
Sec1 |
Sec2 |
Отнесение |
||||||
|
νг |
νанг |
IИК |
IКР |
νг |
νанг |
IИК |
IКР |
||
|
1 |
40 |
43 |
2,1 |
1,2 |
29 |
22 |
2,3 |
1,5 |
τ(COO) |
|
2 |
81 |
57 |
0,2 |
0,5 |
76 |
75 |
0,1 |
0,5 |
τ(CCC) |
|
3 |
155 |
124 |
0,3 |
0,2 |
149 |
117 |
0,3 |
0,2 |
τ(NH2) |
|
4 |
198 |
234i |
6,8 |
0,4 |
198 |
155i |
3,1 |
0,2 |
τ(SeCC) |
|
5 |
251 |
244 |
3,5 |
0,3 |
252 |
252 |
9,8 |
1,3 |
τ(CH), τ(NH2) |
|
6 |
265 |
235 |
5,6 |
1,8 |
267 |
244 |
8,2 |
0,3 |
τ(SeH), τ(NH2) |
|
7 |
297 |
233 |
26,7 |
2,7 |
296 |
272 |
21,1 |
3,2 |
τ(NH2) |
|
8 |
329 |
284 |
18,5 |
2,6 |
322 |
289 |
19,8 |
1,8 |
γ (SeCN), γ (CCN) |
|
9 |
475 |
468 |
27,6 |
2,4 |
470 |
465 |
25,2 |
3,5 |
γ (SeCN), γ (OCN) |
|
10 |
595 |
582 |
32,1 |
3,6 |
604 |
589 |
14,4 |
2,4 |
β(OH), β(CH2) |
|
11 |
625 |
613 |
95,3 |
4,1 |
628 |
603 |
108,8 |
10,1 |
β(OH), β(CH2) |
|
12 |
651 |
639 |
10,5 |
14,5 |
659 |
644 |
4,9 |
9,8 |
Q(CSe) |
|
13 |
725 |
704 |
2,7 |
6,6 |
719 |
694 |
6,5 |
14,3 |
β(SeH), γ (CCN) |
|
14 |
765 |
750 |
32,6 |
7,9 |
782 |
754 |
44,8 |
2,3 |
β(SeH), γ (CCO) |
|
15 |
813 |
789 |
78,9 |
1,2 |
804 |
777 |
59,7 |
2,6 |
β(NH2) |
|
16 |
845 |
755 |
89,7 |
4,7 |
847 |
734 |
103,1 |
3,5 |
β(SeH), β(NH2), β(CH2) |
|
17 |
954 |
928 |
23 |
2,6 |
958 |
929 |
28,1 |
4,5 |
β(NH2), β(CH2) |
|
18 |
1013 |
982 |
13,6 |
4,9 |
1008 |
983 |
14,3 |
4,3 |
β(SeH), β(NH2) |
|
19 |
1092 |
1055 |
52,1 |
8,7 |
1094 |
1057 |
28,7 |
7,5 |
Q(C-N) |
|
20 |
1134 |
1103 |
76,3 |
1,5 |
1139 |
1105 |
170,3 |
1,6 |
Q(C-O), β(CH2) |
|
21 |
1148 |
1110 |
186,2 |
1,4 |
1153 |
1121 |
96,5 |
1,6 |
Q(C-O), β(CH2) |
|
22 |
1228 |
1194 |
8,5 |
4,2 |
1218 |
1187 |
8,9 |
3,9 |
β(NH2), β(CH2), β(CH) |
|
23 |
1273 |
1234 |
17,5 |
11,6 |
1277 |
1248 |
17,8 |
11,8 |
β(OH) |
|
24 |
1305 |
1260 |
9,2 |
4,3 |
1306 |
1265 |
7,4 |
4,8 |
β(CH2) |
|
25 |
1395 |
1355 |
7,8 |
3,8 |
1393 |
1356 |
20,2 |
3,4 |
Q(CC) |
|
26 |
1401 |
1355 |
20,9 |
4,8 |
1407 |
1372 |
12,1 |
6,4 |
Q(CC) |
|
27 |
1458 |
1422 |
11,2 |
6,7 |
1460 |
1419 |
12,5 |
6,6 |
β(CH2) |
|
28 |
1657 |
1650 |
33,0 |
1,9 |
1658 |
1611 |
31,6 |
1,9 |
β(NH2) |
|
29 |
1802 |
1769 |
266,7 |
9,9 |
1805 |
1774 |
268,7 |
9,7 |
Q(C=O) |
|
30 |
2372 |
2419 |
8,6 |
110,4 |
2356 |
2441 |
20,2 |
139,3 |
q(she) |
|
31 |
3085 |
2951 |
3,1 |
133,7 |
3080 |
2946 |
2,3 |
125,8 |
q(CH2) sym, q(CH) |
|
32 |
3091 |
2952 |
6,5 |
24,4 |
3091 |
2957 |
9,5 |
16,4 |
q(CH2) sym, q(CH) |
|
33 |
3146 |
2996 |
1,6 |
42,1 |
3149 |
2998 |
1 |
52,6 |
q(CH2) asym |
|
34 |
3498 |
3371 |
2 |
135,6 |
3497 |
3365 |
1,8 |
139,4 |
q(NH2) sym |
|
35 |
3585 |
3415 |
6,8 |
70,8 |
3582 |
3415 |
7 |
72,7 |
q(NH2) asym |
|
36 |
3747 |
3556 |
68,5 |
141,9 |
3743 |
3545 |
65,1 |
148,9 |
q(OH) |
Как и в случае Cys, в ангармоническом приближении частота колебания 4 имеет отрицательное значение. В отличие от Cys, мнимое колебание характерно для обоих конформеров Sec1 и Sec2, потенциальный барьер между которыми составляет 0,19 ккал/моль, что в 2,5 раза меньше аналогичной величины для конформеров Cys1 и Cys2.
Сравнение колебательных спектров двух конформеров Sec1 и Sec2 показывает, что основное отличие ИК спектров наблюдается в области проявления колебаний 20, 21 и 25, 26 – интенсивности полос поглощения в этих парах колебаний соответственно уменьшаются или возрастают в ~2 раза, что связано с поворотом связи Se-H относительно связи Se-C.
В спектрах КР основное отличие конформеров связано с изменением интенсивности линий для колебаний 12 и 13 – они так же, как и в спектрах ИК, уменьшаются и возрастают в ~1,52 раза.
Выводы
Таким образом, расчёт колебательных спектров незаряженных конформеров Cys и Sec показал, что при интерпретации колебательных спектров аминокислот в газовой фазе необходимо учитывать возможность одновременного существования обоих конформеров 1 и 2.
Интерпретация ИК и КР колебательных спектров, выполненная с учётом ангармонизма колебаний, показала, что каждый конформер Cys и Sec имеет характерные линии, специфичность проявления которых даёт возможность определить присутствие конформеров в смеси аминокислот.
Библиографическая ссылка
Тен Г.Н., Щербакова Н.Е., Баранов В.И. КОЛЕБАТЕЛЬНЫЕ СПЕКТРЫ НЕЗАРЯЖЕННЫХ КОНФОРМЕРОВ ЦИСТЕИНА И СЕЛЕНОЦИСТЕИНА // Международный журнал прикладных и фундаментальных исследований. 2017. № 8-2. С. 221-225;URL: https://applied-research.ru/en/article/view?id=11789 (дата обращения: 04.06.2026).

