Scientific journal
International Journal of Applied and fundamental research
ISSN 1996-3955
ИФ РИНЦ = 0,556
FIRST DESCRIPTION OF ENTEROCYTOZOONIDAE (FUNGI: MICROSPORIDIA) IN FISH FROM LAKE BAIKAL
Микроспоридии – одноклеточные эукариоты, являющиеся облигатными внутриклеточными паразитами многоклеточных животных. Различные виды микроспоридий обнаружены у широкого спектра хозяев, от беспозвоночных до людей, и могут вызывать серьезные патологии вплоть до летального исхода. Так, описаны эпизоотические вспышки микроспоридиозов, имевшие серьезные экономические последствия для аквакультуры рыб и беспозвоночных. Кроме того, некоторые из них считаются потенциальной угрозой для свободноживущих популяций рыб, например, в Красном море [9, 10, и др.].
Несмотря на сравнительно высокий уровень изученности животных озера Байкал, данные о видовом составе паразитических простейших пищеварительной системы рыб до сих пор являются неполными [1, 4, 6]. Использование молекулярно-генетических методов, включающих секвенирование генов рибосомного оперона посредством выделения ДНК и амплификации, позволяет не только существенно расширить наши знания о паразитофауне рыб, но и скорректировать уже имеющиеся данные. Так, молекулярно-генетический анализ ассоциированной микрофлоры кишечника черного байкальского хариуса Thymallus baicalensis Dybowski, 1874 позволил выявить генотип Spironucleus barkhanus (Diplomonadida: Hexamitidae) [2], ранее описанный как Hexamita sp. [4].
Желтокрылка Cottocomephorus grewingkii (Dybowski, 1874) (Cottidаe) является одним из наиболее многочисленных представителей ихтиоценоза мелководной зоны Байкала. В пределах вида выделяют три разновременно нерестующих стада: мартовское, майское и августовское [5, 7]. В зависимости от сроков нереста и температурного режима у разновременно нерестующих стад желтокрылки инкубационный период развития кладок составляет от 20 до 80–90 суток [7]. С момента нереста до выхода из кладки личинок её оберегает самец: обмахивает кладку плавниками, улучшая аэрацию потоком воды, удаляет из неё погибшие икринки и охраняет кладку от хищников. В течение всего этого периода рыбы не питаются, что позволяет определять состав собственной микрофлоры их пищеварительной системы.
Целью исследования явился анализ эукариотической микрофлоры кишечника самцов желтокрылки в нерестовый период методом молекулярно-генетической детекции фрагментов генов малой субъединицы рРНК.
Материалы и методы исследования
Объектом исследования стали самцы желтокрылки в период инкубации икры. Рыб собирали на кладках с помощью легкого водолазного снаряжения в Лиственничном заливе оз. Байкал 28–31 мая (6 экз.) и 18 августа (6 экз.) 2012 г. Фрагменты кишечника свежевыловленных рыб отбирали в асептических условиях. Выделение ДНК проводили с использованием коммерческих наборов «ДНК-сорб-B» (АмплиСенс, Москва) в соответствии с рекомендациями фирмы-производителя. Полученные образцы нуклеиновых кислот анализировали методом ПЦР с использованием набора «Taq DNA Polymerase» (QIAGEN, Германия) и универсальных эукариотических праймеров DpFun 5’- GCCAGCAGCCGCGGTAATTCC и DpRUn 5’- GAGCGACGGGCGGTGTGTAC [8] в режиме 94 °C/20 сек.; 68 °C/20 сек.; 72 °C/30 сек. (35 циклов). Продукты амплификации анализировали в 2 % агарозном геле. Ампликоны длиной менее 1090 п.н. вырезали и клонировали в плазмидном векторе CloneJET™ PCR Cloning Kit (FERMENTAS, Литва). Плазмидную ДНК из выросших колоний секвенировали с использованием предлагаемых в наборе праймеров. Сравнительный анализ нуклеотидных последовательностей c международной базой генетических данных GenBank проводили с помощью программы BLAST (URL: http://blast.ncbi.nlm.nih.gov). Нуклеотидные последовательности выравнивали с помощью программы Clustal W 2.0.10. Редактирование выровненных последовательностей проводили с использованием пакета программы BioEdit. Филогенетический анализ проводили с помощью пакета программ Mega v.6.06.
Результаты исследования и их обсуждение
К настоящему времени в составе эукариотической микрофлоры, ассоциированной с пищеварительной системой керчаковых рыб оз. Байкал, зарегистрированы представители Diplomonadida, Coccidia и Microsporidia [1]. Использованные в работе праймеры позволяют амплифицировать фрагменты гена малой субъединицы рРНК всех эукариотических организмов. При этом разница в длине полученных ампликонов обеспечивает разделение фрагментов ДНК организма хозяина и кормовых объектов (около 1100 п.н.), дипломонад (около 880 п.н.) и микроспоридий (около 800 п.н.) в процессе электрофореза. В трех из проанализированных в работе образцов выявлены последовательности микроспоридий, других протистов не обнаружено. Ближайшими родственниками обнаруженных микроспоридий являются представители семейства Enterocytozoonidae: Enterocytozoon hepatopenaei из гигантской тигровой креветки Penaeus monodon Fabricius, 1798 и из белоногой креветки Penaeus vannamei Boone, 1931 с гомологией 91 %, и Enterospora nucleophila, культивированной из интестинального эпителия дорады Sparus aurata Linnaeus, 1758, с гомологией 88 % (рисунок). При этом в общую кладку с последовательностями Enterocytozoonidae из кишечника желтокрылки попали последовательности Enterocytozoon bieneusi, паразита, вызывающего системные микроспоридиозы у людей с угнетенным иммунитетом. Последовательности других представителей Enterocytozoonidae, инфицирующих рыб (Nucleospora и Paranucleospora) кластеризуются отдельно с поддержкой 100 % (рисунок).
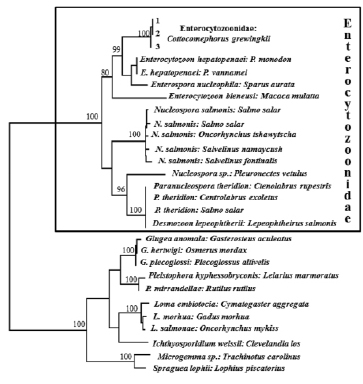
Филогенетическое древо на основании последовательностей фрагмента гена малой субъединицы рРНК длиной 780 п.н. (neighbor-joining), демонстрирующее положение микроспоридии из желтокрылки среди микроспоридий – паразитов рыб
Необходимо отметить, что ранее у рыб оз. Байкал с использованием классических паразитологических методов были отмечены только микроспоридии семейства Glugeidae: Glugea anomala (Moniez, 1887) у горбатой широколобки Cyphocottus megalops (Gratzianov, 1902) (син. Asprocottus megalops (Gratzianov, 1902)) и Glugea fennica Lom et Weiser, 1969 у налима Lota lota (Linnaeus, 1758) [1, 4].
Кроме того, у амурской широколобки Mesocottus haitej (Dybowski, 1869) и амурского подкаменщика Cottus szanaga Dybowski, 1869 описана Glugea mesocotti sp. n. [3]. G. anomala локализована в клетках подкожной и мышечной соединительной ткани, а также мезентерия [4]. В то время как ксеномы G. mesocotti sp. n. локализованы на поверхности тела рыб, на плавниках, в ротовой полости, в почках, стенке кишечника, реже в гонадах и других внутренних органах [3]. Микроспоридий семейства Enterocytozoonidae детектировали в эпителии кишечника, жабр, кожи, во внутренних органах, включая центральную нервную систему; описано размножение E. nucleophila в макрофагах и энтероцитах [10].
Представители Enterocytozoonidae биологически пластичны, способны как к цитоплазматическому, так и к внутриядерному размножению, причем иногда в конкретном организме хозяина показаны оба пути размножения паразита (например, для E. nucleophila). Кроме того, спектр хозяев Enterocytozoonidae чрезвычайно широк: от водных беспозвоночных и позвоночных животных до наземных позвоночных, включая человека (Enterocytozoon bieneusi). Для представителей Enterocytozoonidae (Paranucleospora theridion) описан трофический механизм смены хозяина между паразитическими раками Lepeophtheirus salmonis и рыбами, принадлежащими разным семействам (Centrolabrus exoletus (Linnaeus, 1758), Ctenolabrus rupestris (Linnaeus, 1758), Salmo salar Linnaeus, 1758). Принимая во внимание этот факт, сделано предположение, что способность к смене хозяина в трофической цепи (между беспозвоночными и позвоночными животными) является общей для представителей Enterocytozoonidae [10].
С учетом полученных данных и вероятности передачи микроспоридий в трофических цепях необходимо применение комплекса морфологических, ультраструктурных и молекулярно-генетических методов для дальнейших исследований представителей класса Microsporidea в других видах рыб и беспозвоночных животных озера Байкал и его бассейна.
Работа выполнена в рамках программы РАН: Проект 1.29.7. «Исследование микробиоты эндемичных керчаковых рыб (Сottoidei) озера Байкал».
Библиографическая ссылка
Небесных И.А., Деникина Н.Н., Кондратов И.Г., Ханаев И.В., Смолин И.Н., Белькова Н.Л., Дзюба Е.В. ПЕРВОЕ ОБНАРУЖЕНИЕ ПРЕДСТАВИТЕЛЕЙ ENTEROCYTOZOONIDAE (FUNGI: MICROSPORIDIA) В РЫБАХ ОЗ. БАЙКАЛ // Международный журнал прикладных и фундаментальных исследований. 2017. № 10-1. С. 86-89;URL: https://applied-research.ru/en/article/view?id=11866 (дата обращения: 05.05.2026).
DOI: https://doi.org/10.17513/mjpfi.11866

