Актуальность вопроса
Для профилактики воспалительных осложнений, улучшения результатов и повышения эффективности хирургического лечения больных с обширными дефектами костных и мягкотканных структур челюстно-лицевой области используются различные методы предоперационного планирования. Одним из них является мультиспиральная компьютерная томография, позволяющая построить объёмные реформации, изготовить стереолитографические прототипы реципиентной и донорской зон, хирургические шаблоны и модели [1]. Эта технология стала доступной для повседневного использования и с успехом применяется при планировании оперативного вмешательства у больных с комбинированными, обширными дефектами тканей лицевого и мозгового черепа [2].
Детальное изучение дефекта и выполнение виртуальной реконструкции нижней челюсти любой сложности и протяжённости является основой для изготовления прототипа утраченного фрагмента нижней челюсти, хирургического шаблона, успешного устранения комбинированного дефекта, у больных с сопутствующей патологией, не позволяющей иногда выполнить микрохирургическую пересадку тканей.
Обсуждаемая технология стала незаменимой при проведении биологической подготовки ТДЛ с ребром, формируемого для замещения обширных изъянов нижней челюсти и окружающих мягких тканей [3]. Однако для повышения эффективности планирования этапов реабилитации пациентов с обширными дефектами нижней челюсти и окружающих мягких тканей необходимо учитывать особенности донорской и реципиентной зон. Следует отметить, что биологическая подготовка сложного мягкоткано-костного лоскута проводится зачастую у больных, которым планируется замещение дефекта в условиях рубцово-изменённого инфицированного воспринимающего ложа. Как правило, у таких пациентов ранее проводившиеся операции закончились неудачей [4].
Особенности реципиентной зоны:
- Во всех случаях реконструкции нижней челюсти и окружающих мягких тканей с применением биологически подготовленного ТДЛ с ребром в его составе – это вторичная пластика. В этой связи ткани реципиентной зоны всегда рубцово-изменены, деформированы, имеют нарушения микроциркуляции на фоне комбинированного лечения, включающего лучевую терапию у онкологических больных.
Зачастую после первого этапа – удаления опухоли, фрагменты нижней челюсти остаются не фиксированными и смещаются кверху и медиально. Нередко приходится удалять прорезавшиеся фиксирующие конструкции.
Использование ортопедических конструкций (шина «Ванкевич») для профилактики смещения оставшихся участков нижней челюсти при протяжённых дефектах практически невозможно, ввиду отсутствия точек фиксации в области нижней челюсти.
В этой связи после проведения томографии в первую очередь необходимо выполнить установку фрагментов нижней челюсти в ортотопическое положение на компьютерной модели, являющееся в дальнейшем основой для изготовления прототипа.
- Планирование размеров трансплантата, его формы необходимо проводить с учётом объёма и расположения мягкотканной части лоскута (кожа с подкожно-жировой клетчаткой, мышечный слой).
- При дефиците мягких тканей в реципиентной зоне контуры костной части трансплантата должны быть уменьшены для исключения натяжения мягкотканого компонента лоскута при формировании подбородочного изгиба нижней челюсти.
Сложности формирования ребра в составе ТДЛ, как правило, обусловлены особенностями донорской зоны [5, 6]:
- Костная часть лоскута (X или XI) ребро формируется на заднем межрёберном сосудистом пучке. Костный сегмент характеризуется неправильной формой, изогнутой в 3 плоскостях, что затрудняет моделирование ребра, близкого по форме и размерам к утраченному сегменту нижней челюсти.
- Расположение сосудистого пучка по нижнему краю рёберного лоскута.
- При виртуальном моделировании костной части лоскута (ребра) необходимо учитывать длину межрёберной сосудистой ножки, так как для её удлинения необходимо выполнить поднадкостничное удаление участка ребра.
- Планировать расположение изогнутого рёберного фрагмента на сосудистой ножке в подкожном тоннеле над широчайшей мышцей спины с учетом ротации лоскута при перемещении его в реципиентную зону.
Материалы и методы исследования
За период с 1993 по 2015 г. в клинике челюстно-лицевой хирургии СПбГМУ им. акад. И.П. Павлова были прооперированы 4 женщины и 16 мужчин в возрасте от 25 до 60 лет. В 7 случаях проводилась предоперационная подготовка с использованием мультиспиральной компьютерной томографии, с последующим построением реформаций, изготовлением стереолитографических прототипов реципиентной и донорской зон.
Результаты исследования и их обсуждение
У 4 из 7 пациентов выполнена полная реабилитация, включая зубное протезирование. Применение описанных методик на этапах планирования позволило обеспечить преемственность на всех этапах реабилитации, сократить время вмешательства, уменьшить травматичность операции, улучшить эстетические и функциональные результаты хирургического лечения одной из наиболее сложной группы больных.
Клинический пример:
Пациентка А., 49 лет. Поступила в клинику челюстно-лицевой хирургии с диагнозом: дефект нижней челюсти справа, рубцовая деформация нижней зоны лица справа. Комбинированное лечение рака слизистой оболочки альвеолярной части нижней челюсти справа с метастазами в подчелюстные лимфоузлы (Т3N2M0). У представленного пациента проводилось первичное возмещение послеоперационного дефекта малоберцовым трансплантатом с реваскуляризацией. Однако в результате тромбоза сосудистой ножки произошла гибель перемещённого фрагмента МБК. После заживления раны в данной зоне появилась выраженная деформация с дефицитом мягких тканей. С учётом проводимой лучевой терапии на этапах комбинированного лечения было предложено использование предварительной подготовки ТДЛ с ребром в его составе на сосудистой ножке.
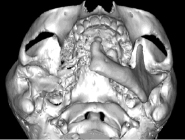
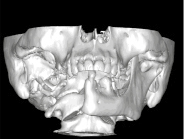
На первом этапе выполнено МСКТ с построением реформации, определено положение оставшихся фрагментов и размер дефекта нижней челюсти. Произведена виртуальная репозиция оставшихся фрагментов челюсти и определены истинные размеры дефекта (рис. 1, а, б).
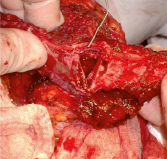
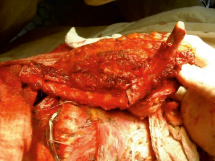
Для замещения изъяна поднято XI ребро в составе ТДЛ с включением в лоскут участка m. Serratus anterior для улучшения кровоснабжения рёберного фрагмента, при этом сосудистая ножка ТДЛ не выделялась. Выделение XI ребра выполнено без повреждения париетальной плевры. Образовавшийся дефект перекрыт полипропиленовой сеткой для предотвращения образования послеоперационных грыж. Произведено моделирование рёберного фрагмента без нарушения его связи с мышечной частью лоскута и сохранением а. et v. Intercostales, согласно форме и размеру дефекта, осуществлена фиксация минипластинами (рис. 2, а, б).
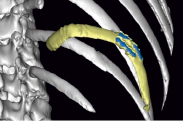
Ребро в составе ТДЛ, смоделированное по форме утраченного сегмента нижней челюсти, оставлено в донорской зоне до момента консолидации фрагментов (преламинация). Такой подход обеспечил перестройку кровоснабжения костной части лоскута за счёт перфорантных сосудов из бассейна а. thoracodorsalis и отсутствие рисков инфицирования. После консолидации фрагментов ребра в местах его изгибов выполнено МСКТ донорской и реципиентной ран с построением реформаций и изготовлением стереолитографических моделей донорской и реципиентной зон, хирургических шаблонов. После чего проводилась виртуальная операция – расположения костной части лоскута в зоне дефекта (рис. 3, а, б).
а б
Рис. 1. Оставшиеся фрагменты нижней челюсти а) до виртуальной репозиции, б) после виртуальной репозиции
а б
Рис. 2. а) Остеотомия ребра в составе ТДЛ, б) Формирование изгибов нижней челюсти

а б
Рис. 3. а) Реформация изображения донорской зоны, б) Расположение хирургического шаблона на модели
После проведения виртуального планирования проводился хирургический этап переноса ТДЛ с предварительно подготовленным ребром в его составе на сосудистой ножке a. et v. thoracodorsalis в реципиентную зону. Для этого в подмышечной ямке выделялась сосудистая ножка будущего лоскута (a. et v. Thoracodorsales). Далее проводилось выделение мышечной части лоскута, с включением в ТДЛ островка кожи и консолидированного ребра (рис. 4).
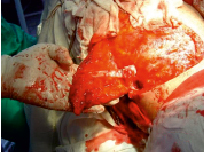
Рис. 4. ТДЛ с подготовленным ребром поднят на сосудистой ножке
Сформированный лоскут на сосудистой ножке проведён под большой грудной мышцей в реципиентную область, после чего пересечён n. Thoracodorsales, сохранено сухожильное прикрепление m. Latissimus dorsi к плечевой кости, что предохраняет сосудистый пучок лоскута от перерастяжения.
Рёберный фрагмент фиксировался согласно моделям. Правильное позиционирование костного фрагмента и возмещение дефицита слизистой оболочки с помощью кожной части лоскута позволяет создать условия для проведения альвеолопластики, дентальной имплантации и протезирования зубов. Пластика альвеолярной части нижней челюсти проведена с использованием свободного аутотрансплантата из гребня подвздошной кости с последующей дентальной имплантацией. Для создания прикреплённой десны в зоне реконструкции альвеолярной части нижней челюсти перед началом изготовления протезов с опорой на имплантаты выполнена вестибулопластика полнослойным кожным аутотрансплантатом с передней брюшной стенки. Свободный кожный трансплантат фиксировался к костной ткани с использованием защитной пластинки, выполненной из быстротвердеющей пластмассы, по моделям, изготовленным на основе оттисков, сделанных интраоперационно. Формирующая пластинка фиксировалась в полости рта за счёт интегрированных дентальных имплантатов. Для протезирования зубов пациенту выполнена ортопедическая конструкция, представленная съёмным протезом, опирающимся на балку, фиксированную к зубным имплантатам (рис. 5, а, б).
Применение методов 3D моделирования позволило выполнить реконструкцию нижней челюсти в условиях дефицита мягких тканей и обеспечить возможность зубного протезирования с опорой на дентальные имплантаты.
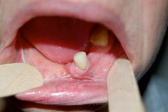
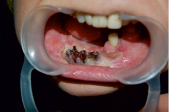
а б
Рис 5. а) Вид протезного ложа после приживления лоскута, б) Балочная конструкция на дентальных имплантатах для фиксации съёмного протеза

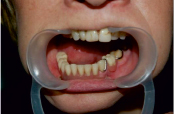
а б
Рис 6. а) Внешний вид больной через 1 год после реконструкции, б) Вид протезов в полости рта с фиксацией на имплантатах
Заключение
- Биологическая подготовка ребра в составе ТДЛ исключает потерю реберного сегмента, так как последний всегда надёжно изолирован от ротовой полости, а его консолидированные фрагменты облегчают хорошую стабилизацию в области культей нижней челюсти.
- Использование метода биологической подготовки ТДЛ с ребром в его составе позволяет надёжно замещать обширные изъяны нижней челюсти и окружающих мягких тканей в случаях, когда проведение микрохирургических пересадок невозможно.
- Уменьшается время и травматичность операции за счёт разделения её на этапы.
- Применение современных технологий, с учётом особенностей донорской и реципиентной зон на этапах планирования, создает благоприятные условия для проведения комплексной реабилитации пациентов, включающей зубное протезирование и восстановление функции жевания.

