Scientific journal
International Journal of Applied and fundamental research
ISSN 1996-3955
ИФ РИНЦ = 0,556
EXTRACTION OF IRIDIUM FROM CHLORIDE SOLUTIONS WITH A MIXTURE OF TRIBUTYL PHOSPHATE AND HYPOCHLOROUS ACID
В настоящее время для вскрытия платиносодержащего сырья в основном используется процесс гидрохлорирования, в результате которого металлы платиновой группы (МПГ) переходят в раствор в виде комплексных хлоридов. В процессе аффинажа МПГ, как правило, получают отдельно платино-палладиевый концентрат и концентрат, содержащий иридий, родий и рутений. На стадиях разделения МПГ нередко возникают проблемы с выделением иридия из-за чрезвычайной инертности его соединений. Применяемые схемы многостадийны, получение целевого продукта иридия происходит на последних стадиях, что приводит к значительным потерям металла с вторичными растворами [1]. Изучены способы разделения Ir (IV), Rh (III) и Ru (III) из растворов хлористоводородной кислоты N-содержащими экстрагентами: n-октиланилином [2], Alamine336 в присутствии SnCl2 и смесями Alamine336 – ТБФ [3].
Для решения задач селективной экстракции Ir (III, IV) из хлоридных растворов и разделения металлов платиновой группы исследованы различные фосфиноксиды, Cyanex 921 и Cyanex 923 с добавлением ТБФ в качестве модификатора. Широкий спектр исследований в этом направлении обусловлен, как разнообразием проблем, возникающих при переработке различного сырья МПГ, так и недостаточной эффективностью известных технологических решений.
В работе [4] была установлена возможность селективного извлечения иридия трибутилфосфатом в виде комплексной кислоты иридия (IV) – Н[IrCl5•H2O]. Вместе с тем при получении хлоридов иридия (IV) доля этой формы комплексов оказывается небольшой. Так, по данным эстракционно-хроматографических исследований, при СHCl = 8,0 M содержание экстрагируемого соединения [IrCl5•H2O]- составляет лишь 0,2 % от общего количества иридия и возрастает до 8,6 % при СHCl = 0,1 M. Для повышения доли экстрагируемых форм иридия авторы предложили проводить экстракцию из смешанных солянокислых-сернокислых растворов [4, 5].
В настоящей работе исследована экстракция хлорокомплексов иридия трибутилфосфатом в присутствии окислителя, способного значительно увеличить долю хорошо экстрагируемой комплексной кислоты Н[IrCl5•H2O]. Это достигается гетерогенным окислением иридия в хлоридных растворах соединением хлорноватистой кислоты с трибутилфосфатом (ТБФ•HOCl) с одновременной экстракцией иридиевого продукта окисления в органическую фазу.
Материалы и методы исследования
В качестве исходных соединений металлов платиновой группы использовали: хлорокомплексные кислоты H3IrCl6, H2IrCl6, H2PdCl4, H2PtCl6 и соли RhCl3, K2[RuCl5·H2O].
С целью уменьшения содержания хлора, солянокислый раствор комплексных кислот МПГ c расчетным содержанием металла упаривали и разбавляли 0,1 М раствором азотной кислоты до прежнего объема. На этой стадии содержание соляной кислоты снижалось с 1 М до ~0,02 М.
«Окислительную» экстракцию иридия проводили контактированием водных растворов хлорида иридия с раствором HOCl в 80 % трибутилфосфате при равных объемах водной и органической фаз (О:В = 1:1).
Гетерогенный окислитель ТБФ•HOCl получали продувкой хлора через эмульсию трибутилфосфата в водном растворе гидроксида натрия по реакции (1). Процесс протекает с хорошими выходами, если количество хлора несколько превышает количество гидроксида натрия от стехиометрии реакции (1). При этом без больших осложнений в органической фазе может быть достигнута концентрация хлорноватистой кислоты 1–1,5 моль/л. Получаемое соединение достаточно устойчиво и не разрушается при промывке водой. Величина коэффициентов распределения HOCl для 80 % ТБФ составляет около 33–35.
Cl2 + NaOH(в) + ТБФ(o) > ТБФ•HOCl (o) + NaCl(в), (1)
здесь и далее символы (в) и (о) обозначают принадлежность компонента к водной или органической фазам, соответственно.
Концентрации металлов в исходных растворах и в водных фазах после экстракции определяли фотоколориметрическим и атомно-адсорбционным методами. Содержание металлов в органических фазах рассчитывали по разности между концентрациями в исходных растворах и в водных фазах после экстракции.
Электронные спектры поглощения (ЭСП) записывали на регистрирующем спектрометре AvaSpec-2048L.
Результаты исследования и их обсуждение
Окислительно-восстановительные свойства системы «водный раствор – трибутилфосфат – хлорноватистая кислота» исследованы нами в работе [6]. Было установлено, что аддукт ТБФ•HOCl достаточно устойчив и является сильным окислителем. При контактировании этого окислителя с водными растворами кислот окислительный потенциал гетерогенной системы возрастает с увеличением кислотности, достигая значений 1,5–1,53 В для нулевого значения рН раствора. Соответственно, для подкисленных растворов хлоридов иридия (III) в системе будут протекать два основных процесса, это окисление примесей соляной кислоты по реакции (2) и окисление иридия до степени окисления (+4).
H+(в) + Cl-(в) + ТБФ•HOCl(o) >
> ТБФ •Cl2(o) + H2O (2)
Контактирование смесей соляной и азотной, а также соляной и серной кислот с исследуемым экстрагентом показывает, что в избытке HOCl за 10–15 минут 98–99 % соляной кислоты разлагается с выделением хлора. Получаемый по реакции (2) аддукт ТБФ •Cl2 нестоек [6] и разлагается далее с выделением газообразного хлора.
Исходная комплексная кислота иридия (III) – H3IrCl6 слабо экстрагируется трибутилфосфатом. Однако после смешивания ее водного раствора с HOCl в ТБФ наблюдается значительное извлечение иридия в органическую фазу, достигающее в некоторых случаях 90 %. На рис. 1 приведена зависимость величины коэффициентов распределения иридия от исходной концентрации HOCl в органической фазе. В этом эксперименте использовали водный раствор Н3IrCl6 в разбавленной азотной кислоте. Его готовили упаркой солянокислого раствора хлоридного комплекса иридия (для удаления избытка HCl) и последующим разбавлением в 0,1 М азотной кислоты. Как видно из полученных данных, зависимость имеет S-образный характер. На начальном участке иридий экстрагируется слабо. Однако при добавлении в органическую фазу более 0,01 М HOCl наблюдается значительный рост извлечения иридия с достижением коэффициентов распределения до величин 2–2,5. Низкие коэффициенты распределения иридия при добавлении небольших количеств HOCl, очевидно, обусловлены окислением остатков HCl в водном растворе. После удаления хлорид-иона из раствора в системе начинает образовываться хорошо экстрагируемая форма иридия, что обусловливает значительный рост коэффициентов распределения металла. Такой формой не может быть продукт окисления иридия – H2IrCl6, который, так же как и H3IrCl6, слабо экстрагируется трибутилфосфатом.
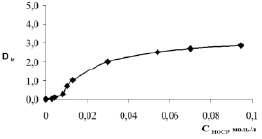
Рис. 1. Влияние концентрации HOCl на извлечение иридия в системе ТБФ-HOCl СIr = 0,008М
Анализ электронных спектров поглощения органической и водной фаз показал, что при гетерогенном окислении иридия HOCl в системе образуется значительное количество моногидратного хлоридного комплекса иридия (IV) – H[IrCl5H2O], который и обеспечивает хорошее извлечение иридия в органическую фазу. Электронные спектры поглощения (ЭСП) исходного водного раствора, иридиевого экстракта для системы HOCl-ТБФ и для сравнения – экстракта для ТБФ без HOCl приведены на рис. 2. Как видно из приведенных данных, при экстракции хлоридных комплексов иридия (III) трибутилфосфатом без окислителя в ЭСП экстракта (рис. 1, спектр 2) регистрируются полосы с λmax = 420 нм, подтверждающие извлечение комплексного аниона [IrCl6]3-. ЭСП экстрагируемых комплексов иридия, полученные при экстракции ТБФ•HOCl (рис. 1 спектр 3), характеризуются двумя полосами поглощения с λmax = 450 нм и λmax = 360 нм, что позволяет говорить об образовании и извлечении в органическую фазу комплексной кислоты H[IrCl5•H2O], которая, как уже упоминалось выше, хорошо извлекается трибутилфосфатом.
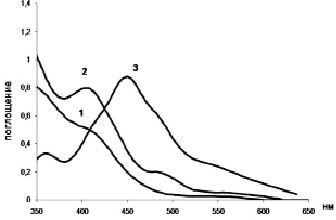
Рис. 2. ЭСП водного исходного раствора комплексной кислоты Н3IrCl6 (1) и органических фаз после экстракции иридия (III) раствором ТБФ (2), ТБФ•HOCl (3) в гептане
При экстракции иридия смесями ТБФ•HOCl наряду с хорошо экстрагируемыми соединениями H[IrCl5•H2O] образуются слабо экстрагируемые комплексы H2[IrCl6], которые в основном остаются в водном растворе. На рис. 3, а, приведен ЭСП органической фазы после экстракции в такой системе, а на рис. 3, б, – ЭСП водной фазы. Спектры водной и органической фаз значительно отличаются друг от друга и отвечают комплексным кислотам, соответственно H[IrCl5•H2O] для экстракта и H2[IrCl6] – для рафината. Доли экстрагируемой и плохо экстрагируемой форм заметно изменяются в зависимости от условий эксперимента.
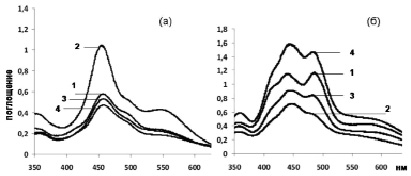
Рис. 3. ЭСП органических (а) и водных фаз (б) после экстракции иридия в системе ТБФ-HOCl. Условия: рН равн = 0,3 (1–1); 0,55 (2–2); 1,07 (3–3); 1,36 (4–4); τэкстракции = 10 мин
В целом полученные предварительные данные показали, что при гетерогенном взаимодействии растворов хлоридных комплексов иридия (III) с хлорноватистой кислотой в ТБФ может со значительным выходом образовываться хорошо экстрагируемая ТБФ комплексная кислота H[IrCl5•H2O] по общей реакции (3).
3H+(в)+IrCl63-(в)+2ТБФ•HOCl(o)>
> 2ТБФ•H[IrCl5H2O] (о)+1,5Cl2^+ H2O. (3)
Очевидно, что процесс протекает по более сложной схеме с окислением иридия в водной или органической фазах, учитывая обратимость межфазных процессов распределения всех участников реакции. Одной из главных задач, решение которой позволило бы оптимизировать процесс и обеспечить условия максимального извлечения иридия и отделения его от других металлов платиновой группы, является понимание механизма образования моногидрата хлоридного комплекса иридия (IV) – H[IrCl5H2O], с заменой одного аниона хлорид-иона на молекулу воды.
Для этого процесса можно выделить два основных маршрута его реализации. Первый – заключается в окислении иридия до четырехвалентного состояния на начальной стадии хлорноватистой кислотой (4) или хлором (5), также присутствующим в системе, с последующим окислением хлорид-иона внутренней координационной сферы комплекса и образованием моногидрата (6).
H+ + IrCl63- + HOCl > IrCl62- + 1/2Cl2 + H2O, (4)
IrCl63- + 1/2Cl2 > IrCl62- + Cl- + H2O, (5)
H+ + IrCl62-+ HOCl > [IrCl5H2O]- + Cl2. (6)
Во втором варианте сначала образуется моногидратный комплекс иридия (III) по реакции (7), который затем окисляется хлорноватистой кислотой (8). Избыток хлорид-иона удаляется из раствора также окислением HOCl (9).
IrCl63- + H2O > [IrCl5H2O]2- + Cl-, (7)
Н+ + [IrCl5H2O]2- + HOCl >
[IrCl5H2O]- + 1/2Cl2 + H2O, (8)
H+ + Cl- +HOCl > H2O + Cl2. (9)
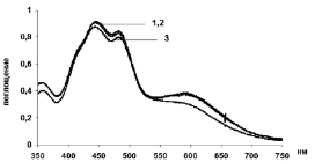
При оценке возможности протекания процесса по первому варианту учитывали, что реакции окисления хлоридов иридия (III) протекают достаточно легко. Лимитирующей стадией в этом случае может являться замещение хлорид-иона водой (6) в инертном комплексе иридия (IV). С учетом этого водные растворы, содержащие IrCl62-, контактировали в течение различного времени с хлорноватистой кислотой в ТБФ (рис. 4). Из полученных данных видно, что окислительная обработка гексахлоридных комплексов иридия (IV) органическим раствором ТБФ•HOCl в течение 10 мин и 60 мин не приводит к заметному уменьшению содержания IrCl62- и образованию моногидратов [IrCl5H2O]-.
Рис. 4. ЭСП водных фаз после контактирования растворов IrCl62- с 0,04 моль/л раствором HOCl в 80 % ТБФ: время контакта фаз, мин: 10 (1), 30 (2), 60 (3)
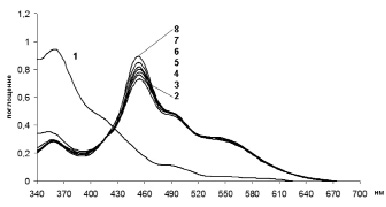
Низкая скорость реакции может быть обусловлена гетерофазным характером реакции и невысокими концентрациями реагирующих компонентов – с одной стороны, HOCl в водной фазе, а с другой – иридия в органической. В этой связи реакцию реализовали в одной – органической фазе при высоких содержаниях как иридия, так и HOCl. Для повышения концентрации Н2IrCl6 в органической фазе необходимое количество гидратированной твердой кислоты H2IrCl6 растворяли в 80 % ТБФ, затем к полученному раствору добавляли избыток HOCl в ТБФ и следили за изменением ЭСП комплексов во времени. Однако, как и для водной фазы, в спектрах комплексов H2IrCl6 в органических растворах не наблюдалось в течение 1 часа заметных изменений.
Аналогичный эксперимент с комплексной кислотой иридия (III) – Н3IrCl6, показывает (рис. 5), что окисление этого соединения в органической фазе приводит к быстрому образованию моногидратной формы Н[IrCl5H2O].
Рис. 5. Изменения ЭСП органической фазы при окислении комплексов H3IrCl6 хлорноватистой кислотой: 1 – 80 % ТБФ в гептане, СH3IrCl6(исх) = 0,0017 моль/л; 2 – 80 % ТБФ в гептане, СH3IrCl6(исх) = 0,0017 моль/л СHOCl(исх) = 0,015 моль/л через 5 мин после добавления; 3–8 – условия системы (2) с последующими временными интервалами 10 мин
Таблица 1
Извлечение металлов платиновой группы (МПГ) раствором хлорноватистой кислоты в 80 % ТБФ (п. 1) и 80 % раствором ТБФ (п. 2)
|
№ п/п |
Экстрагент |
% извлечения МПГ |
||||
|
Ru |
Rh |
Pd |
Ir |
Pt |
||
|
1 |
0,11 М раствор хлорноватистой кислоты в 80 % трибутилфосфате (разбавитель гептан) |
<5 |
<5 |
10 |
90 |
<5 |
|
2 |
80 % трибутилфосфат (разбавитель гептан) |
<5 |
<5 |
8 |
<5 |
<5 |
Таблица 2
Коэффициенты разделения иридий/МПГ при обработке водных растворов хлоридов МПГ раствором хлорноватистой кислоты в 80 % ТБФ (п. 1) и 80 % раствором ТБФ (п. 2) (разбавитель гептан)
|
№ п/п |
Экстрагент |
Коэффициенты разделения иридий/МПГ (DIr/DМПГ) |
|||
|
Ir/Ru |
Ir/Rh |
Ir/Pd |
`Ir/Pt |
||
|
1 |
0,11 М раствор хлорноватистой кислоты в 80 % трибутилфосфате |
>170 |
>170 |
82 |
>170 |
|
2 |
80 % трибутилфосфат |
~1 |
~1 |
<0,5 |
~1 |
При добавлении к раствору иридия HOCl интенсивность пиков ЭСП комплекса H3IrCl6 снижается почти на порядок в первые минуты (рис. 5). При этом одновременно появляются пики поглощения комплекса Н[IrCl5H2O]. Основные изменения в системе наблюдаются в течение первых минут и далее в течение 60–80 мин доля комплекса Н[IrCl5H2O] возрастает еще приблизительно на 10 %.
Таким образом, выполненные эксперименты показывают, что в исследуемой системе хорошо экстрагируемый комплекс Н[IrCl5H2O] образуется в результате протекания процесса по второму варианту, когда на первой стадии образуется моногидрат иридия (III), а затем происходит окисление металла. Окисление иридия в начале процесса приводит к образованию кинетически устойчивой формы H2IrCl6, что снижает глубину извлечения иридия в органическую фазу.
Исследуемая система представляет значительный практический интерес для решения проблем выделения иридия из технологических растворов и его очистки, так как другие металлы платиновой группы (Pt, Pd, Rh, Ru) экстрагируются ТБФ в присутствии хлорноватистой кислоты слабо и их основная часть остается в водном растворе при экстракции [7].
В табл. 1 представлены результаты некоторых исследований экстракции иридия, платины, палладия, родия и рутения растворами хлорноватистой кислоты в 80 % трибутилфосфате и для сравнения 80 % трибутилфосфатом (растворитель – гептан) без окислителя. При использовании ТБФ•HOCl извлечение иридия за 1 контакт составляет 90 % (коэффициент распределения – 9). Для других МПГ извлечение не превышает 5 % (коэффициент распределения менее 0,05), за исключением палладия, извлечение которого составляет 10 % (коэффициент распределения – 0,25).
Коэффициенты разделения для пар Ir/МПГ (βIr/МПГ) приведены в табл. 2. Можно видеть, что селективность извлечения иридия очень высока и величины βIr/МПГ составляют от 80 до более чем 170.
Реэкстракция иридия из органической фазы достигается обработкой экстрактов водой. За 1 контакт извлечение иридия в водную фазу составляет около 80 % при отношении О:В=1:1.
Учитывая практическую важность данной системы, значительный интерес представляет ее дальнейшее исследование, выявление особенностей механизма процесса, установлению влияния различных факторов на извлечение иридия.
Заключение
Изучена гетерофазная реакция хлоридных комплексов иридия (III) с органическим раствором хлорноватистой кислоты в трибутилфосфате. Показано, что при межфазном взаимодействии с большим выходом образуется моногидрат хлоридного комплекса иридия (IV) – Н[IrCl5H2O], который извлекается в органическую фазу с достаточно высокими коэффициентами распределения и разделения относительно других металлов платиновой группы. В процессе экстракции одновременно из раствора удаляется избыток хлорид-иона в виде молекулярного хлора. Анализ электронных спектров поглощения растворов и данных межфазного распределения иридия позволяет заключить, что основным маршрутом гетерофазного процесса является замещение хлорид-иона на молекулу воды на первой стадии процесса и последующее окисление иридия до четырехвалентного состояния на завершающей. Это обеспечивает образование хорошо экстрагируемого трибутилфосфатом иридиевого комплекса.
Библиографическая ссылка
Кузьмин В.И., Жидкова Т.И., Кузьмин Д.В. ЭКСТРАКЦИОННОЕ ИЗВЛЕЧЕНИЕ ИРИДИЯ ИЗ ХЛОРИДНЫХ РАСТВОРОВ СМЕСЬЮ ТРИБУТИЛФОСФАТА И ХЛОРНОВАТИСТОЙ КИСЛОТЫ // Международный журнал прикладных и фундаментальных исследований. 2018. № 3. С. 37-43;URL: https://applied-research.ru/en/article/view?id=12145 (дата обращения: 31.05.2026).
DOI: https://doi.org/10.17513/mjpfi.12145

