Scientific journal
International Journal of Applied and fundamental research
ISSN 1996-3955
ИФ РИНЦ = 0,556
DIFFICULTIES OF CLINICO-SONOGRAPHIC DIFFERENTIAL DIAGNOSTICS OF ABDOMINAL ENDOMETRIOSIS AND DESMOID
Проблема диагностики и лечения экстрагенитального эндометриоза и десмоида передней брюшной стенки продолжает привлекать повышенное внимание онкологов, гинекологов и врачей ультразвуковой диагностики [1, 2].
Экстрагенитальный эндометриоз передней брюшной стенки является редким опухолеподобным поражением. Он развивается в результате имплантации кусочков эндометрия в края операционной раны во время акушерско-гинекологических операций, связанных со вскрытием полости матки [3, 4]. Всего на долю экстрагенитального эндометриоза приходится 6–8 % от всех гинекологических заболеваний и 0,03–1 % в общей структуре заболеваемости [4]. Чаще он возникает у женщин репродуктивного возраста от 25 до 45 лет. Клинические симптомы зависят от локализации заболевания, но практически всегда прослеживается связь с менструальным циклом женщины [5, 6].
Десмоидные опухоли являются редкими мускулоапоневротическими опухолями мезенхимального происхождения, возникающими в результате пролиферации хорошо дифференцированных фибробластов. На долю десмоидов приходится 0,03 % всех новообразований и 3,5 % всех опухолей мягких тканей, чаще поражают молодых женщин в возрасте от 20 до 40 лет [7]. Принята теория их травматического происхождения на почве надрывов мышц и соединительнотканных элементов. Кроме того, отмечается связь его возникновения с беременностью и последующими родами, приемом оральных контрацептивов, гиперэстрогенией [3].
Золотым стандартом для диагностики опухолей и опухолеподобных заболеваний мягких тканей передней брюшной стенки является УЗИ. Вместе с тем еще не полностью изучены его возможности в дифференциальной диагностике описываемых заболеваний, в связи с отсутствием разработанных систематизированных сонографических критериев [1]. Процент диагностических ошибок остается высоким и достигает 60–90 % [3]. Все вышеперечисленное позволяет считать проведенное исследование актуальным.
Цель исследования: провести детальный сравнительный анализ приведенных нами клинических случаев с данными литературы для выявления достоверных клинико-эхографических критериев в дифференциальной диагностике эндометриоза и десмоида передней брюшной стенки.
Материалы и методы исследования
В период с мая 2014 г. по сентябрь 2017 г. под нашим наблюдением находились три женщины фертильного возраста 23, 30 и 38 лет. Две из них получили стационарное лечение по поводу эндометриоза и одна по поводу десмоида мягких тканей передней брюшной стенки. Всем было проведено комплексное обследование, включающее сбор анамнестических данных, гинекологическое обследование, клинико-лабораторное обследование, УЗИ и МРТ объемных новообразований передней брюшной стенки, ТАПБ опухолей под ультразвуковым контролем, оперативные вмешательства в объеме иссечения в пределах здоровой ткани с последующим гистоморфологическим исследованием. Комплексная сонографическая визуализация выполнена на ультразвуковом сканере GE Logic P6 (США) с использованием стандартных методик. В зонах интереса мягких тканей проводили доплерографию сосудов с исследованием скорости кровотока и анализом доплеровского спектра эхосигналов.
Результаты исследования и их обсуждение
Общая симптоматология экстрагенитального эндометриоза и десмоидной фибромы мягких тканей передней брюшной стенки включали в себя наличие болезненного опухолеподобного образования, прогрессивный автономный рост, способность инфильтрировать окружающие мягкие ткани, а также схожие клинико-анамнестические признаки, такие как прием оральных контрацептивов и оперативное родоразрешение. Общими сонографическими признаками являются неправильная форма, неровные контуры, солидная неоднородная структура. В режиме доплеровского сканирования во всех наблюдениях отмечалось наличие интранодулярных сосудов. Приводим клинические случаи.
Эпизод 1. Пациент Б., 30 лет, обратилась с жалобами на болезненные и обильные менструации (дисменорея, гиперполименорея), болезненные половые контакты (диспареуния), припухлость и асимметрию мягких тканей слева от пупка, наличие болей тупого характера, усиливающихся во время менструации и спадающих после. На основании локального статуса, данных УЗИ, гистероскопии, выскабливания полости матки установлен клинический диагноз – аденомиоз матки. Акушерско-гинекологический анамнез: регулярные и болезненные менструации начались с 15 лет, продолжительностью по 7 дней, регулярная половая жизнь – с 19 лет. Три беременности, из них 2 родов в 2008 и 2011 гг. через кесарево сечение, а также 1 медицинский аборт. В 2014 г. при УЗИ передней брюшной стенки в мягких тканях мезогастрия слева от пупка, в толще прямой мышцы живота, было обнаружено солидное объемное образование, на сосудистой артериальной ножке, толщиной до 16 мм, с четкими неровными контурами, размером до 37,7х13,0х29,5мм (рис. 1).
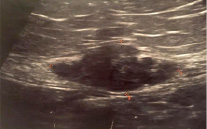
Рис. 1. Эхографическая картина до начала лечения
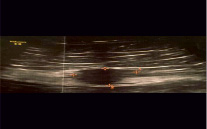
Рис. 2. Эхографическая картина спустя 6 месяцев от начала лечения
С учетом вышеизложенного была назначена гормонотерапия диферелином 11,25 мг каждые три месяца. На фоне проводимого лечения при УЗИ отмечалась положительная динамика, в виде уменьшения размеров объемного образования на 62 % (рис. 2).
Однако, через год, ссылаясь на соматический дискомфорт, больная отказалась продолжать гормональное лечение. Вышеописанные жалобы вновь появились в сентябре 2017 г., в связи с чем была проведена операция в объеме иссечения опухоли в пределах здоровой ткани. Макропрепарат: на фоне поперечно-полосатых мышечных волокон обнаружено образование без четких контуров и границ, размерами 37,0х41,2 мм, плотной консистенции. На разрезе оно серо-розового цвета, с очагами кровоизлияний. Гистологическое заключение: эндометриоз прямой мышцы передней брюшной стенки (рис. 3).
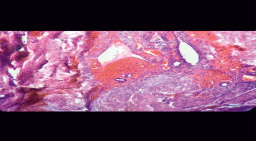
Рис. 3. Эндометриоз прямой мышцы передней брюшной стенки. Окраска гемотоксилином и эозином, х100
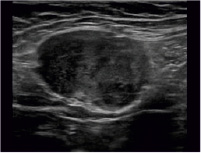
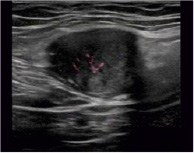
Рис. 4. Эхографическая картина описанного объемного образования
Эпизод 2. Пациент Ж., 23 года, в 2016 г. обратилась с жалобами на наличие болезненного образования в мягких тканях справа от пупка. Из анамнеза одни роды через кесарево сечение в 2013 г. Гинекологический статус без особенностей. Последние полтора года принимает оральные контрацептивы. При УЗИ мягких тканей передней брюшной стенки справа от пупка, в толще подкожно-жировой клетчатки, фасции и в толще прямой мышцы, обнаружено фиксированное гипоэхогенное солидное объемное образование, болезненное при компрессии датчиком, с четкими неровными контурами и интранодулярным кровотоком, размером 34,6 х 45,0 мм (рис. 4).
При повторных сонографических исследованиях в динамике отмечена тенденция к росту опухолевидного образования до 50,4х45,8 мм в поперечнике, без УЗ-признаков инвазии в подлежащие ткани. В клинической картине отмечалось увеличение интенсивности болей, которые имели место и в период менструального цикла. Была проведена чрескожная аспирационная пункционная биопсия. Цитологические данные за скопление зрелых фиброцитов и клеток, подобных фибробластам, что может соответствовать десмоиду мягких тканей. Проведена колоноскопия до уровня купола слепой кишки. Патологических изменений исследованных отделов толстой кишки не выявлено.
Больной был проведен курс терапии золадексом, но без видимого эффекта, в связи с чем была произведена операция в объеме иссечения солидного объемного образования с резекцией передней брюшной стенки.
Гистологическое заключение: десмоид с инфильтрацией прямой мышцы живота и жировой клетчатки (рис. 5). В течение девяти месяцев после операции данных за рецидив заболевания не выявлено, пациентка остается под клиническим наблюдением.
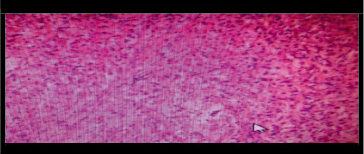
Рис. 5. Окраска гемотоксилином и эозином, х100
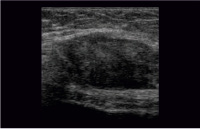
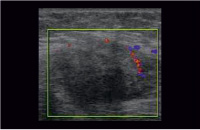
Рис. 6. Эхографическая картина описываемого объемного образования
Эпизод 3. Пациентка К., 38 лет, обратилась с жалобами на боль в области пальпируемого уплотнения в области передней брюшной стенки. При физикальном обследовании по переднелатеральному контуру прямой мышцы живота обнаружена опухоль около 3 см в поперечнике. Имеется также отягощенный акушерский анамнез – две операции кесарева сечения в 2006 и 2012 гг. Нарушения менструального цикла не отмечает, жалоб по гинекологическому профилю не предъявляет. При колоноскопии патологических изменений не выявлено. По данным УЗИ в мягких тканях гипогастрия слева, в толще прямой и косых мышц, определяется солидное объемное образование низкой акустической плотности, гетерогенной структуры, размером до 27,8х30,5 мм в поперечнике. В режиме доплеровского картирования определяется интра- и перинодулярная артериальная перфузия.
По данным МРТ в мягких тканях брюшной стенки слева, на 6–7 см выше лобка и латерально от послеоперационного шва, определялось гетерогенное солидное образование 3,0х2,5 см с поражением прямой и косых боковых мышечных пучков и фасций. Контуры образования нечеткие, местами «лучистые» за счет перифокальной инфильтрации. Отмечается повышение интенсивности МР-сигнала в T1W режиме сканирования и умеренно выраженное утолщение веретеновидных мышц прямой мышцы живота вокруг поражения. Заключение: неоплазма мягких тканей передней брюшной стенки, не исключается малигнизация. Больной была выполнена эксцизионная биопсия. Гистологические данные за эндометриоз с перифокальной инфильтрацией мягких тканей.
В приведенных клинических случаях наглядно представлены определенные трудности в дифференцированной клинико-сонографической интерпретации представленных нами форм опухолевых образований. Во всех случаях анализируемые параметры крови находились в пределах нормы, а маркеры опухолей были отрицательными. Клинически выделена триада симптомов, состоящая из акушерской истории кесарева сечения, наличия опухолеподобных узлов вблизи хирургического рубца и цикличности болей. По многочисленным источникам литературы дифференциально-диагностическими критериями абдоминального эндометриоза является цикличность болей, умеренное увеличение опухолевого узла во второй фазе менструального цикла и нодулярная регрессия при гормонотерапии. Однако в наших наблюдениях мы отметили симптом цикличности при абдоминальном десмоиде, что подкрепляем также данными литературы [2, 8]. Кроме того, в литературе описываются случаи бессимптомного течения эндометриоза передней брюшной стенки, что также приносит затруднения в клинической диагностике [9, 10].
Атипичные презентации как эндометриоза, так и десмоида часто создают большую диагностическую проблему с учетом различных визуальных представлений описанных опухолей мягких тканей, особенно при оценке пациента с перенесенными операциями. Это также совпадает с представленными нами клиническими случаями. Эндометриоидные очаги имеют более разнообразную картину: опухоли могут быть гетерогенно солидной или кистозной структуры, разнородной эхоплотности с достаточно четкими неровными контурами, в некоторых случаях могут иметь хорошо очерченный гиперэхогенный ободок и интранодулярные сосуды, что зачастую придает им неспецифичный и малоинформативный характер. По данным исследований J. Casillas резюмирует об отсутствии конкретных дифференциальных критериев десмоидных опухолей от других солидных масс [11].
Мы провели систематический поиск литературы по вопросам дифференциальной диагностики и лечения эндометриоза и десмоида брюшной стенки. Детальный анализ литературы показал, что установить окончательный клинический диагноз невозможно лишь на основании клинико-инструментальных исследований, поскольку они имитируют друг друга ввиду идентичности факторов риска, клинической манифестации, многоликой эхосемиотики. Патофизиология сложна и противоречива. В литературе описан уникальный случай сосуществования двух нозологий в одной туморозной массе передней брюшной стенки у одного индивидуума, верифицированных гистологически [8].
В лечении по данным литературы отмечено, что уровень успешной медикаментозной терапии низкий, отмечается лишь временное облегчение симптомов, часто сопровождаемое рецидивом после прекращения приема препарата. Кроме того, наблюдается высокий риск развития побочных эффектов, таких как аменорея, увеличение веса, гирсутизм, возникновение угрей [10], что клинически проявлялось и в наших описываемых эпизодах.
Поэтому основным резюмирующим ключом в дифференциальной диагностике является обязательная хирургия с гистологической верификацией [5, 6], которая несет не только подтверждающий характер, но и позволяет выявить ранние признаки риска малигнизации очагов [12]. По немногочисленным источникам в 5–8 % случаев возникновения десмоида наблюдается малигнизация, в результате чего на месте опухоли развивается плоскоклеточный рак, что может проявляться прогрессирующим ростом опухоли [2, 12]. Авторами предложено рассматривать десмоиды как фибросаркомы с низким уровнем злокачественности, несмотря на доброкачественную гистологию и отсутствие метастазирования. Эндометриоз передней брюшной стенки редко малигнизируется в эндометриоид или светлоклеточную карциному [6, 10, 13].
Однако следует помнить, что хирургический метод не всегда приводит к гарантированному излечению, высокий риск развития локальных рецидивов особенно характерен для десмоидных опухолей (от 40 % до 100 %), что требует продолжительного последующего наблюдения [12, 14].
Заключение
Таким образом, выявленные клинико-эхографические признаки абдоминального эндометриоза и десмоида имеют много общего. Относительно редкая встречаемость, а также вариабельность проявлений не позволяет провести достоверную дифференциальную диагностику между ними в допатоморфологический период обследования. Окончательная верификация процесса возможна только после гистологического или имуногистохимического подтверждения с длительным наблюдением ввиду высокого риска рецидивирования.
Библиографическая ссылка
Кадырова А.И., Миненков Г.О., Абдуллаева А.А., Юсупова Д.В. СЛОЖНОСТИ КЛИНИКО-СОНОГРАФИЧЕСКОЙ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ АБДОМИНАЛЬНОГО ЭНДОМЕТРИОЗА И ДЕСМОИДА // Международный журнал прикладных и фундаментальных исследований. 2018. № 7. С. 101-106;URL: https://applied-research.ru/en/article/view?id=12336 (дата обращения: 28.05.2026).
DOI: https://doi.org/10.17513/mjpfi.12336

