Scientific journal
International Journal of Applied and fundamental research
ISSN 1996-3955
ИФ РИНЦ = 0,556
DETERMINATION OF THE CONCENTRATION OF MEDICINAL MIXTURES CONTAINING PROPIFENAZONE, PARACETAMOL, COFFEEIN, BY THE FIRORDER METHOD
Определение количества лекарственного препарата в составе сложных смесей – одна из задач фармацевтического анализа. Актуально это и для фармакологии. Многие лекарства при совместном употреблении дополняют терапевтический эффект друг друга на организм человека. Противовоспалительные нестероидные препараты сочетают с обезболивающими. Лекарственные препараты «Саридон» имеют в своём составе парацетамол (ацетаминофен), пропифеназон и кофеин. Анальгетическое и жаропонижающее действие парацетамола дополняется ненаркотическим анальгетиком – пропифеназоном. Кофеин относится к группе психостимулирующих средств. Повышенное внимание к определению концентраций лекарственных препаратов в смесях связано с тем, что на рынке фармацевтической продукции появляются новые лекарства, среди которых немало некачественных. Данный факт ставит перед исследователями задачу разработки и внедрения простых в применении методов определения концентраций лекарственных препаратов в смесях.
Спектрофотометрический анализ применяют для быстрого и точного определения содержания веществ в широком диапазоне значений концентраций [1]. Определение концентраций веществ в смеси из двух соединений с известными показателями поглощения, при условии наложения полос поглощения (без их разделения) методом Фирордта, используется при анализе лекарственных препаратов [2, 3]. Применение метода возможно только при соблюдении закона Бугера обоих компонентов и выполнении принципа аддитивности их смеси [4], что требует от исследователей более детального изучения применимости метода. В частности, на выполнение принципа аддитивности влияет выбор оптимального набора аналитических длин волн в спектре поглощения смеси. Количественный анализ лекарственных препаратов методом дифференциальной спектрофотометрии использовался нами ранее [5], однако он требовал трудоёмких математических вычислений, проведение которых невозможно без использования компьютерной программы.
Целью данной работы было изучение условий применения метода Фирордта к проведению анализа смесей, разработка простого и точного метода количественного определения компонентов, содержащихся в лекарственных препаратах с помощью ЭВМ.
Материалы и методы исследования
Использовали материалы: анальгин (метамизол натрия), кофеин, парацетамол (ацетаминофен), раствор натрия гидроксида фармакопейного уровня чистоты. Таблетки «Саридон», производство Лаборатории Рош Николас С.А., Гайярд, Франция, дочерней компанией Ф. Хоффманн – Ля Рош Лтд., Швейцария.
Приготовляли растворы: анальгина, кофеина, парацетамола, модельной смеси лекарственной формы таблеток «Саридон», раствор таблеток «Саридон» в 0,01 моль/л растворе натрия гидроксида.
Были сняты спектры поглощения анальгина, кофеина, парацетамола, модельной смеси лекарственной формы таблеток «Саридон» и раствора таблеток «Саридон» в области 220–320 нм в кюветах 1 см на фоне растворителя – 0,01 моль/л раствора натрия гидроксида.
При изучении влияния рН на спектры поглощения препаратов, величину рН контролировали ионометром ЭВ-74.
Метод Фирордта
Основное условие применимости метода – выполнение принципа аддитивности, т.е. оптическая плотность смеси при любой длине волны должна равняться сумме оптических плотностей компонентов, измеренных порознь. Для определения концентраций C1 и C2 необходимо решать систему из двух уравнений, называемую уравнениями Фирордта [1]:
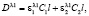
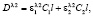 (1)
(1)
где C1 и C2 – концентрации компонентов (в моль/л); 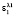 и
и 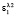 – молярные показатели поглощения (МПП) компонентов смеси при соответствующих длинах волн l1 и l2; l – длина кюветы (в см). Размерность МПП – л/(моль.см), а его численное значение равно оптической плотности монораствора с концентрацией 1 моль/л при длине кюветы 1 см. Для сравнения в нашей работе использовали два метода решения системы уравнений: метод Крамера и метод Гаусса.
– молярные показатели поглощения (МПП) компонентов смеси при соответствующих длинах волн l1 и l2; l – длина кюветы (в см). Размерность МПП – л/(моль.см), а его численное значение равно оптической плотности монораствора с концентрацией 1 моль/л при длине кюветы 1 см. Для сравнения в нашей работе использовали два метода решения системы уравнений: метод Крамера и метод Гаусса.
Метод Крамера
Систему (1) рассматривают как матрицу, где неизвестные переменные находят по универсальной формуле Крамера [6]:
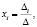 (2)
(2)
где i = 1,2,...,n; ∆ – определитель системы (детерминант матрицы системы),
∆i – дополнительные определители.
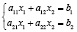
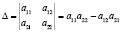 ,
,
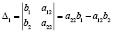 ,
,
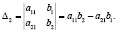 (3)
(3)
Расчёты по формулам (3) удобно проводить с помощью компьютерной программы Excel или в режиме онлайн [7].
Метод Гаусса
Численное решение линейных алгебраических уравнений с помощью определителей успешно применяют для системы, состоящей из двух или трёх уравнений. В случае же большего числа уравнений в системе проще пользоваться методом Гаусса, который заключается в последовательном исключении неизвестных. Алгоритм метода подробно описан в учебниках по высшей математике [6], и его легко записать в виде компьютерной программы. Мы использовали программу, написанную нами в QBASIC.
Результаты исследования и их обсуждение
Было изучено влияние рН на величину оптической плотности парацетамола, анальгина, кофеина в растворе натрия гидроксида. Исследования показали, что в качестве растворителя в области 220–320 нм при получении спектров поглощения, следует выбрать 0,01 моль/л раствор натрия гидроксида.
Не было возможности получить субстанцию пропифеназона, отвечающую требованиям нормативной документации (НД). В анализе использовалась субстанция метамизола натрия (анальгина), отвечающая требованиям НД. Пропифеназон и метамизол натрия по химической структуре соответствуют производным от пирозола. В их спектрах одна полоса поглощения, с максимумом при длине волны 240 нм (для пропифеназона) и 258 нм (для метамизола натрия).
Выбор оптимальных условий количественного анализа, обеспечивающих максимальную воспроизводимость и правильность результатов, зависит от характера спектров поглощения всех компонентов, степени их перекрывания и числа используемых длин волн lанал [4]. При поиске аналитических длин волн АДВ, в качестве простого критерия можно использовать коэффициент rij [1, 3], определяемый по формуле
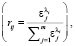 (4)
(4)
где 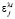 – молярный показатель поглощения (МПП) j-го компонента смеси для соответствующих длинах волн li. В числителе
– молярный показатель поглощения (МПП) j-го компонента смеси для соответствующих длинах волн li. В числителе 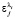 – максимальный МПП j-го компонента при некотором l, m – число длин волн в спектре поглощения данного вещества. Чем выше коэффициент r, тем большую информацию о компоненте j содержит оптическая плотность
– максимальный МПП j-го компонента при некотором l, m – число длин волн в спектре поглощения данного вещества. Чем выше коэффициент r, тем большую информацию о компоненте j содержит оптическая плотность 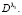 Критерий r не связан с другими длинами волн, которые входят в изучаемый набор.
Критерий r не связан с другими длинами волн, которые входят в изучаемый набор.
На рис. 1 представлены результаты определения оптической плотности растворов веществ, входящих в состав модельной смеси.
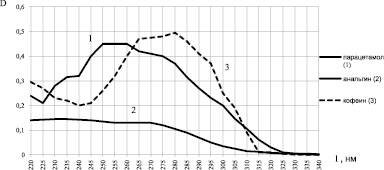
Рис. 1. Спектры поглощения парацетамола, анальгина, кофеина в 0,01 моль/л растворе натрия гидроксида
Концентрации вещества составляли: парацетамола (около 0,01 %), анальгина (около 0,02 %), кофеина (около 0,001 %) в среде 0,01 % раствора гидроксида натрия. Использовали кюветы толщиной 1 см. Из рис. 1 следует, что в выбранном растворителе спектры поглощения парацетамола и анальгина будут перекрываться. Набор АДВ состоял из длин волн, при которых компоненты смеси имеют максимальное поглощение. Максимум поглощения парацетамола соответствует длине волны 250 нм. В спектре анальгина чётко выраженного максимума не наблюдалось. При длине волны 230 нм имели небольшое увеличение оптической плотности. Кофеин имеет ярко выраженный максимум на длине волны 280 нм, поэтому для определения концентрации кофеина в смеси можно применить однокомпонентный спектральный анализ, используя формулу
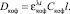 (5)
(5)
Если для вещества неизвестна молярная масса или представлена смесь неизвестного состава, в фармакопейном анализе концентрацию раствора выражают в весе объёмных процентах, а вместо МПП используют (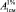 ) – удельный показатель поглощения (УПП). УПП численно равен оптической плотности 1 % раствора при толщине кюветы 1 см. Рассчитанные по спектрам поглощения УПП, на выбранных АДВ, представлены в табл. 1. Жирным шрифтом выделены максимальные значения УПП и информационные коэффициенты каждого монораствора. Коэффициент r вычисляли по формуле (4). Значения
) – удельный показатель поглощения (УПП). УПП численно равен оптической плотности 1 % раствора при толщине кюветы 1 см. Рассчитанные по спектрам поглощения УПП, на выбранных АДВ, представлены в табл. 1. Жирным шрифтом выделены максимальные значения УПП и информационные коэффициенты каждого монораствора. Коэффициент r вычисляли по формуле (4). Значения 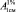 для каждого компонента использовали для расчёта его концентрации в смеси методом Фирордта.
для каждого компонента использовали для расчёта его концентрации в смеси методом Фирордта.
Таблица 1
Аналитические длины волн и удельные показатели поглощения
|
Название лекарственного вещества |
Длина волны, λ (нм) |
|||||
|
250 |
230 |
280 |
||||
|
|
r |
|
r |
|
r |
|
|
Парацетамол (ацетаминофен) |
45 |
0,074 |
28 |
0,046 |
37 |
0,061 |
|
Анальгин (метамизол натрия) |
6,8 |
0,066 |
7,3 |
0,070 |
5,3 |
0,051 |
|
Кофеин |
260 |
0,042 |
230 |
0,038 |
500 |
0,081 |
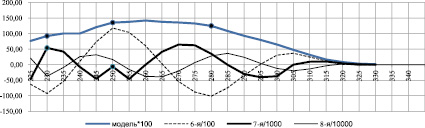
Рис. 2. Спектр поглощения модельной смеси «Саридон» и его производные
Способ нахождения rij по формуле (4)предполагает спектрофотометрический анализ каждого компонента смеси в широком диапазоне длин волн. Мы предлагаем снять спектр поглощения только смеси и методом производной УФ-спектроскопии найти длины волн максимального поглощения для каждого компонента смеси, используя оптимальную производную спектра n-го порядка [5]. Для вычисления производных спектров высокого порядка на основе полиномов Чебышева использовали компьютерную программу POLINOM.BAS. Программа составлена нами для персонального компьютера ПК, работающего в среде Microsoft Windows на программном языке Visual Basik.
Сняли спектр поглощения модельной смеси таблеток «Саридон» в области 220–340 нм. Вычисление производных спектра поглощения показало, что оптимальной производной для данного спектра является производная 7-го порядка (минимальная ошибка производной). В этом случае максимумы кривой производной должны соответствовать максимумам поглощения компонентов модельной смеси – парацетамолу (250 нм), анальгину (230 нм), кофеину (280 нм). Графики спектра поглощения и производных 6, 7, 8-го порядков представлены на рис. 2. Для представления всех производных на одном графике выбрали соответствующий масштаб.
Из анализа графиков следует, что оптимальной производной будет производная 7-го порядка, так как её максимумы соответствуют положению максимального поглощения компонентов смеси.
Методика приготовления стандартного раствора – модельной смеси таблеток «Саридон»
Отвешивали точные навески парацетамола (около 0,25 г), анальгина (около 0,15 г), кофеина (около 0,05 г) и переносили в мерную колбу вместимостью 100 мл. Прибавляли 50 мл 0,01 моль/л раствора гидроксида натрия и полностью растворяли. Затем доводили объём раствора до метки 100 мл тем же растворителем и перемешивали. 1 мл полученного раствора переносили в мерную колбу вместимостью 100 мл, доводили объём до метки.
Определяли оптическую плотность модельной смеси с помощью спектрофотометра при длинах волн 230, 250 нм (для определения концентраций парацетамола и анальгина) и 280 нм – для кофеина. Кюветы толщиной 10 мм. Раствор сравнения – 0,01 моль/л раствор гидроксида натрия. Оптические плотности модельной смеси и рассчитанные значения концентраций компонентов модельной смеси представлены в табл. 2. Концентрации парацетамола и анальгина вычисляли с помощью уравнений Фирордта (1). Для решения уравнений Фирордта применяли метод Крамера (3) и метод Гаусса. При сравнении результатов расчётов обоими методами убедились в их 100 % идентичности.
Таблица 2
Результаты количественного определения парацетамола и анальгина в модельной смеси таблеток «Саридон»
|
Навески препаратов в модельной смеси «Саридон», г |
D250x |
D230x |
Метод Гаусса |
Метод Крамера |
|
|
Xi, г |
Xi, г |
||||
|
Парацетамол |
0,248 |
0,122 |
0,08 |
0, 251 |
0,251 |
|
Анальгин |
0,145 |
0,133 |
0,133 |
||
|
Парацетамол |
0,245 |
0,124 |
0,078 |
0,271 |
0,271 |
|
Анальгин |
0,142 |
0,028 |
0,028 |
||
|
Парацетамол |
0,258 |
0,120 |
0,079 |
0,245 |
0,245 |
|
Анальгин |
0,159 |
0,141 |
0,141 |
||
|
Парацетамол |
0,260 |
0,125 |
0,081 |
0,262 |
0,262 |
|
Анальгин |
0,148 |
0,105 |
0,105 |
||
|
Парацетамол |
0,254 |
0,122 |
0,078 |
0,261 |
0,261 |
|
Анальгин |
0,154 |
0,068 |
0,068 |
||
Среднее значение концентрации парацетамола в модели «Саридон», полученное методом Фирордта (табл. 2): Хпарацетамола = 0,26 ± 0,01 (г). Относительная погрешность вычислений Е = 3,9 %. Исходная концентрация парацетамола в модельной смеси 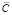 парацетамол = 0,250 ± 0,006 (г). Погрешность определения концентрации парацетамола с учётом погрешности измерений составила 4 %.
парацетамол = 0,250 ± 0,006 (г). Погрешность определения концентрации парацетамола с учётом погрешности измерений составила 4 %.
Среднее значение концентрации анальгина в модели «Саридон», полученное методом Фирордта, составляет (табл. 2): Ханальгина = 0,10 ± 0,05 (г). Относительная погрешность Е = 50 %. Исходная концентрация анальгина в модельной смеси 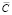 анальгин = 0,150 ± 0,007 ( %). Погрешность определения концентрации анальгина методом Фирордта с учётом погрешности удовлетворяет требуемой точности.
анальгин = 0,150 ± 0,007 ( %). Погрешность определения концентрации анальгина методом Фирордта с учётом погрешности удовлетворяет требуемой точности.
Количество кофеина определяли по формуле (5), используя оптическую плотность модельной смеси на длине волны 280 нм. На этой длине волны наблюдалось максимальное поглощение кофеина и минимальные значения поглощения парацетамола и анальгина. Оптическая плотности кофеина составила D280 = 0,245 ± 0,003. Исходная концентрация кофеина в модельной смеси равнялась Скофеин = 0,0500 ± 0,0016 г. Из анализа спектра поглощения на длине волны 280 нм концентрация кофеина составила – Хкофеин = 0,0495 ± 0,0006 (%). Относительная погрешность вычисления составляет Е = 1,2 %. Погрешность определения концентрации кофеина методом Фирордта с учётом погрешности измерений составляет 1 %.
Проведённый количественный анализ компонентов модельной смеси с удовлетворительной точностью определения концентраций позволил провести аналогичное исследование с таблетками «Саридон». Измеряли оптическую плотность с помощью спектрофотометра при длинах волн 230, 250 нм – для парацетамола и анальгина и 280 нм – для кофеина, в кюветах толщиной 10 мм. Раствор сравнения – 0,01 моль/л раствор гидроксида натрия.
Методика приготовления исследуемого раствора – таблетки «Саридон»
Точную навеску порошка 20 растёртых таблеток (около 0,45 г) помещали в мерную колбу вместимостью 100 мл и растворяли в 50 мл 0,01 моль/л растворе гидроксида натрия, перемешивали, доводили до метки, фильтровали. 1 мл фильтрата помещали в мерную колбу вместимостью 100 мл и доводили объём до метки растворителем.
Содержание парацетамола и анальгина вычисляли методом Гаусса. Результаты расчётов представлены в табл. 3.
Средние значения концентрации парацетамола в таблетках «Саридон», полученные методом Фирордта (табл. 3): Хпарацетамола = 0,25 ± 0,01 (г). Относительная погрешность вычислений Е = 4 %. Исходная концентрация парацетамола в таблетке «Саридон» 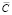 парацетамол = 0,25 ± 0,02(г). Погрешность определения концентрации парацетамола с учётом погрешности измерений 4 %. Средние значения концентрации пропифеназона в таблетках «Саридон», полученные методом Фирордта, составляют (табл. 3): Хпропифеназон = 0,21 ± 0,09 ( %). Относительная погрешность Е = 42 %. Исходная концентрация пропифеназона в таблетках «Саридон»
парацетамол = 0,25 ± 0,02(г). Погрешность определения концентрации парацетамола с учётом погрешности измерений 4 %. Средние значения концентрации пропифеназона в таблетках «Саридон», полученные методом Фирордта, составляют (табл. 3): Хпропифеназон = 0,21 ± 0,09 ( %). Относительная погрешность Е = 42 %. Исходная концентрация пропифеназона в таблетках «Саридон» 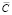 пропифеназон = 0,150 ± 0,011 (г). Погрешность определения концентрации пропифеназона с учётом погрешности измерений составляет 29 %. Для определения количества кофеина в таблетках «Саридон» использовали формулу (5). Оптическая плотность кофеина на длине волны 280 нм – D280нм = 0,245 ± 0,004. Рассчитанное значение концентрации кофеина – Хкофеин = 0,0490 ± 0,0008 (г). Относительная погрешность вычисления составляет Е = 1,6 %. Исходная концентрация кофеина в таблетках «Саридон» составляла Скофеин = 0,05 ± 0,004 г. Погрешность определения концентрации кофеина с учётом погрешности измерений составила 2 %, что соответствует требуемой точности.
пропифеназон = 0,150 ± 0,011 (г). Погрешность определения концентрации пропифеназона с учётом погрешности измерений составляет 29 %. Для определения количества кофеина в таблетках «Саридон» использовали формулу (5). Оптическая плотность кофеина на длине волны 280 нм – D280нм = 0,245 ± 0,004. Рассчитанное значение концентрации кофеина – Хкофеин = 0,0490 ± 0,0008 (г). Относительная погрешность вычисления составляет Е = 1,6 %. Исходная концентрация кофеина в таблетках «Саридон» составляла Скофеин = 0,05 ± 0,004 г. Погрешность определения концентрации кофеина с учётом погрешности измерений составила 2 %, что соответствует требуемой точности.
Таблица 3
Результаты спектрофотометрического анализа парацетамола и пропифеназона в таблетках «Саридон»
|
Название препарата |
D250x |
D230x |
Метод Гаусса |
|
Xi, г |
|||
|
Парацетамол |
0,120 |
0,08 |
0,240 |
|
Пропифеназон |
0,174 |
||
|
Парацетамол |
0,130 |
0,09 |
0,244 |
|
Пропифеназон |
0,297 |
||
|
Парацетамол |
0,125 |
0,09 |
0,267 |
|
Пропифеназон |
0,072 |
||
|
Парацетамол |
0,135 |
0,08 |
0,270 |
|
Пропифеназон |
0,196 |
||
|
Парацетамол |
0,130 |
0,09 |
0,244 |
|
Пропифеназон |
0,297 |
Заключение
В работе были исследованы оптимальные условия проведения спектрофотометрического анализа компонентов таблеток «Саридон». Растворителем был выбран 0,01 моль/л раствора натрия гидроксида. Была создана адекватная модель таблеток «Саридон». Для выбора АДВ, необходимых для применения метода Фирордта, был предложен метод производной спектроскопии, для осуществления которого использовалась компьютерная программа.
Полученные результаты позволяют сделать вывод о том, что метод Фирордта можно применять для определения концентраций компонентов лекарственных препаратов, однако точность исследований будет зависеть от условий экспериментальных исследований. Для повышения точности количественного определения веществ в смеси необходимо снимать спектры поглощения с шагом не более 2 нм, чтобы точнее определять АДВ, влияющие на концентрацию определяемого вещества в смесях. Для выбора АДВ применять метод производной спектроскопии.
Библиографическая ссылка
Цокова Т.Н., Котлова Л.И. ОПРЕДЕЛЕНИЕ КОНЦЕНТРАЦИИ ЛЕКАРСТВЕННЫХ СМЕСЕЙ, СОДЕРЖАЩИХ ПРОПИФЕНАЗОН, ПАРАЦЕТАМОЛ, КОФЕИН, МЕТОДОМ ФИРОРДТА // Международный журнал прикладных и фундаментальных исследований. 2019. № 4. С. 76-81;URL: https://applied-research.ru/en/article/view?id=12701 (дата обращения: 14.05.2026).