Scientific journal
International Journal of Applied and fundamental research
ISSN 1996-3955
ИФ РИНЦ = 0,556
THE MOLECULAR BASES OF ALLERGY INDUCED BY HOUSE DUST MITES DERMATOPHAGOIDES PTERONYSSINUS
Клещи домашней пыли (HDM, Dermatophagoides sp.) являются одним из самых распространенных источников воздушных аллергенов во всем мире, сенсибилизация HDM затрагивает от 1 % до 2 % населения мира, что эквивалентно 65–130 миллионам человек [1]. С XVII в. известно, что вдыхание домашней пыли может вызвать астму и ринит. Однако только в 1964 г. группа, работающая с Рейндертом Воорхорстом и супружеской парой Фрица Т. Спиксма и Марис И. Спиксма-Боземан, продемонстрировала, что наличие HDM в образцах пыли вызвало симптомы астмы [2]. Экспериментальные доказательства указывают на то, что HDM-специфические Th2-клетки играют центральную роль в аллергическом воспалительном ответе, продуцируя IL-4, IL-5, IL-13: IL-4 важен для аллергической сенсибилизации и продукции IgE; IL-5 обеспечивает выживаемость эозинофилов; IL-13 обусловливает плейотропные эффекты в легких [3].
Цель обзора: предоставить основные данные по содержанию аллергенов в экстракте клещей домашней пыли (HDM, Dermatophagoides sp.), описать возможные микробные компоненты, участвующие в индуцированной HDM поляризации T-клеток по Th2 типу.
Классификация аллергенов HMD по группам [3]
|
Группа |
Свойства |
Группа |
Свойства |
|
1 |
Цистеиновая протеаза |
12 |
Хитиназа |
|
2 |
MD-2-подобный липид-связывающий белок |
13 |
Липокалин |
|
3 |
Трипсин-подобная сериновая протеаза |
14 |
Вителлогенин/аполипофорин-подобный белок |
|
4 |
Амилаза |
15 |
Хитиназа |
|
5 |
Липид-связывающий белок |
16 |
Гельсолин |
|
6 |
Хемотрипсин-подобная сериновая протеаза |
17 |
EF-Ca2+-связывающий белок |
|
7 |
Липид-связывающий белок |
18 |
Хитиназа |
|
8 |
Глутатион-S-трансфераза |
19 |
Антимикробный пептид |
|
9 |
Коллагенолитическая сериновая протеаза |
20 |
Аргининовая киназа |
|
10 |
Тропомиозин |
21 |
Липид-связывающий белок |
|
11 |
Парамиозин |
22 |
Липид-связывающий белок |
Клещи домашней пыли относятся к семейству Pyroglyphidae, подклассу Acari, классу Arachid, роду Anthropods. Наиболее распространенными видами являются Dermatophagoides pteronyssinus и Dermatophagoides farinae. Существуют три вида экскреторных выделений клещей: личиночные шкурки, секрет латеральных желез и экскременты (фекальные шарики) [4]. Кроме идентифицированных HDM-аллергенов фекалии клеща содержат белковые и небелковые соединения, которые могут участвовать в активации врожденного иммунитета.
HDM рассматривается не только как носитель аллергена, а также как важный транспортер микробных PAMPs (консервативных молекулярных структур (паттернов), ассоциированных со специфическим патогеном), способных вызывать реакции врожденного иммунитета. Домашняя пыль, естественная среда обитания клещей, содержит большое количество ЛПС (липополисахарид, эндотоксин) и/или бактерий, а также β-глюканов и/или грибов, которые могут быть связаны с аллергенами HDM [5, 6]. Хитин, полимер из звеньев β-(1-4)-поли-N-ацетил-D-глюкозамина, входящий в состав экзоскелета клещей и обнаруженный в их фекалиях, поляризует иммунные ответы по типу Th1, Th2 и Th17 [7]. Было показано, что введение хитина in vivo в мышей рекрутирует IL-4-позитивные врожденные иммунные клетки, включая эозинофилы и базофилы [8]. Остальные примеси экстракта, такие как флагеллин и β-глюканы, активируют TLR5 и TLR2 соответственно [9]. Найденная в экстрактах клещей бактериальная рибосомальная РНК свидетельствует о наличии эндосимбионтов [10].
Аллергены HDM были классифицированы в соответствии с системой номенклатуры Линнея, которая поддерживается Всемирной организацией здравоохранения (ВОЗ) и Подкомитетом по номенклатуре Международного союза иммунологических обществ (IUIS). HDM-аллергены называются Der (первые три буквы рода Dermatophagoides), p или f (первая буква вида pteronyssinus или farinae) и число, представляющее порядок, в котором они были очищены или классифицированы [11]. Аллергены D. pteronyssinus и D. farinae гомологичны, имеют аналогичные биологические активности, среди них выделяют четыре класса соединений: протеазы; белки, имеющие сродство к липидам; непротеолитические ферменты и неферментативные компоненты (таблица).
Приблизительно 80–90 % всех людей, страдающих аллергией на клещей, реагируют с частично выраженными аллергическими симптомами на аллергены основных групп – 1 и 2. Der p 23, впервые идентифицированный в 2013 г., также классифицируется как основной аллерген, поскольку он также имеет большое клиническое значение (уровень сенсибилизации около 70 %). Специфичные для Der p 23 уровни IgE у тестируемых пациентов были сопоставимы с уровнями IgE с Der p 1 и Der p 2. Der p 1 и Der p 2 быстро элюируются из фекальных гранул в водных растворах, тогда как Der р 23 элюируется медленно и в меньших количествах [12]. Возможно, что Der p 23 способен напрямую активировать врожденную иммунную систему [13].
Белки первой группы рассматриваются как папаин-подобные цистеиновые протеазы; 3, 6 и 9 группы представляют собой трипсин-подобные, хемотрипсин-подобные и коллагенолитические сериновые протеазы соответственно. Эти протеазы, скорее всего, участвуют в пищеварении клеща, поскольку они были обнаружены в клетках отделенных от стенки кишечника и в фекалиях [14]. Однако в отличие от белков первой группы они играют незначительную роль в связывании с IgE. Протеазы D. pteronissinus активируют эозинофилы и бронхиальные эпителиальные клетки, инициируют высвобождение воспалительных медиаторов тучных клеток [15].
Группы 5, 7 и 21 могут связывать липиды, гликопротеины и гликолипиды для взаимодействия с врожденной иммунной системой и влиять на доставку антигена [16]. Аллергены этих групп выявляются примерно у 30 % пациентов с аллергией на клещей домашней пыли и связаны с началом аллергической астмы [2]. Исследование структуры димеризованного Der p 5 показало наличие большого гидрофобного кармана, который может представлять собой сайт для связывания гидрофобных лигандов, позволяющий, подобно 2-й группе аллергенов HDM, транспортировать PAMPs липидной природы [17]. Der p 5 также стимулирует продукцию IL-6 и IL-8 в эпителиальных клетках дыхательных путей человека [18]. Аллергены группы 7 обладают сходной структурой с ЛПС-связывающим белком (LBP) [19, 20]. В отличие от белков группы 2 они не связывают ЛПС, но могут взаимодействовать с другими лигандами, обеспечивая активацию TLR 2-4 [21].
Согласно структурным гомологиям последовательностей аллергены групп 2, 13 и 14 могут быть отнесены к белкам, связывающим жирные кислоты и липиды [21]. Der p 2 демонстрирует структурную гомологию с корецептором TLR4 MD-2 (11 % идентичности, 29 % сходства), известным также как лимфоцитарный антиген 96 (LY96) [22, 23]. Однако наибольшее сходство последовательностей и трехмерных структур Der p 2 имеет с NPC2 (Niemann-Picktype C2 proteins, белки Нимана – Пика типа С2) – 23,5 % идентичности, 44 % сходства. При помощи анализов связывания липидов и масс-спектрометрии было выяснено, что Der p 2, а также его гомолог Der f 2, аналогично NPC2 связывают холестерин. Аллергены группы 13 связываются с жирными кислотами и другими липидами, такими как эйкозаноиды и ретиноиды. Аллергены HDM 14 группы гомологичны семейству липид-транспортирующих белков LLTP (large lipid transfer protein), включающему аполипофорные или вителлогенин-подобные белки, которые, как предполагается, обладают функциями накопления и транспорта энергии [23].
Другие аллергены HDM проявляют ферментативную активность: группы 4, 8 и 20 – представляют собой амилазы, глутатион-S-трансферазы и аргинин-киназы соответственно, тогда как группы 12, 15 и 18 демонстрируют гомологию с хитиназами [3].
Белки тропомиозина и парамиозина составляют группы 10 и 11 соответственно. Тропомиозин Der p 10 также является второстепенным аллергеном, однако из-за высокой гомологии последовательности с другими тропомиозинами он является важным перекрестным аллергеном к продуктам животного происхождения и иногда связан с тяжелыми реакциями [2]. Der p 11, парамиозин клеща, играет вторичную роль у пациентов с респираторной формой аллергии на HDM, являясь основным аллергеном у пациентов с атопическим дерматитом. Аналогично Der p 14 и Der p 18, тропомиозин и парамиозин клеща не встречаются в фекалиях, что указывает на сенсибилизацию к этим аллергенам при контакте тела клеща с кожей. Было обнаружено, что контакт с кожей может вызывать аллергическую сенсибилизацию и даже может усиливать последующую респираторную аллергию на тот же антиген [24]. Группы 16 и 17 были идентифицированы как гельсолин-подобные и EF- Ca2+ связывающие белки [3].
Исследования подтвердили важность Толл-подобных рецепторов (TLR) в развитии аллергии на клещей домашней пыли [25]. Совместная активация клеток экстрактом из HDM и эндотоксином может стимулировать TLR4-зависимое аллергическое воспаление дыхательных путей при очень низких уровнях ЛПС. Гомология Der p 2 и MD-2 обусловливает активацию TLR4-сигнального пути на клетках бронхиального эпителия через прямое взаимодействие с Der p 2 в отсутствии связывания ЛПС с MD-2 [16]. Модель сенсибилизации дыхательных путей Der p 2+ЛПС вызывала аллергическую астму у мышей дикого типа и MD-2-дефицитных, но не TLR4-дефицитных, что явно подтверждает, что Der p 2 может переносить ЛПС на TLR4. Аллергенность белков 2-й группы является следствием аутоадъювантных свойств, что было подтверждено связыванием Der f 2 и ЛПС (афинность Der p 2 к ЛПС ниже, чем Der f 2) [26]. Der p 2 индуцирует аллергическую астму прямым связыванием с TLR4 или связыванием с TLR4 после взаимодействия с ЛПС [27]. Th2-смещенный ответ на Der p 2 при подкожном введении не зависит от функционального TLR4 (который, возможно, имеет защитную функцию против кожных аллергенов) [28].
Из-за наличия гидрофобного кармана в структуре белков-аллергенов HDM 2-й группы кроме ЛПС с ними также могут связываться другие липидные соединения, которые потенциально могут активировать гетеродимеры TLR1/TLR2 и TLR2/TLR6, проявляющие сродство к бактериальным липопептидам/липопротеинам. Рекомбинантный Der p 2 способен стимулировать гладкомышечные клетки дыхательных путей TLR4-независимым способом, через TLR2 по MyD88-зависимому сигнальному пути. [29]. Это указывает на то, что гидрофобный карман Der p 2 может транспортировать липиды, отличные от ЛПС, являющиеся лигандами TLR2. Der p 2 также способствует активации В-клеток человека через индукцию TLR4/MD-2 и NF-κB-зависимый синтез IL-1β, CXCL10, IL-8 и TNF-α [30]. In vitro показано, что Der p 2 взаимодействует с TLR4 при участии положительно заряженных аминокислотных остатков, индуцирует секрецию IL-6, IL-8 и MCP-1 в нормальных и аллергических лимфоцитах. Секретируемые в ответ на Der p 2 цитокины подавляют спонтанный апоптоз нейтрофилов [31], передача сигнала осуществляется при участии TLR4, Lyn, PI3K, Akt, ERK и NF-κB [32, 33].
Экстракт клещей D. pteronyssinus (DpE) стимулирует продукцию IL-4 и IL-13 в чувствительных к клещам базофилах при астме [34]. Показано, что DpE повышает экспрессию мРНК и секрецию белков MCP-1, IL-6 и IL-8 без участия протеаз, входящих в состав экстракта; в регуляции экспрессии MCP-1, IL-6 и IL-8 участвуют тирозинкиназа Src-семейства PKC δ и ERK, тогда как p38 MAPK участвует в регуляции экспрессии MCP-1 и IL-6 [35]. Следует отметить, что состав коммерческих экстрактов аллергенов из клещей домашней пыли может в значительной степени изменяться в зависимости от способа их подготовки, что приводит к их отличиям по ряду характеристик: содержание эндотоксина; различные количества основных групп аллергенов (Der p 1, Der p 2); отсутствие некоторых групп [14, 36]. Параллельно с исследованиями на экстрактах осуществляется изучение биологической активности рекомбинантных белков клеща (преимущественно исследуются белки 1, 2, 3, 6, 9 группы) [37].
Упрощенная модель иммунной активации при аллергии HDM представлена на рисунке.
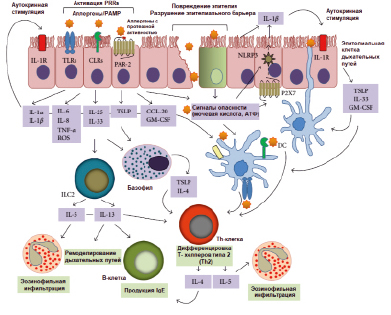
Упрощенная модель HDM-индуцированной иммунной активации, приводящей к аллергической астме [Jacquet A., 2013 (с изменениями)]
Джекет предложил заменить классификацию аллергенов согласно их способности стимулировать врожденные иммунные реакции. В таком контексте две группы аллергенов играют решающую роль в HDM-индуцированном врожденном иммунитете: протеазы (группы 1, 3, 6 и 9), которые непосредственно вызывают передачу сигналов через протеолитические атаки и липидсвязывающие белки (группы 2, 5, 7, 13, 14 и 21), которые могут переносить PAMPs на основе микробных липидов. Однако не выяснено, обладают ли липидсвязывающие белки собственной аллергенностью или их способность активировать клетки обусловлена связанными с ними липидами [3].
Заключение
Клещей домашней пыли следует рассматривать как организм, несущий как собственные аллергены с характерными свойствами, так и содержащий эндосимбиотические и/или загрязняющие микробные компоненты. Собственные аллергены представлены двумя основными группами: белки пищеварительного тракта, выделяющиеся в окружающую среду в составе фекальных шариков, и структурные белки клеща. Фекальные шарики имеют диаметр 10–40 мкм и поэтому могут откладываться не только на слизистой оболочке верхних дыхательных путей, но и попадать в легкие. Следует отметить, что микробные соединения, обнаруженные в клещах домашней пыли, в значительной степени участвуют в индуцированной HDM Th2-поляризации посредством активации PRRs (рецепторов, распознающих молекулярные паттерны). В связи с этим необходимо уделять внимание идентификации микробных соединений, присутствующих в экстрактах или среде. Подробное изучение рецепторов и сигнальных путей, вовлеченных в аллергический ответ, позволит разработать более эффективное лечение для пациентов с аллергией на клещей домашней пыли.
Библиографическая ссылка
Морозова А.А., Косякова Н.И., Прохоренко И.Р. МОЛЕКУЛЯРНЫЕ ОСНОВЫ АЛЛЕРГИИ, ВЫЗВАННОЙ КЛЕЩАМИ ДОМАШНЕЙ ПЫЛИ DERMATOPHAGOIDES PTERONYSSINUS // Международный журнал прикладных и фундаментальных исследований. 2019. № 10-1. С. 137-142;URL: https://applied-research.ru/en/article/view?id=12881 (дата обращения: 29.05.2026).
DOI: https://doi.org/10.17513/mjpfi.12881

