Scientific journal
International Journal of Applied and fundamental research
ISSN 1996-3955
ИФ РИНЦ = 0,556
DYNAMICS OF BLOOD COUNTS IN PATIENTS WITH RADIAL SHAFT FRACTURE TREATED BY TRANSOSSEOUS OSTEOSYNTHESIS WITH THE EXTERNAL FIXATION DEVICE OF THE ROD CONFIGURATION
Чрескостный остеосинтез как метод лечения переломов костей предплечья на уровне диафизов используется ограниченно, но продолжает совершенствоваться. Анализируя литературу, можно встретить достаточное количество публикаций, подтверждающих эффективность применения чрескостного остеосинтеза разнообразными видами фиксаторов: спицами, резьбовыми стержнями и их комбинациями [1–3].
При изучении биомеханических исследований чрескостного остеосинтеза в большинстве случаев проводится сравнительный анализ функциональных возможностей аппаратов внешней фиксации разных компоновок и стабильности систем «аппарат – кость» [3, 4].
Наряду со спицевыми компоновками аппаратов внешней фиксации, стали внедряться стержневые аппараты и их модификации, что дало возможность дифференцированного и оптимального выбора конструкций. Это позволило обеспечить манёвренность аппаратов – упрощение проведения монтажа аппарата за счёт уменьшения количества чрескостных элементов (стержней-шурупов) в рекомендуемые позиции; проведение максимально точной закрытой репозиции отломков с восстановлением целостности кости; восстановление функций мышечного аппарата сегмента и смежных ему суставов в наиболее короткие сроки; адаптированность аппаратов к сегментам; проведение адекватного лечения ран мягких тканей сегмента при открытых повреждениях.
Известно, что продолжительность реабилитационного срока зависит от многих факторов (точная репозиция, жёсткая фиксация костных фрагментов, ранняя функция в смежных суставах, снижение общего веса конструкции), в том числе и от баланса в системе гемостаза.
Нами проведено исследование влияния введённых чрескостных элементов (спиц) при выполнении чрескостного остеосинтеза повреждённой лучевой кости на показатели периферической крови. Считаем данное направление комплексного исследования гемостатических показателей перспективным и требующим дальнейшего изучения при использовании технологии чрескостного остеосинтеза [5].
Цель исследования: оценить динамику лабораторных показателей крови у больных с переломами лучевой кости на уровне диафиза при использовании чрескостного остеосинтеза стержневой компоновки аппарата внешней фиксации.
Материалы и методы исследования
Обследовано 46 пациентов: 26 женщин и 20 мужчин в возрасте от 25 до 60 лет с переломом диафиза лучевой кости в средней трети со смещением костных отломков согласно классификации АО/ASIF (тип 22А2).
Забор крови для исследования проводили утром натощак из локтевой вены в пластиковые пробирки для гематологических исследований в следующие сроки: до операции; на третьи и седьмые сутки после операции. Определялись следующие показатели: эритроциты, гемоглобин, лейкоциты, тромбоциты, фибриноген, активированное парциальное тромбопластиновое время (АПТВ), растворимые фибрин-мономерные комплексы (РФМК). На коагулометре Sysmex (Япония) определяли АПТВ, фибриноген, РФМК при помощи диагностических наборов фирмы «Технология – стандарт». Эритроциты, гемоглобин, лейкоциты, тромбоциты определяли на автоматическом гематологическом анализаторе Mindray BC- 5300 (China).
Монтаж аппарата внешней фиксации выполняли согласно «Методу унифицированного обозначения чрескостного остеосинтеза» [6].
Чрескостные элементы – стержнями-шурупами М6, D = 4 мм, L = 90 мм конической формы в количестве четырёх, проведёнными через оба кортикальных слоя лучевой кости, изолированно от локтевой кости на уровне I, III, VI и VIII. Таким образом, сохранялась ротация предплечья. Стремясь уменьшить вес и размеры аппарата, а также повысить его репонирующие возможности, была изменена форма внешней опоры – кольцевая на сектор, и добавлен репонирующий узел [7]:
|
I, 9, 90; |
III, 10, 80; |
VI, 11, 90; |
VIII, 12, 90 |
|||
|
сектор |
сектор |
сектор |
сектор |
В основу исследования положено сравнение динамики изменений показателей крови обследуемых пациентов с переломами лучевой кости на уровне диафиза, пролеченных методикой чрескостного остеосинтеза стержневой компоновкой аппарата внешней фиксации.
Для оценки достоверности полученных данных применяли стандартные значения критерия Стьюдента. При обработке результатов на персональном компьютере использовали статистическую программу «Statistica».
Результаты исследования и их обсуждение
Исследования крови, проведённые на базе ФГБНУ ИНЦХТ, в группе больных с повреждением диафиза лучевой кости, которым применён чрескостный остеосинтез АВФ стержневой компоновки, позволили выявить определённые закономерности. В дооперационном периоде изучаемые показатели крови находились в пределах физиологической нормы (таблица).

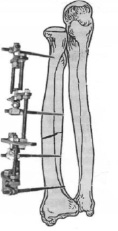
Рис. 1. Схема стержневой компоновки лучевой кости (диаметр опор выбран условно)
Лабораторные показатели крови при лечении перелома диафиза лучевой кости чрескостным остеосинтезом с помощью АВФ стержневой компоновки
|
Показатели |
До операции |
3-и сутки после операции |
7-е сутки после операции |
|
Эритроциты, ×1012 г/л |
4,25 ± 0,24 |
3,7 ± 0,18 |
4,0 ± 0,21 |
|
Гемоглобин, г/л |
134 ± 6,5 |
120 ± 5,9 |
135 ± 6,0 |
|
Лейкоциты, ×109 г/л |
7,6 ± 1,57 |
10,0 ± 1,5 |
8,2 ± 0,97 |
|
Тромбоциты, ×109 г/л |
221 ± 16,5 |
238 ± 11,8 |
247 ± 19,9 |
|
Фибриноген, г/л |
3,8 ± 0,5 |
3,2 ± 0,58 |
3,7 ± 0,33 |
|
АПТВ, с |
38 ± 0,24 |
28 ± 0,35 |
29 ± 0,25 |
|
РФМК, мг/100 мл |
4,18 ± 0,32 |
3,71 ± 0,63 |
2,7 ± 0,34 |
Количество эритроцитов, гемоглобина, лейкоцитов до операции и в послеоперационном периоде не имело статистически значимых различий. Отмечено, что на протяжении всего срока наблюдения страдает система гемостаза. По данным таблицы, по сравнению с дооперационным периодом лабораторные показатели гемостаза у больных выявили статистически значимые различия (увеличение количества тромбоцитов за счёт выброса их из депо, укорочение времени АПТВ, снижение количества РФМК). На седьмые сутки послеоперационного периода количество тромбоцитов увеличилось на 11,8 %, что можно объяснить их массированным выбросом из депо. Определение активированного парциального тромбопластинового времени (АПТВ) обычно используется для оценки внутреннего пути свёртывания плазмы крови. По данным таблицы, показатель АПТВ снизился на 23,7 % (с 38 до 29 с), укорочение времени свёртывания возможно при синдроме коагулопатии. Определение в плазме крови растворимых фибрин-маломерных комплексов (РФМК) является маркером внутрисосудистого свёртывания крови при тромбозах, тромбоэмболиях, ДВС-синдромах. Показатель РФМК на седьмые сутки после операции снизился по сравнению с дооперационным периодом на 35,7 % (рис. 2), свидетельствуя о положительной динамике процесса.
Изучение количества тромбоцитов, АПТФ и РФМК является важным для определения гемодинамических сдвигов, наблюдающихся при чрескостном остеосинтезе аппаратом стержневой компоновки, и определяет эффективность данного способа лечения. Циркулирующая в кровеносном русле кровь при нарушении целостности стенки кровеносных сосудов вследствие травмы претерпевает изменения, в свёртывающей системе срабатывает система регулирующая агрегатное состояние крови. Данная регуляция осуществляется механизмами с участием факторов свёртывающей и противосвёртывающей, и фибринолитической систем. При переломе кости нарушение функциональных взаимосвязей взаимодействующих систем может привести к патологическим состояниям, опасным для организма (кровоточивость или внутрисосудистое тромбообразование).
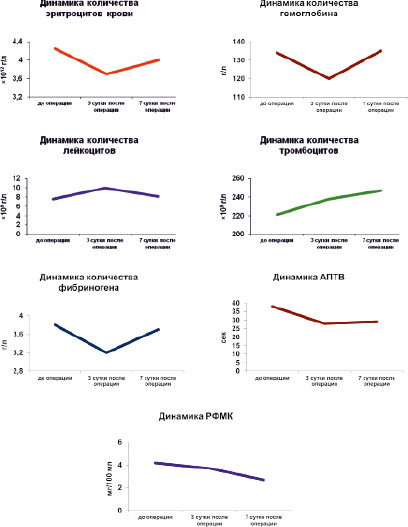
Рис. 2. Динамика показателей крови при лечении перелома диафиза лучевой кости чрескостным остеосинтезом с помощью АВФ стержневой компоновки
Отсутствие достоверных изменений фибриногена по сравнению с показателями в дооперационном периоде, возможно, связано с низкой острофазовой реакцией организма на механическое повреждение мягких тканей кости при проведении стержней-шурупов.
Монолатеральное проведение чрескостных стержней при монтаже аппарата внешней фиксации вызывает незначительную механическую травму сегмента и, следовательно, не происходит выраженной активации процессов свёртывания, как по внешнему механизму за счёт поступления в кровяное русло тромбопластина, так и по внутреннему – за счёт контакта с повреждённой поверхностью эндотелия.
Таким образом, суммируя все данные по исследованию лабораторных показателей крови при хирургическом лечении лучевой кости с применением метода чрескостного остеосинтеза аппаратом внешней фиксации стержневой компоновки, можно сделать вывод, что в системе гемостаза претерпели изменения показатели активированного парциального тромбопластинового времени (АПТВ), растворимых фибрин-маломерных комплексов (РФМК) и количества тромбоцитов, что является защитной реакцией организма в системе регуляции гемостаза. Выявленные изменения в системе свёртывания крови могут иметь значение при выборе тактики хирургического лечения в пользу чрескостного остеосинтеза стержневой компоновки.
Выводы
1. Эффективность репозиции отломков при переломах диафиза лучевой кости с применением стержневой компоновки аппарата внешней фиксации заключалась в снижении веса аппарата в целом за счёт секторов, улучшении его функциональности за счёт наличия репозиционных узлов, позволяющих устранять остаточное смещение отломков в любой плоскости. Стабильная фиксация костных отломков меньшим количеством чрескостных элементов (стержней) уменьшает риск воспаления мягких тканей вокруг чрескостных элементов. Жёсткость фиксации в системе «аппарат – кость» даёт возможность начать ранние движения в суставах оперированного предплечья, в том числе и ротационных.
2. Выявленные изменения в системе гемостаза (увеличение количества тромбоцитов, снижение уровня фибриногена и уровня РФМК) характеризуют активацию внутренних механизмов свёртывающей системы крови и свидетельствуют в пользу применения чрескостного остеосинтеза стержневой компоновки у пациентов с переломами лучевой кости на уровне диафиза. Необходим постоянный контроль этих показателей на всех этапах реабилитации с целью оценки состояния пациента и возможности своевременной профилактики осложнений.
Библиографическая ссылка
Бутаев Ч.З., Пусева М.Э., Кинаш И.Н., Ипполитова Е.Г. ДИНАМИКА ПОКАЗАТЕЛЕЙ КРОВИ У ПАЦИЕНТОВ С ПОВРЕЖДЕНИЕМ ДИАФИЗА ЛУЧЕВОЙ КОСТИ ПРИ ИСПОЛЬЗОВАНИИ МЕТОДА ЧРЕСКОСТНОГО ОСТЕОСИНТЕЗА АППАРАТОМ ВНЕШНЕЙ ФИКСАЦИИ СТЕРЖНЕВОЙ КОМПОНОВКИ // Международный журнал прикладных и фундаментальных исследований. 2019. № 11. С. 49-53;URL: https://applied-research.ru/en/article/view?id=12930 (дата обращения: 26.05.2026).
DOI: https://doi.org/10.17513/mjpfi.12930

