Scientific journal
International Journal of Applied and fundamental research
ISSN 1996-3955
ИФ РИНЦ = 0,556
RESEARCH OF THE FORMS OF METALS IN THE PRODUCTS OF THE COMPLEX CHLORIDE TECHNOLOGY OF ASH PROCESSING
Истощение запасов первичного сырья, снижение его качества привело к резкому росту некондиционных полупродуктов и отходов. Ввиду отсутствия рациональной технологии их переработки значительные объемы накопленных отходов занимают большие территории и представляют серьезную экологическую проблему. В этом ряду вопросы ресурсосбережения и разработки новых перспективных технологий переработки золошлаковых отходов ТЭЦ приобретают острый характер. На сегодняшний день объемы ежегодного выхода и накопления золы в разрезе развитых стран огромны: Индия – 112 млн т, Китай – 100 млн т, США – 75 млн т, Германия – 40 млн т, Великобритания – 15 млн т [1, 2].
В Казахстане годовой выход золы, а также золошлаковых смесей, полученных после сжигания углей, составляет приблизительно 19 млн т. Объем отходов, накопленных на сегодняшний день в золоотвалах, составляет более 300 млн т [3]. Переработка золы и развитие производства электроэнергии является одним из главных приоритетов государства.
Используемые на практике методы переработки золы [4–6] дают возможность извлекать лишь небольшие количества ценных элементов, что с точки зрения комплексности ее использования представляется неэффективным. Согласно вещественному составу золу, полученную после сжигания угля, можно рассматривать как независимое месторождение нерудных и рудных металлов [2, 7, 8]. Химический состав золы зависит от типа сжигаемого угля и может варьировать в широких пределах по основным компонентам. Содержание глинозема может составлять от 5 до 35 %. Золы содержат значительное количество редких, в г/т: Sr – 110, Zr – 2,30, Nb – 7, Ga – до 9, и редкоземельных металлов, в г/т: Y – 14, Eu – 0,68, La – 19, Pr – 7, Sm – до 15. При отсутствии разведанных источников редкоземельных элементов извлечение их из золы становится привлекательным. При переработке золы не требуются дополнительные расходы на добычу и извлечение сырья.
Принимая во внимание сложный химический состав золошлаковых отходов, их нужно рассматривать как перспективный источник сырья для извлечения металлов. При этом нужно учитывать возможность извлечения всех металлов, включая основные их компоненты: оксиды алюминия, кремнезема, железа и цветных металлов. В ракурсе исследования данного вопроса огромный интерес для практики представляет разработанная в работе [9] комплексная, высокоэффективная технология переработки золы с избирательным извлечением кремнезема, оксида алюминия, железа, цветных металлов и РЗМ в товарные продукты. Теоретические аспекты технологии, в части обжига золы совместно с CaCl2 и поведения ее компонентов при обжиге, освещены в работах [10, 11]. С точки зрения расширения границ теоретических знаний хлорирующих процессов и получения новых данных, необходимых для уточнения механизма процесса обжига и выщелачивания, требуется дополнительное комплексное изучение распределения металлов между продуктами хлорирующего обжига и выщелачивания огарка соляной кислотой.
Цель настоящей работы – исследование формы нахождения алюминия, кремнезема, цветных и редкоземельных металлов в огарке и продуктах выщелачивания и определение распределения металлов между продуктами процесса выщелачивания огарка соляной кислотой.
Материалы и методы исследования
В работе исследованы пробы огарка и твердого осадка (кварца), полученные в процессе обжига золы совместно с CaCl2 и выщелачивания огарка соляной кислотой в условиях различного расхода CaCl2, температуры, расхода HCl и Т:Ж.
Комплексным исследованиям подвергнуто 18 выборочных проб от общего количества опытов, из которых 9 проб – пробы огарка и 9 проб – кремнезем, полученный после выщелачивания огарка соляной кислотой.
Химический и фазовый состав исходной золы характеризовали с помощью атомно-абсорбционного спектрофотометра, оснащенного графитовой камерой сгорания (Perkin Elmer 5100). Порошковая рентгеновская дифракция (XRD) проводилась на дифрактометре Ultima III (Rigaku Corp., Япония) с количественным фазовым анализом с использованием программного обеспечения Jade_10 (MDI, Cal.) и базы данных ICSD.
Элементный и фазовый анализ также проводили с использованием электронно-зондового микроанализатора JXA-8230 фирмы JEOL.
С целью повышения достоверности результатов был проведен дополнительный рентгенодифрактометрический анализ на автоматизированном дифрактометре ДРОН-3 (CuКa – излучение, β-фильтр). Условия съемки дифрактограмм: U = 35 кВ; I = 20 мА; съемка θ-2θ; детектор 2 град/мин. По дифрактограммам порошковых проб был проведен рентгенофазовый анализ на полуколичественной основе с применением метода равных навесок и искусственных смесей. Устанавливали количественные соотношения кристаллических фаз. Толкование дифрактограмм проводилось с использованием данных картотеки ICDD: база порошковых дифрактометрических данных PDF2 (Powder Diffraction File) и дифрактограмм чистых от примесей минералов. Для основных фаз проводился расчет содержания.
Результаты исследования и их обсуждение
Формы нахождения металлов в огарке
Результаты EDS картирования пробы огарка, полученного в условиях оптимального режима обжига золы совместно с CaCl2 (Т = 1100 °С; расход CaCl2 – 2 раза больше стехиометрии, необходимого для разложения муллита; τ = 60 минут), показаны на рис. 1.
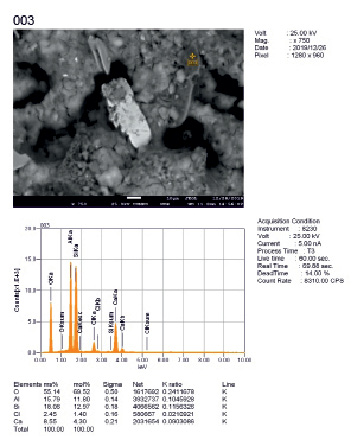
Рис. 1. Результаты EDS картирования пробы огарка
В пробе полученного огарка установлены неоднородности и незначительные участки с ярко выраженными частицами различного химического состава. Это может свидетельствовать о том, что в случае неподвижного слоя золы в условиях обжига, возможно, остается незначительное количество не прореагировавшего с хлоридом кальция огарка.
На рис. 2 показаны дифрактограммы пробы огарка, полученные на аппарате D8 Advance (Bruker).
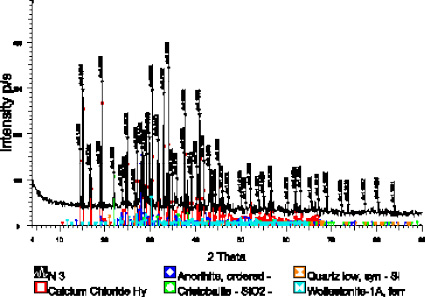
Рис. 2. Дифрактограммы пробы огарка
С использованием программного обеспечения EVA проводилась обработка полученных данных дифрактограмм и расчеты межплоскостных расстояний. При помощи программы Search/match были расшифрованы пробы и проведен поиск фаз. Полученные результаты полуколичественного анализа огарка приведены в табл. 1.
Таблица 1
Результаты полуколичественного анализа огарка
|
Название фазы |
Формула |
Концентрация, % |
|
Анортит |
Ca(Al2Si2O8) |
6,7 |
|
Геленит |
Ca2Al(SiAl)O7 |
26,32 |
|
Гематит |
Fe2O3 |
0,96 |
|
Волластонит |
CaSiO3 |
29,67 |
|
Хлорид кальция |
CaCl2 |
13,90 |
|
Кварц |
SiO2 |
1,35 |
|
КПШ |
KAlSi3O8 |
21,1 |
Для повышения точности и достоверности результатов, а также проведения сравнительного анализа пробы огарков были подвергнуты дополнительному рентгенофазовому анализу. Фазовый состав огарка характеризовали с помощью атомно-абсорбционного спектрофотометра, оснащенного графитовой камерой сгорания (Perkin Elmer 5100). Порошковая рентгеновская дифракция (XRD) проводилась на дифрактометре Ultima III (Rigaku Corp., Япония) с количественным фазовым анализом с использованием программного обеспечения Jade 10 (MDI, Cal.) и базы данных ICSD.
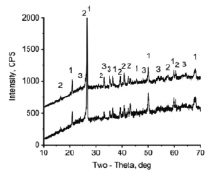
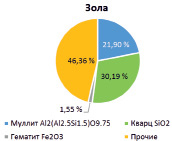
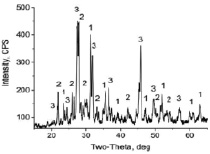
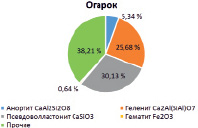
Результаты исследований показаны на рис. 3.
А)
Б)
Рис. 3. Результаты XRD анализа (слева) и фазового состава образцов А) исходная зола (немагнитная фракция); Б) огарок. 1 – анортит; 2 – геленит; 3 – волластонит
Полученные результаты показывают хорошее совпадение с данными полуколичественного анализа, приведенными в табл. 1, что позволяет принять их за основу для расчета рационального состава огарка.
Результаты расчета рационального состава огарка приведены в табл. 2.
Таблица 2
Рациональный состав огарка
|
Соединения |
Al |
Si |
Fe |
Ca |
O |
Cl |
Прочие |
Итого: |
|
Анортит CaAl2Si2O8 |
1,04 |
1,08 |
0,77 |
2,46 |
5,34 |
|||
|
Геленит Ca2Al(SiAl)O7 |
5,05 |
2,63 |
7,51 |
10,49 |
25,68 |
|||
|
Волластонит CaSiO3 |
8,44 |
12,05 |
9,64 |
30,13 |
||||
|
Гематит Fe2O3 |
0,49 |
0,15 |
0,64 |
|||||
|
СаCl2 |
10,41 |
20,65 |
31,06 |
|||||
|
Прочие |
7,15 |
7,15 |
||||||
|
Всего: |
6,09 |
12,15 |
0,49 |
30,74 |
22,74 |
20,65 |
23,22 |
100,00 |
Таким образом, можно заключить, что обжиг немагнитной фракции золы совместно с CaCl2 в условиях окислительной атмосферы сопровождается практически полным разрушением муллита. В полученном огарке алюминий в основном присутствует в виде геленита. В условиях оптимального режима ведения обжига количественное соотношение геленита к анортиту в огарке составляет пять к одному (рис. 3). При дальнейшем выщелачивании огарка соляной кислотой геленит и анортит практически полностью растворяются в соляной кислоте и переходят в маточный раствор в форме хлорида алюминия. Это повышает извлечение алюминия в раствор.
Для практических целей принципиальным представляется организация процесса обжига золы с CaCl2 в условиях перемешивания шихты, например в трубчатой вращающейся печи. Это увеличит контакт частиц золы с хлоридом кальция и создаст благоприятные условия для полного протекания реакций разрушения муллита и образования легкорастворимых соединений алюминия – анортита и геленита.
Наиболее значимым параметром, влияющим на степень разрушения муллита, является расход CaCl2. Математическая обработка результатов экспериментальных опытов позволила установить зависимость степени разрушения муллита (ξ) от расхода CaCl2 и температуры. В результате обработки построено уравнение множественной корреляции, которое имеет вид
ξ = 40,1×CaCl2 + 0,06×Т – 50,09, r = 0,97. (*)
Высокий коэффициент корреляции r = 0,97 уравнения (*) указывает на сильную связь между степенью разрушения муллита и расходом CaCl2 и температурой. При этом, как видно из уравнения, влияние расхода CaCl2 на степень разрушения муллита более значимо.
Формы нахождения металлов в продуктах выщелачивания
Продуктами процесса выщелачивания огарка являются маточный раствор, концентрированный хлоридом алюминия, и твердый осадок кремнезема. В процессе выщелачивания алюминий, железо, цветные и редкоземельные металлы переходят в раствор в виде хлоридов. Выход кремнезема в виде твердого осадка зависит от содержания кремнезема в исходной золе.
В условиях оптимального режима ведения укрупненно-лабораторного опыта по выщелачиванию огарка, выход кремнезема составил ~6 % от веса исходного огарка. Содержание кремнезема, перешедшего в маточный раствор, минимально – 0,14 г/л.
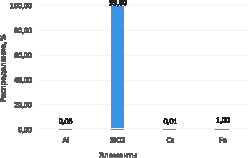
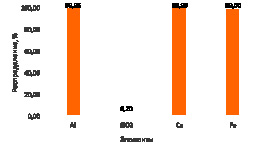
На рис. 4 показано распределение Al, SiO2, Ca и Fe между твердым осадком кремнезема и маточным раствором выщелачивания, рассчитанное по результатам материального баланса укрупненно-лабораторного выщелачивания огарка в оптимальных условиях.
А)
Б)
Рис. 4. Распределение Al, SiO2, Ca и Fe между осадком кремнезема и маточным раствором выщелачивания: А) твердый осадок кремнезема; Б) маточный раствор
Распределение цветных и редкоземельных металлов между продуктами выщелачивания показано на рис. 5.
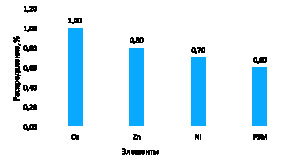
А)
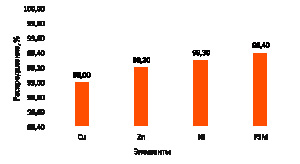
Б)
Рис. 5. Распределение Cu, Zn, Ni и РЗМ между осадком кремнезема и маточным раствором выщелачивания: А) твердый осадок кремнезема; Б) маточный раствор
Заключение
1. Изучены формы нахождения Al, SiO2, Ca, Fe, цветных и редкоземельных металлов в огарке и продуктах выщелачивания. Определено количественное соотношение анортита и геленита в огарке. Установлено, что ~80 % алюминия от общего его количества в золе при обжиге переходит в геленит, а оставшаяся его часть присутствует в форме анортита.
2. Получены новые данные по распределению металлов между твердым осадком кремнезема и маточным раствором. Установлено, что более 99 % цветных металлов и РЗМ переходят в раствор в форме хлоридов.
Исследования проводились в рамках грантового финансирования Комитета науки Министерства образования и науки Республики Казахстан на 2021–2023 годы по приоритетному направлению «Рациональное использование природных ресурсов, в том числе водных ресурсов, геологии, переработки, новых материалов и технологий, безопасных изделий и конструкций» проекта № AP09259637 «Разработка высокоэффективной безотходной технологии для утилизации золы от сжигания угля с получением товарных продуктов».
Библиографическая ссылка
Досмухамедов Н.К., Каплан В.А., Жолдасбай Е.Е., Даруеш Г.С. ИССЛЕДОВАНИЕ ФОРМ НАХОЖДЕНИЯ МЕТАЛЛОВ В ПРОДУКТАХ КОМПЛЕКСНОЙ ХЛОРИДНОЙ ТЕХНОЛОГИИ ПЕРЕРАБОТКИ ЗОЛЫ // Международный журнал прикладных и фундаментальных исследований. 2021. № 10. С. 106-113;URL: https://applied-research.ru/en/article/view?id=13301 (дата обращения: 11.05.2026).

