В последние годы внимание исследователей привлекают серебряные катализаторы, которые в сравнении с металлами платиновой группы значительно дешевле. Серебро, обладая уникальными химическими свойствами, является эффективным катализатором в реакциях гидрогенизации [1, 2]. Серебро используют в качестве катализатора во многих химических реакциях, например в производстве формальдегида и этиленоксида [3].
Целью исследования является создание серебряных катализаторов, нанесенных на углеродные носители, и изучение их физико-химических свойств.
Материалы и методы исследования
В работе в качестве носителей катализаторов использовали: бурый уголь (месторождение Мин-Куш КР) в нативной форме, а также уголь, модифицированный окислением азотной кислотой. Окисленный образец угля получали обработкой 5 % азотной кислотой при 80 °С в течение 2 ч, промывали деионизированной водой до рН 5–6 и сушили при температуре 110 °С. Катализаторы готовили методом ионной адсорбции [4].
Основные физико-химические характеристики полученных катализаторов были определены традиционными методами [5]. Количество и природа функциональных групп на поверхности образцов были определены методом кислотно-основного титрования [6]. ИК-спектроскопический метод анализа выполнен на ИК-спектрометре «Nicolet Avatar 370 GDTS» в диапазоне 4000–400 см-1. ИК-спектры регистрировали в виде таблетки с калия бромидом.
Количественное определение серебра выполнено на атомно-эмиссионном спектрометре с индуктивно-связанной плазмой ICP-AES Agilent 5110 после четырехкратного кислотного разложения.
Исследование структуры носителей и катализаторов проводили методом сканирующей электронной микроскопии на приборе TESCAN Vega 3 LMH, оборудованным энергодисперсионным рентгеновским микроанализатором Oxford X-ACT c программным обеспечением Oxford AZtec Energy. Качественный и количественный энергодисперсионный химический анализ проводился в режимах сканирования Point-ID (точечное сканирование). Для более точного количественного анализа выбиралась плоская поверхность частиц. Для исследования морфологии поверхности использовался детектор вторичных электронов (SE), обеспечивающий топографический контраст исследуемой поверхности. Для уменьшения заряда поверхности использованы низкие ускоряющие напряжения от 2 до 5 КВ.
Результаты исследования и их обсуждение
Данные по элементному и функциональному составу нативного угля и окисленного азотной кислотой приведены в табл. 1.
По результатам элементного анализа установлено, что количество углерода в нативной форме угля выше, чем в модифицированном угле, а количество кислорода увеличивается. Атомные отношения Н/С и О/С характеризуют структурные особенности органической массы угля. Расчетные значения отношения Н/С характеризуют степень ароматичности угля, а О/С – степень окисления угля. Данные элементного анализа показывают значение возрастания отношения Н/С и О/С после кислотной модификации угля, что свидетельствует об уменьшении степени ароматичности и увеличении кислородсодержащих фрагментов в макромолекуле угля. Результаты определения функциональных групп показали, что при обработке угля кислотой количество всех кислотных центров увеличивается с 4,76 до 8,78 мг-экв/г, -ОН групп с 3,90 до 6,61 мг-экв/г и -СООН групп – с 0,86 до 2,17 мг-экв/г. Уменьшение отношения С/N указывает на увеличение азотсодержащих фрагментов в структуре угля.
ИК-спектры носителей и катализаторов представлены на рис.1.
В ИК-спектрах рассматриваемых углеродных носителей присутствует широкая и интенсивная полоса поглощения в области 3500–3300 см-1, которая относится к -ОН и =NH группам, образующим водородные связи. Характеристические полосы с максимумом в области 1720–1700 см-1, вероятно, обусловлены колебаниями связи С=О в карбоксильных и альдегидных группах. Поглощение в области 1300–1000 см-1характерно для деформационных колебаний связи О-Н в спиртовых гидроксилах. Полосы поглощения в области 900–700 см-1 могут быть отнесены к внеплоскостным деформационным колебаниям связей Сар-Н. В области ниже 650 см-1 проявляются колебания скелета углеводородов. Полосы поглощения в области 650–400 см-1можно отнести к характеристическим колебаниям метильных –СН3 групп.
Таблица 1
Элементный и функциональный состав угля
|
Образец |
Элементный состав, атом. % |
Атомные отношения |
Содержание функциональных групп, мг-экв/г |
|||||||
|
С |
H |
N |
S |
O |
Н/С |
О/С |
С/N |
-СООН |
-ОН |
|
|
НУ |
46,04 |
43,20 |
0,85 |
0,23 |
9,68 |
0,94 |
0,21 |
54,16 |
0,86 |
3,90 |
|
МУ |
42,86 |
43,01 |
1,10 |
0,23 |
12,79 |
1,00 |
0,30 |
38,96 |
2,17 |
6,61 |
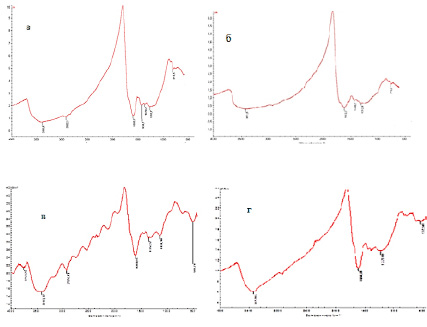
Рис. 1. ИК-спектры носителей НУ (а), МУ (б) и катализаторов НУ-Ag (в), МУ-Ag (г)
В ИК-спектрах угля, обработанного азотной кислотой, в области 1640–1620 см-1 появляется полоса, характерная для валентных колебаний O-N (O-NO2) групп. Валентные колебания связи С=N в группах, сопряженных с открытой цепью, вызывают поглощение в области 1690–1640 см-1. Полоса поглощения при 1440–1400 см-1 характерна для деформационных колебаний –СН2 групп, соединенных с электроакцепторными N+ содержащими центрами. Полосы поглощения в области 1340–1250 см-1 характерны для деформационных колебаний –NH групп.
В спектрах нанесенного на углеродный носитель серебра появляется полоса поглощения в области 1620 см-1, показывающая смещение в низкочастотную область, свидетельствующая об ионизации функциональных групп и замещение Н+ на Меn+. Замещение водорода на ион металла характеризуется поглощением при 1608 см-1. Полосы в области 661–506 см-1 характерны для колебаний М-С связей. Положение характеристических полос для связи М-С зависит от природы углеродного носителя. При использовании нативного угля валентные колебания связи Ag-C поглощают свет при 506 см-1, тогда как на окисленном угле связь Ag-C – при 532 см-1.
Текстурные характеристики углеродных образцов и катализаторов представлены в табл. 2.
Таблица 2
Текстурные характеристики образцов
|
Образец |
Sуд, м2/г |
Vпор, см3/г |
Ws, см3/г |
d, нм |
СОЕ, мг-экв/г |
|
НУ |
374 |
0,05 |
0,02 |
0,69 |
0,56 |
|
МУ |
485 |
0,45 |
0,37 |
0,64 |
1,44 |
|
НУ-Ag |
391 |
0,24 |
0,05 |
1,35 |
– |
|
МУ-Ag |
469 |
0,28 |
0,04 |
1,19 |
– |
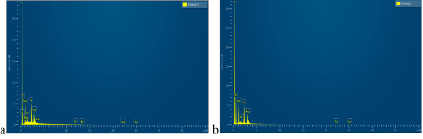
Рис. 2. Данные рентгеновского энергодисперсионного анализа: а – НУ-Ag, b – МУ-Ag

Рис. 3. Снимки СЭМ: НУ (a), МУ (b), НУ-Ag (c), МУ-Ag (d)
Окисленный образец угля имеет на поверхности большее количество протоногенных групп, чем исходный уголь. Удельная поверхность увеличивается у носителя, обработанного кислотой (МУ) и соответствующего катализатора (МУ-Ag), что обусловлено наличием микро- и мезопор.
Содержание активного серебра составило 0,96 % мас. в НУ-Аg, 1,4 % мас. МУ-Ag, которое подтверждалось с помощью атомно-эмиссионного и рентгеновского энергодисперсионного анализов (рис. 2).
Структура и морфология поверхности носителей и катализаторов изучена сканирующей электронной микроскопией (рис. 3).
Снимки СЭМ полученных образцов показывают наличие пористой структуры. Образец нативного угля (рис. 3, а) имеет плотную поверхностную структуру, при этом морфология материала не изменяется. При химической активации угля азотной кислотой получен углеродный носитель с характерной пористой структурой (рис. 3, b), рыхлой морфологией поверхности и текстуры. Текстура поверхности серебряных катализаторов (рис. 3 c, d) состоит из плотно сросшихся глобул, между которыми просматриваются пустоты, образующие бугристую текстуру поверхности. Серебро на поверхности катализаторов имеет кристаллическую структуру.
Заключение
Получены серебряные катализаторы на основе угля Мин-Куш и изучены их физико-химические свойства. Модифицирование угля кислотой приводит к увеличению протоногенных групп на его поверхности. Изучение физико-химических свойств показывает наличие пористой структуры в образцах углеродных носителей и катализаторов, увеличение удельной поверхности у носителя, обработанного кислотой (МУ) и соответствующего катализатора (МУ-Ag), что обусловлено наличием микро- и мезопор.

