Введение
Огромные затраты и время, затрачиваемые на разработку новых лекарств, подчеркивают необходимость «кардинального изменения» парадигмы создания лекарств. Необходимость своевременной адаптации и применения подходов компьютерного моделирования (in silico) в фармацевтических исследованиях широко признана, и ожидается, что это улучшит общую согласованность процесса разработки лекарств [1]. Использование вычислительных методов при поиске и разработке лекарств в настоящее время регулярно используется в качестве инструмента для определения приоритетов экспериментов на каждом этапе процесса. По истечении времени, при проведении исследования, соединение может выходить из строя в процессе разработки, тем дороже оно обходится, следовательно, крайне желательно предсказать этот сбой на ранней стадии процесса разработки лекарственного средства. Количественная оценка характеристики химических структур является основным направлением в изучении взаимосвязей структуры и активности. Информатика и вычислительная химия потенциально могут сыграть важную и разнообразную роль в разработке библиотек, предшествующих синтезу, поскольку невозможно синтезировать каждую молекулу, которая может быть получена. В последние годы изучению взаимосвязи «структура – активность» уделяется значительное внимание, поскольку они могут быть получены непосредственно из молекулярной структуры без особых экспериментальных усилий [2]. Прогнозирование биологической активности лиганда является ключевой проблемой в разработке лекарств. Статистические подходы на основе лигандов часто затрудняются шумом из-за недостаточной выборки: количество молекул, которые, как известно, активны или неактивны, значительно меньше количества возможных химических характеристик, которые могут определять связывание [3].
Успех подходов, связанных с количественным моделированием активности от структуры, можно объяснить возможностью определения приоритета будущих виртуальных аналогов перед синтезом. Методы изучения взаимосвязей, основанные на математическом сравнении связи – перспективны [4].
Цель исследования заключается в проведении поиска числовой структурной характеристики анальгетической активности в ряду амидов и гидразидов N-замещенных антраниловых кислот исследованием взаимодействия молекулярной стыковкой по интерлейкину 2.
Материалы и методы исследования
Статистическую обработку, построенную на корреляции, автор проводил с применением Microsoft Excel 2007 и пакета Statistica 10. Молекулярная стыковка в отношении интерлейкина 2 изучена при помощи программ изучения стыковки Autodock 4 и МGL Tools. Модель биомолекулы (PDB ID code: 1m48 [5]). Обезболивающий эффект определен на модели горячей пластинки, в секундах.
Результаты исследования и их обсуждение
В ходе изучения было выяснено, что в качестве участка стыковки и ориентирования изучаемых молекул, декартовых координат точки – кластера, полученный на основе ацетилсалициловой кислоты (АСК), как вещества, обладающего противовоспалительным и обезболивающим эффектом. Кластер состоит из структур, найденных по результатам стыковки с биомолекулой (интерлейкин 2 (ИЛ-2)), и наименьшим значением потенциальной энергии стыковки (Be = -5,22 ккал/моль) (рис. 1).
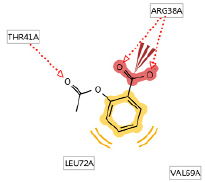
Рис. 1. Область связывания анализируемой АСК с ИЛ-2
Область связывания АСК по биомолекуле интерлейкина 2 включает в себя липофильные области по остаткам аминокислот: лейцин 72 (LEU72A) и валин 69 (VAL62A)). Ионное и водород-связанное взаимодействие с формированием связей кислорода карбонильной группы по остатку аргинина 38, и ацетильного фрагмента по сложно-эфирной группе.
При использовании кластера молекулярная стыковка происходит по четырем фрагментам аминокислот: лейцин 72 (LEU72A), валин 69 (VAL62A), треонин 41 (THR41A) и аргинин 38 (ARG38A)).
Изучение молекулярной стыковки по интерлейкину 2 и корреляционное моделирование проведено для выборки из 24 веществ (рис. 3): амиды и гидразиды N-замещенных антраниловых кислот, общая формула которых представлена на рис. 2.
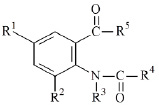
Рис. 2. Строение исследуемых веществ I–XXIV, которые изучены в работе, с радикалами: R1, R2, R3, R4, R5
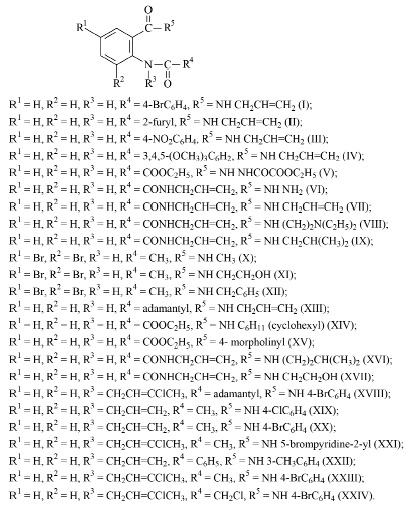
Рис. 3. Строение изучаемых соединений I–XXIV
Для класса веществ, которые исследуются, характерен широкий спектр биологической активности [6, 7].
В результате проведенного молекулярного докинга, основанного на кластере с координатами (x = -4,560, y = 11,693, z = -11,274), автором получены результаты, которые описаны в табл. 1. По каждому производному (I–XXIV) представлены данные: 10 результатов молекулярной стыковки в виде значений энергий по ИЛ 2 (binding energy (Beил 2)).
Выполнен корреляционный отбор методом подстановки и выравнивания по коэффициенту корреляции результатов молекулярного докинга по связи с анальгетической активностью.
Для определения АА использована методика горячая пластинка, данные приведены в секундах (с). Данные, полученные из десяти конформаций по каждому соединению, были подвергнуты статистическому анализу.
Таблица 1
Анальгетическая активность и энергии стыковки анализируемых соединений (I–XXIV) по ИЛ 2
|
№ |
Энергия связывания (Be) по конформациям (Beил 2) |
ААэксп., с |
|||||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
||
|
I |
-6,47 |
-4,53 |
-5,19 |
-5,35 |
-4,9 |
-5,52 |
-5,45 |
-5,54 |
-7,00 |
-4,75 |
17,4 |
|
II |
-4,80 |
-4,45 |
-4,19 |
-5,23 |
-5,3 |
-4,48 |
-4,55 |
-4,37 |
-4,74 |
-4,80 |
31,8 |
|
III |
-5,75 |
-5,30 |
-4,82 |
-6,01 |
-5,88 |
-5,08 |
-5,6 |
-4,71 |
-5,17 |
-4,72 |
23,0 |
|
IV |
-3,96 |
-3,43 |
-4,37 |
-5,22 |
-3,12 |
-3,76 |
-2,88 |
-3,44 |
-4,30 |
-3,34 |
24,4 |
|
V |
-5,36 |
-3,53 |
-4,01 |
-3,44 |
-4,60 |
-3,12 |
-3,27 |
-3,39 |
-3,23 |
-3,86 |
26,0 |
|
VI |
-4,39 |
-5,42 |
-5,22 |
-4,62 |
-4,77 |
-4,03 |
-3,33 |
-3,52 |
-3,92 |
-5,13 |
36,6 |
|
VII |
-5,01 |
-5,26 |
-5,63 |
-4,38 |
-4,74 |
-3,17 |
-3,88 |
-4,26 |
-4,47 |
-3,89 |
31,6 |
|
VIII |
-3,18 |
-3,12 |
-3,10 |
-3,49 |
-2,17 |
-2,08 |
-3,01 |
-4,6 |
-3,69 |
-3,33 |
31,3 |
|
IX |
-3,94 |
-4,06 |
-3,82 |
-3,25 |
-4,21 |
-3,89 |
-3,74 |
-4,54 |
-4,67 |
-3,24 |
27,0 |
|
X |
-4,86 |
-5,03 |
-5,08 |
-4,72 |
-4,34 |
-5,29 |
-5,06 |
-5,23 |
-5,17 |
-5,15 |
21,4 |
|
XI |
-4,29 |
-4,72 |
-3,97 |
-3,82 |
-4,52 |
-4,07 |
-4,15 |
-4,45 |
-4,22 |
-3,56 |
19,0 |
|
XII |
-6,16 |
-6,37 |
-5,73 |
-5,53 |
-5,67 |
-5,46 |
-5,43 |
-5,00 |
-4,85 |
-5,57 |
27,4 |
|
XIII |
-4,05 |
-4,53 |
-6,14 |
-4,88 |
-4,63 |
-4,41 |
-4,13 |
-4,77 |
-4,35 |
-4,83 |
27,0 |
|
XIV |
-4,11 |
-4,33 |
-5,37 |
-5,2 |
-4,76 |
-4,94 |
-3,93 |
-4,72 |
-4,67 |
-4,74 |
31,0 |
|
XV |
-4,28 |
-4,49 |
-3,88 |
-4,28 |
-3,78 |
-3,90 |
-4,32 |
-3,98 |
-4,21 |
-4,47 |
25,0 |
|
XVI |
-4,53 |
-4,28 |
-3,18 |
-3,72 |
-4,53 |
-4,76 |
-3,38 |
-3,24 |
-4,36 |
-4,76 |
28,0 |
|
XVII |
-4,00 |
-4,53 |
-3,27 |
-2,76 |
-4,14 |
-3,20 |
-4,14 |
-4,73 |
-2,59 |
-3,70 |
41,3 |
|
XVIII |
-3,68 |
-4,89 |
-4,83 |
-4,98 |
-5,14 |
-5,39 |
-5,09 |
-4,88 |
-4,38 |
-3,89 |
11,0 |
|
XIX |
-5,25 |
-5,28 |
-4,54 |
-4,81 |
-5,25 |
-5,17 |
-5,04 |
-4,90 |
-5,35 |
-4,50 |
29,0 |
|
XX |
-5,04 |
-5,62 |
-5,63 |
-5,23 |
-5,42 |
-5,21 |
-5,48 |
-4,64 |
-5,40 |
-5,01 |
17,0 |
|
XXI |
-5,10 |
-5,2 |
-4,88 |
-5,17 |
-5,74 |
-5,71 |
-4,90 |
-5,27 |
-5,35 |
-5,28 |
27,0 |
|
XXII |
-5,23 |
-4,64 |
-5,35 |
-4,77 |
-5,51 |
-4,11 |
-5,40 |
-4,88 |
-4,61 |
-5,05 |
13,6 |
|
XXIII |
-5,63 |
-5,47 |
-5,36 |
-5,20 |
-5,18 |
-5,66 |
-5,23 |
-6,02 |
-5,72 |
-5,43 |
21,2 |
|
XXIV |
-5,57 |
-5,19 |
-4,78 |
-4,57 |
-5,07 |
-4,36 |
-5,47 |
-5,01 |
-5,56 |
-5,26 |
15,2 |
Всего изучено 24 соединения (I–XXIV). Проведена оценка взаимодействия исследуемых веществ с активным участком ИЛ-2 по энергии связывания. Вещества с АА: 25 с и более, энергетически взаимодействуют с участком мишени при BeИЛ-2 в диапазоне от -4,49 до -5,42 ккал/моль.
Энергетически коррелируемое взаимодействие позволяет предположить наличие пространственной области биомишени, обеспечивающей контакт с ИЛ-2. Наличие области взаимодействия подтверждается проведением исследования с использованием трехмерного моделирования АА, осуществлен поиск дескриптора АА на основе энергии докинга, выраженной в ккал/моль. Поиск дескриптора осуществлялся методом линеаризации, выравнивая выборку относительно прямой линии, достигая максимальной линейности, что является следствием проводимого изучения, проведением обучения дескриптора на количественную связанность с АА (BeИЛ-2 АА).
Выбор конформаций представлен в табл. 2. В ходе изучения было выявлено, что все соединения имеют высокие показатели стыковки при взаимодействии с различными аминокислотными остатками: аргинин (ARG38), треонин (THR41) и лизин (LYS43). Анализ результатов молекулярного докинга показал, что корреляционный анализ в области поиска дескриптора АА позволяет проводить отбор конформаций вне зависимости от одного пространственного кластера.
По данным, приведенным в табл. 2, обнаружено наличие нескольких кластеров, поэтому обработка выборки только по одному кластеру не приведет к получению целевого результата.
Таблица 2
Результаты взаимодействия анализируемого ряда лигандов с ИЛ-2 по зависимости с ААэксп.
|
№ соединения |
Конформация № |
Н-связь (ИЛ-2) |
BeИЛ-2 |
Ki ИЛ-2, мкмоль |
Ime ИЛ-2 |
RMSD ref |
АА эксп., с |
|
I |
2 |
THR41 |
-4,53 |
479,03 |
-6,02 |
8,13 |
17,4 |
|
II |
5 |
ARG38, THR41 |
-5,3 |
129,92 |
-6,79 |
3,76 |
31,8 |
|
III |
8 |
нет |
-4,71 |
350,25 |
-6,50 |
5,03 |
23,0 |
|
IV |
3 |
ARG38, THR41 |
-4,37 |
628,22 |
-6,75 |
3,80 |
24,4 |
|
V |
5 |
ARG38, THR41 |
-4,60 |
422,17 |
-7,29 |
6,06 |
26,0 |
|
VI |
2 |
ARG38, THR41 |
-5,42 |
106,39 |
-7,21 |
3,08 |
36,6 |
|
VII |
2 |
ARG38, THR41 |
-5,26 |
140,59 |
-7,34 |
3,18 |
31,6 |
|
VIII |
8 |
ARG38, THR41 |
-4,6 |
421,83 |
-7,59 |
5,08 |
31,3 |
|
IX |
9 |
ARG38, THR41 |
-4,67 |
374,69 |
-6,76 |
4,07 |
27,0 |
|
X |
5 |
ARG38 |
-4,34 |
655,09 |
-4,94 |
4,28 |
21,4 |
|
XI |
7 |
нет |
-4,15 |
913,47 |
-5,64 |
5,31 |
19,0 |
|
XII |
9 |
нет |
-4,85 |
278,05 |
-6,04 |
5,77 |
27,4 |
|
XIII |
10 |
LYS43, THR41 |
-4,83 |
286,09 |
-6,33 |
2,01 |
27,0 |
|
XIV |
4 |
ARG38, THR41 |
-5,2 |
154,39 |
-6,99 |
3,34 |
31,0 |
|
XV |
2 |
ARG38 |
-4,49 |
509,07 |
-5,98 |
3,69 |
25,0 |
|
XVI |
10 |
ARG38 |
-4,76 |
326,03 |
-7,14 |
3,76 |
28,0 |
|
XVII |
8 |
ARG38, THR41 |
-4,73 |
343,64 |
-7,11 |
2,95 |
41,3 |
|
XVIII |
1 |
LYS43 |
-3,68 |
2,0 |
-5,47 |
7,89 |
11,0 |
|
XIX |
8 |
ARG38 |
-4,9 |
256,59 |
-6,39 |
4,95 |
29,0 |
|
XX |
8 |
THR41 |
-4,64 |
400,25 |
-6,13 |
6,09 |
17,0 |
|
XXI |
3 |
THR41 |
-4,88 |
262,63 |
-6,38 |
6,85 |
27,0 |
|
XXII |
6 |
ARG38, THR41 |
-4,11 |
976,66 |
-5,90 |
3,60 |
13,6 |
|
XXIII |
5 |
THR41 |
-5,18 |
159,23 |
-6,67 |
5,92 |
21,2 |
|
XXIV |
6 |
THR41 |
-4,36 |
632,42 |
-6,15 |
5,84 |
15,2 |
Проведено описание коррелируемого кластера поиска анализируемого ряда лигандов по результатам анализа Statistica 10 и простого регрессионного анализа. Результаты отбора докинг-конформаций описаны значимым уравнением линейной регрессии (p < 0,05), с коэффициентом корреляции равным 0,720:
BeИЛ-2 АА = – 3,6629 – 0,0408 × АА
(R = 0,720; F = 23,71;
p = 0,00007; S = 0,29; N = 24).
Заключение
Проведена оценка взаимодействия исследуемых соединений с интерлейкином 2, с использованием корреляционного анализа с анальгетической активностью. В ходе проведенного исследования обнаружен коэффициент корреляции R, равный 0,720. Предложенная автором методика, получения направленного дескриптора биоактивности, дает возможность объединить несколько пространственных кластеров в один, связанный с биоактивностью. Параллельно с продолжением расчета взаимосвязи «структура – анальгетическая активность» в ряду анализируемых лигандов ряда, показана возможность анализа биомишени, для выявления биоактивных соединений.

