Scientific journal
International Journal of Applied and fundamental research
ISSN 1996-3955
ИФ РИНЦ = 0,556
STUDY OF DEGRADATION OF GRANULATED MATERIALS COMBINING BIOACTIVE AND ANTIBACTERIAL COMPONENTS
Введение
При разработке материалов, предназначенных для восстановления дефектов твердых тканей человека, большое внимание уделяется их составу с точки зрения регулирования сохранности имплантата в организме, возможности и скорости его резорбции, придания необходимых механических свойств, создания пористой структуры. Формирование столь разноплановых характеристик возможно за счет сочетания в одном материале компонентов, различных по своей природе и свойствам. Так, например, смешение фосфатов и силикатов кальция, различающихся между собой величиной произведения растворимости, позволяет получать композиты с варьируемой скоростью растворения [1]. Введение в материал компонентов, выгорающих при прокаливании, обеспечивает появление системы взаимосвязанных открытых пор в структуре продукта [2], что необходимо для успешной остеоинтеграции имплантата в твердую ткань, его долгосрочной физической стабильности. Для модифицирования механических свойств используются добавки полимерных или неорганических волокон, частиц или упрочняющих фаз [3, 4].
Также возможно придание материалам антибактериальных свойств. Данное направление исследований перспективно ввиду стремления к снижению лекарственной нагрузки на организм человека при замещении дефектов, осложненных бактериальной инфекцией. Разрабатываются покрытия на металлических имплантах, керамики, гранулы, включающие антибиотики [5,6,7]. Однако в связи с развивающейся устойчивостью патогенных штаммов бактерий по отношению к известным антимикробным препаратам актуально создание материалов с альтернативными компонентами, проявляющими бактерицидные свойства. К числу последних можно отнести ряд металлов: серебро, цинк, медь, железо и др. [8]. Широко исследуется введение Ag в состав биоматериалов различной природы [9,10]. Перспективно также использование соединений цинка, ввиду его жизненной необходимости для человека. В работе [11] цинк характеризуют как кальций XXI столетия, поскольку данный элемент входит в состав 70 ферментов, включая щелочную фосфатазу, участвует в усвоении силикатов, играет ключевую роль в регуляции гомеостаза костной ткани, ингибирует резорбцию кости остеокластами, стимулирует дифференцировку и пролиферацию клеток, минерализацию кости остеобластами, проявляет антибактериальные свойства.
На основании вышесказанного выполнена серия экспериментов по получению композитных остеопластических материалов в виде полидисперсных образцов гранул, сочетающих фосфат и силикат кальция (биоактивные компоненты) с оксидом цинка, потенциально способным ингибировать рост бактерий. Последнее возможно при условии выделения ионов цинка в среду, окружающую имплант. В этой связи актуально изучение особенностей из деградации в прототипах биологических жидкостей.
Цель данной работы – исследование динамики деградации сферических пористых гранул, включающих фосфат кальция (гидроксиапатит, ГА, Са10(РО4)6(ОН)2), силикат кальция (волластонит, ВТ, β-СаSiO3), желатин и варьируемое количество оксида цинка (ZnO).
Материалы и методы исследования
Экспериментальные образцы гранул получены по суспензионной технологии с использованием композитного порошка, включающего 60 мас. % Са10(РО4)6(ОН)2 и 40 мас. % β-СаSiO3, синтезированного согласно патенту РФ № 2657817, и порошка оксида цинка, осажденного щелочью из водного раствора ZnCl2 и просушенного на воздухе при 300°С. Минеральная составляющая гранул включала 5, 10, 15, 20 или 25 мас.% ZnO. Согласно данным физико-химических исследований образцы имеют пористую структуру, открытую пористость до 60 %, истинную плотность в районе 2.5 г/см3.
В ходе эксперимента оценивали набухание гранул (изменение их размеров и массы) при выдерживании в Трис-буфере с рН = 7.40, как описано в работе [12].
Динамику растворения гранул изучали по изменению рН раствора и концентрации в нем ионов кальция и цинка. Соотношение массы частиц к объему Трис-буфера составляло 1:2. Каждые сутки из системы отбирали порцию раствора для анализа. рН измеряли на рН-метре «рН-150МИ», укомплектованном электродом «ЭСК-10314/7» (Измерительная техника). Концентрации ионов Са2+ и Zn2+ в растворах определяли спектрофотометрическим методом по интенсивности окраски раствора Арсеназо III и сульфарсазена, соответственно. Все эксперименты проведены в статичных условиях при температуре 22 ± 2 °С в трехкратной повторности.
Гранулы исследовали на микроскопе «Микромед 3 (вар. 3-20М)» (Наблюдательные приборы), оснащенном видеокамерой и программой «ToupView» для обработки изображений. Также выполнен анализ материалов с применением ИК-Фурье-спектроскопии на ИК-спектрометре «ФТ-801» с ПО «ZаIR 3.5» (Симекс) и сканирующей электронной микроскопии на электронном микроскопе «JCM-5700» (JEOL).

Рис. 1. Фотографии гранул, содержащих 15 мас.% ZnO (а, б) и 25 мас.% ZnO (в, г) до (а, в) и после (б, г) выдерживания в Трис-буфере в течение 1 суток
Результаты исследования и их обсуждение
Установлено, что при выдерживании гранул в Трис-буфере происходит их набухание. Частицы увеличиваются в диаметре до 20% за счет набухания связующего (рис. 1). Также во времени растет масса материалов (рис. 2а). Наибольший прирост происходит в первый час контакта частей системы. Очевидно, это связано с заполнением жидкой фазой пор во внутренней структуре частиц и гидратацией желатина. Степень набухания (S) для всех образцов через 7 ч слабо изменяется. Вероятно, в данный период завершается формирование на поверхности гранул гидратированного слоя и начинается активный ионный обмен между твердой фазой и раствором. Об этом свидетельствует резкое повышение рН системы на начальном этапе эксперимента и появление в растворах ионов кальция и цинка (рис. 2б-г).
Установлено отсутствие достоверного различия зафиксированных значений рН и концентрации ионов кальция и цинка в растворах, контактировавших с образцами с варьируемым содержанием ZnO (рис. 2б-г). При этом величина рН и концентрация ионов Са2+ изменяются схожим образом: на зависимостях рН = f(t) и C(Ca2+) = f(t) виден резкий скачок измеряемых параметров через 1 сутки контакта гранул всех изучаемых составов с Трис-буфером, далее до 10 суток водородный показатель и количество кальция в среде быстро падают, после 10-ти суток оба показателя медленно снижаются. Вероятно, это связано с быстрой гидратацией поверхности и компонентов гранул, протекающей со связыванием протонов из среды и их обменом на кальций из состава Са10(РО4)6(ОН)2 и β-СаSiO3. Наблюдаемое в дальнейшем снижение рН и количества ионов кальция в системах может быть связано с протеканием процессов вторичной кристаллизации аморфного фосфата кальция в щелочной среде.
По рис. 2г видно, что концентрация ионов цинка в растворах монотонно увеличивается на всем протяжении эксперимента. Хотя достоверного различия между значениями концентрации Zn2+ в растворах, контактировавших с образцами с варьируемым содержанием ZnO, не выявлено, можно отметить, что количество ионов цинка в системах с гранулами, содержащими 25 мас.% ZnO, превышает таковое для гранул с 5 мас.% ZnO на 5 – 20 мкмоль/л. По окончании эксперимента, через 60 дней контакта материалов с 25 мас.% ZnO с Трис-буфером в растворах содержится до 83 мкмоль/л Zn2+, что соответствует растворению примерно 10% цинка от его исходного содержания в гранулах.
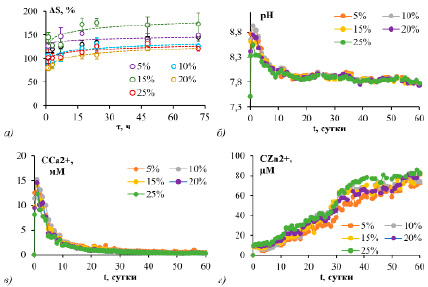
Рис. 2. Зависимости степени набухания гранул (а), рН (б), концентрации ионов кальция (в) и цинка (г) в растворах от содержания ZnO в материалах
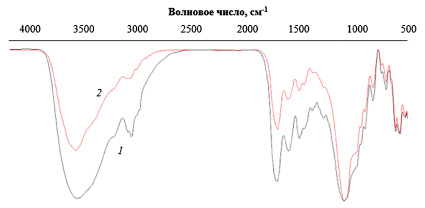
Рис. 3. ИК-спектры гранул, содержащих 25 мас.% ZnO, в исходном состоянии (1) и после 28 суток выдерживания в Трис-буфере (2)
Результаты исследования методом ИК-Фурье-спектроскопии образцов, контактировавших с Трис-буфером в течение 28 суток, указывают на то, что наряду с минеральными компонентами гранул также растворяется желатин (связующее). По рис. 3 заметно снижение интенсивности полос колебаний функциональных группировок, входящих в состав желатина, расположенных в областях 1200 – 1600 см-1 и 2700 – 3000 см-1. О неполном удалении связующего из состава материалов за указанный период также свидетельствует сохранность сферической формы гранул, наблюдающаяся в эксперименте (рис. 4).
В ИК-спектрах гранул, контактировавших с Трис-буфером, не отмечено колебаний, не относящихся к исходным компонентам гранул. Спектры образцов в исходном состоянии и после 28 суток выдерживания в модельном растворе характеризуются набором полос поглощения группировок, входящих в состав гидроксиапатита (563, 603, 630, 962, 1026, 1087 см-1 [13]), волластонита (568, 647, 684, 828, 905, 935, 968, 1020, 1063, 1200 (плечо) см-1 [14]) и желатина (оксид цинка не имеет собственных полос поглощения в области 500 – 4000 см-1). Это позволяет сделать вывод о неизменности качественного состава основного объема гранул. При этом заметно снижение интенсивности полос поглощения группировок Si-O, образующих β-СаSiO3, по истечении 4 недель контакта с водной средой. Очевидно, это связано с большей растворимостью фазы силиката кальция в сравнении с апатитом.
а) 
б) 
Рис. 4. Микрофотографии гранул, содержащих 25 мас.% ZnO, в исходном состоянии (а) и после 28 суток выдерживания в Трис-буфере (б)
На рис. 4 представлены микрофотографии гранул исходном состоянии и после 28 суток выдерживания в Трис-буфере. Видно, что после контакта с водной средой на поверхности сфер появляется большое число пор с диаметром от единиц до нескольких десятков микрометров, гранулы становятся более пористыми. Таким образом, результаты исследования материалов методом сканирующей электронной микроскопии также указывают на постепенное преобразование композитных частиц в результате растворения входящих в их состав компонентов.
Заключение
По результатам выполненного исследования установлено, что синтетические пористые композитные гранулы, сочетающие в своем составе фосфат кальция (гидроксиапатит), силикат кальция (волластонит), желатин и оксид цинка (до 25 мас.%), постепенно деградируют в водном слабощелочном растворе. При этом растворяются все компоненты материалов. Ионы цинка длительно монотонно выделяются в окружающую среду, что может обеспечить устойчивый антибактериальный эффект при имплантации гранул в место инфицированного костного дефекта. При этом варьирование количества ZnO в составе материалов, вероятно, позволит регулировать длительность растворения данной добавки и, соответственно, период противомикробного действия имплантата.
Библиографическая ссылка
Солоненко А.П., Шевченко А.Е., Матюшенко А.А., Полонянкин Д.А. ИССЛЕДОВАНИЕ ДЕГРАДАЦИИ ГРАНУЛИРОВАННЫХ МАТЕРИАЛОВ, СОЧЕТАЮЩИХ БИОАКТИВНЫЕ И АНТИБАКТЕРИАЛЬНЫЕ КОМПОНЕНТЫ // Международный журнал прикладных и фундаментальных исследований. 2024. № 12. С. 58-62;URL: https://applied-research.ru/en/article/view?id=13683 (дата обращения: 05.05.2026).
DOI: https://doi.org/10.17513/mjpfi.13683

