Scientific journal
International Journal of Applied and fundamental research
ISSN 1996-3955
ИФ РИНЦ = 0,556
THE LEVELS OF SEGMENTARY ORGANIZATION OF LYMPH FLOW
Как известно, лимфоток имеет маятникообразный характер. Его регулируют факторы двух групп:
1) вазальные – движения структур стенок лимфатического русла (ЛР), прежде всего – постоянных и множественных клапанов (пассивное ограничение обратного лимфотока) и гладких миоцитов (активное поддержание скорости лимфотока);
2) экстравазальные – воздействия на ЛР окружающих его органов, сосудов, нервов и других структур.
Предложено много концепций об устройстве лимфатической системы (ЛСи): лимфатические сердца L. Ranvier, лимфангионы или клапанные сегменты как функциональные единицы лимфатического сосуда (ЛС) по E. Horstmann – H. Mislin, нервно-сосудистые фрагменты тела и функциональные сегменты лимфатических узлов (ЛУ) Б.В. Огнева, лимфатические регионы Ю.И. Бородина и др. [1–6]. Они с разных сторон характеризуют ЛСи и структурные основы лимфотока, но не дают целостного представления о сегментарной организации лимфотока [7].
Цель исследования: показать структурные уровни сегментарной организации лимфотока.
Материалы и методы исследования
Строение и развитие ЛСи у человека и млекопитающих животных изучены мной на окрашенных тотальных препаратах и гистологических срезах, а также методами иммуногистохимии и электронной микроскопии, инъекции ЛР синей массой Герота и препарирования [4–6].
Результаты исследования и их обсуждение
Лимфа образуется и движется в полости ЛР. Клапаны разделяют ЛР на разные межклапанные сегменты [5–7]: в лимфатических посткапиллярах – безмышечные, организующие пассивный лимфоотток из лимфатических капилляров; в ЛС – мышечные или лимфангионы, способные при дефиците энергии экстравазальных факторов сокращаться и активно продвигать лимфу к венам; в ЛУ – нодальный или лимфоидный лимфангион, который регулирует еще объем и состав лимфы. Сегментарный принцип построения можно также распространить на сеть лимфатических капилляров. Подвижные межклеточные контакты их эндотелия как входные миниклапаны регулируют ток тканевой жидкости в полость ЛР (фильтрацию – лимфообразование). Тканевой насос «качает» тканевую жидкость в полость ЛР: интегральный столб тканевой жидкости (клеточный метаболизм и фильтрат аритериальных капилляров) – «поршень», окружающие ЛР ткани в целом – «манжетка», сдавливающая ЛР с сужением полости и выталкивающая лимфу из корней ЛР. По мере удаления от мест лимфообразования его энергия как первичной лимфодвижущей силы угасает: уплотняющиеся и утолщающиеся стенки ЛР не пропускают тканевую жидкость в полость ЛР, а также ограничивают давление наружной манжетки. Но при растяжении лимфой сравнительно толстых стенок ЛР с разножесткими оболочками (интима «размывается» диффузионными токами лимфы) возникает сдвиговая деформация стенок ЛР. В результате на границе между интимой и адвентицией дифференцируются гладкие миоциты (средний, мышечный слой).
ЛС и ЛУ обычно находят около аорты и ее ветвей, что неудивительно:
1) первичные вены всегда сопровождают артерии эмбриона;
2) часть этих вен выключается из кровотока с образованием первичных ЛС;
3) в их просвет инвагинируют кровеносные сосуды с закладкой ЛУ у плодов – инфильтрация лимфоцитами межсосудистой соединительной ткани инвагинации, интимы ЛР [4].
Лимфоидная ткань ЛУ окружает разветвления хиларных артерий, а сама окружена синусами – краевым (вся паренхима) и промежуточными (части паренхимы – лимфоидные узелки, Т-домены и мозговые тяжи). Поэтому ЛУ, как лимфоидный орган, следует «привязывать» к артериям, а как лимфатический орган (краевой синус с капсулой между входными и выходными клапанами ЛУ) – к ЛС. Промежуточные синусы и трабекулы объединяют лимфатический, межклапанный и лимфоидные, периартериальные сегменты ЛУ в единую систему – лимфоидный лимфангион в составе непрерывного ЛР.
Сегменты ЛСи относятся к двум уровням ее организации [7]:
1) генеральные (общие для ЛР и кровеносного русла), системные;
2) специальные (собственные ЛР), локальные (рис. 1, 2).
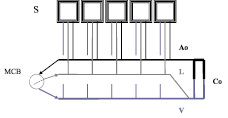
Рис. 1. Схема генеральной сегментации лимфатической системы: Co – сердце; Ao – аорта с ее ветвями; V – главные (полые) вены с их притоками; L – лимфатические протоки с их притоками; MСB – микроциркуляторное русло; S – сегменты тела (~ периферические сегменты лимфатической и всей сердечно-сосудистой системы)
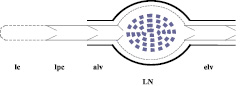
Рис. 2. Cхема собственной сегментации лимфатической системы – лимфатическое русло как цепь межклапанных сегментов с прогрессивно усложняющейся конструкцией стенок: lc – лимфатический капилляр с эндотелиальными стенками, пунктирная линия символизирует подвижные межклеточные контакты, они функционируют как миниклапаны на входе в безмышечный квазимежклапанный сегмент; lpc – лимфатический посткапилляр, в котором появляются типичные, интралюминарные клапаны (безмышечный межклапанный сегмент); alv, elv – афферентный и эфферентный лимфатические сосуды, черные линии символизируют мышечный слой в их стенках (мышечные межклапанные сегменты или лимфангионы); LN – лимфатический узел как нодальный или лимфоидный лимфангион, стенки которого содержат лимфоидную ткань
Генеральные, периартериальные сегменты можно разделить на две группы:
1) центральные, парааортальные;
2) периферические, субаортальные (вдоль ветвей аорты).
Специальные сегменты ЛСи я разделяю на безмышечные и мышечные межклапанные сегменты, а лимфангионы – на сосудистые и нодальные. Собственные сегменты ЛСи соединяются с другими компонентами ее генеральных сегментов (инфраструктура ЛР) посредством рыхлой соединительной ткани. Межклапанные сегменты ЛР окружены общим футляром адвентиции (отсутствует в корнях ЛР). Их наружное продолжение, периадвентиция (кондуктор экстравазальных факторов лимфотока), объединяет стенки ЛР с окружающими органами и сосудами в составе корпоральных сегментов (рис. 3). Высшей ступенью развития генеральных сегментов ЛСи являются ЛУ, в которых межсосудистая соединительная ткань преобразуется в лимфоидную. Более простыми вариантами такого локального морфогенеза генеральных сегментов ЛСи представляются лимфоидные узелки и бляшки.

Рис. 3. Многоуровневая структурно-функциональная организация лимфотока (схема): ЭФ, ВФ – факторы лимфотока, экстравазальные и вазальные (действие окружения и стенок лимфатического русла)
Лимфоток и его факторы относятся к обоим уровням организации ЛСи:
1) лимфообразование, другие экстравазальные факторы лимфотока – генеральные сегменты ЛСи, связи ЛР с окружением (наружной манжеткой). На этом уровне определяются пассивный (базовый) лимфоток и его экстравазальная регуляция;
2) лимфоотток и вазальные факторы лимфотока – собственные, межклапанные сегменты ЛСи, их клапаны и мышечные манжетки (пассивный и активный лимфоток).
Активный лимфоток возникает при торможении пассивного (при дефиците энергии экстравазальных факторов) и возникновении локального лимфостаза, значительном растяжении стенок ЛР и критической деформации сарколемм гладких миоцитов с активацией саркоплазматического ретикулюма. Так запускается сокращение гладких миоцитов, что приводит к повышению тонуса стенок ЛР и/или к их сближению с сужением полости и ускорением лимфотока. Сцепление его внешних и внутренних факторов проявляется в разных формах. Так лимфообразование происходит на стыке сфер влияния вазальных и экстравазальных факторов лимфотока – в корневых генеральных сегментах ЛСи (слепое начало корней ЛР, ограниченное эндотелиоцитами с подвижными контактами). Они переходят в тканевые каналы микроокружения посредством макромолекулярных связей (рис. 4). ЛР адаптируется к условиям дефицита собственной энергии лимфотока путем сегментарного устройства, в т.ч. временной компартментализации – цепной локальной фрагментации полости ЛР закрытыми соседними клапанами. Это позволяет «дробить» лимфоток на порции: лимфа перемещается от одного сегмента к другому и таким образом (клапанами) сегментируется. Их продвижение требует меньше энергии, извлекаемой прежде всего из окружения (экстравазальные факторы).
Важное место в организации лимфотока занимает соединительная ткань, осуществляя взаимосвязь:
1) механическую – ЛС, прежде всего крупных, с кровеносными сосудами, нервами и органами;
2) гуморальную, диффузионную (включая лимфообразование) – прежде всего микроЛС с кровеносными микрососудами, нервными окончаниями и тканями.
Так объединяются наружная и внутренняя манжетки ЛР (интеграция компонентов генеральных сегментов ЛСи – экстравазальная регуляция лимфотока), структуры манжеток.
Особый лимфоток возникает в ЛУ. В ходе развития [4–6] в просвете ЛР формируется лимфоидный фильтр – специальная соединительная ткань, через которую происходит трансфузионный лимфоток:
1) между синусами (непрямой лимфоток через тканевые каналы вещества ЛУ);
2) между синусами и венозными микрососудами (функциональный анастомоз ЛР и кровеносного русла посредством тканевых каналов).
Вторая составляющая трансфузионного (или интерстициального) лимфотока есть процесс, обратный лимфообразованию в корнях ЛР. Их гомологи в ЛУ (сеть промежуточных синусов – ответвления внутренней стенки краевого синуса) погружены в лимфоидную ткань (разросшаяся и разветвленная интима краевого синуса, инфильтрированная лимфоцитами) и вставлены в нодальный сегмент ЛР с мышечной капсулой. Так экстравазальный по происхождению фактор лимфотока (периадвентиция ЛР и кровеносные сосуды – генеральный сегмент ЛСи) становится в составе ЛУ вазальным: периадвентиция преобразуется в межсосудистую лимфоидную ткань гиперплазированной интимы ЛР с функциями регулятора объемной скорости и биофильтра лимфотока (лимфоидный лимфангион – собственный сегмент ЛСи).
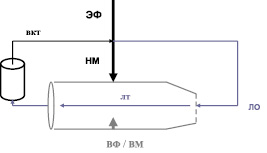
Рис. 4. Регуляция лимфотока (схема): ЭФ, ВФ – экстравазальные и вазальные факторы; НМ, ВМ – наружная и внутренняя манжетки (окружение и стенки) лимфатического русла; ЛО – лимфообразование; лт – лимфоток; вкт – венозный кровоток
Заключение
Лимфоток происходит по двухъярусной цепи сегментов ЛР с постепенно усложняющимся строением. Уровни сегментарной организации лимфотока заложены в устройстве ЛСи:
1) квазисегментарная связь ЛР с артериями (генеральные, периартериальные сегменты) является следствием сегментарного устройства эмбриона и отражает связи ЛР с его окружением – источником экстравазальных факторов лимфотока;
2) складчатая конструкция стенок ЛР (клапаны и межклапанные сегменты) взаимосвязана с колебаниями лимфотока.
Собственные сегменты ЛР во всем их разнообразии организуют базовое, пассивное и дополнительно активное продвижение лимфы от органов к венам. Строение и режим функционирования собственных, межклапанных сегментов ЛР (виды транспорта лимфы) коррелируют с их топографией [5, 7], т.е. – строением генеральных сегментов ЛСи как части сердечно-сосудистой системы и всего организма в целом, его корпоральных сегментов (инфраструктура ЛР).
Структурные основы функционального состояния ЛСи, в т.ч. лимфотока, как и в целом индивида, находятся на субклеточном уровне их организации. Ультраструктурные преобразования начинаются чаще всего с движения так называемых слабых межмолекулярных связей. На макроуровне адекватные структурные изменения организма и его ЛСи обнаруживаются не сразу, но проявляются по мере накопления ультра- и микроструктурных изменений в виде, например, гипертрофии и гиперплазии тех же гладких мышц. Поэтому в последние годы наблюдается интенсификация исследований ЛСи на клеточном и субклеточном, молекулярном уровнях организации [3]. Но для правильной интерпретации результатов таких исследований, их адекватной экстраполяции на макроуровень организации лимфотока требуется знание устройства ЛСи.
Библиографическая ссылка
Петренко В.М. УРОВНИ СЕГМЕНТАРНОЙ ОРГАНИЗАЦИИ ЛИМФОТОКА // Международный журнал прикладных и фундаментальных исследований. 2013. № 10-3. С. 397-400;URL: https://applied-research.ru/en/article/view?id=4216 (дата обращения: 17.05.2026).

