Scientific journal
International Journal of Applied and fundamental research
ISSN 1996-3955
ИФ РИНЦ = 0,556
CONTENT OF BIOGENIC ELEMENTS (NITROGEN AND PHOSPHORUS) IN THE LAKE KENON – THE COOLING POND THERMAL POWER STATION-1
О загрязняющем окружающую среду воздействии ТЭЦ, находящихся в городской черте, пишут многие исследователи. В частности, в работе [6] авторы отмечают, что атмосфера загрязняется пылью, вредными веществами и паром. При мощности станции 1 млн. квт в отходы идут 50 млн. м3 сточных вод, обогащенных 52 т серной кислоты, 26 т хлоридов, 41 т фосфатов, 500 т твердой взвеси и 360 т золы, складирующихся в отвалы.
Озеро Кенон относится к бассейну Верхнего Амура, расположено в черте г. Читы, с 1965 г. используется в качестве водоема-охладителя ТЭЦ-1. Для поддержания уровенного режима озера (653 м) производится подкачка воды из реки Ингода. Работа ТЭЦ-1 оказывает влияние на окружающую среду, в том числе и на экосистему оз. Кенон. Среднегодовая минерализация воды в 1950-х гг. соответствующая 420 мг/л, к настоящему времени увеличилась до 588 мг/л. Состав вод озера из гидрокарбонатно-натриевого трансформировалась в трехкомпонентный: сульфатно-гидрокарбонатно-хлоридный натриево-кальциево-магниевый [8].
Целью данной работы является анализ состояния озера Кенон по концентрации в воде биогенных элементов (азот и фосфор) как важнейших компонентов природных вод, определяющих биологическую продуктивность водных объектов.
Материалы и методы исследования
Отбор проб и определение содержания азота и фосфора проводили общепринятыми в гидрохимии методами [4], ферментативную активность воды определяли по методике [3]. Ферментативная активность водных экосистем указывает на степень гидролиза (распада) высокомолекулярных органических веществ: протеолитическая активность – степень распада белка (в водных экосистемах – это составная часть животных организмов), а амилолитическая – степень распада углеводов (растительных организмов). При распаде органических веществ в воду поступают питательные вещества для жизни и деятельности живых организмов. Неиспользованные продукты распада выпадают в осадок и в последующем они также могут вовлекаться в круговорот веществ. Количество атмосферных осадков и изменения концентрации общего фосфора представлены на основе данных ГУ «Читинский ЦГМС-Р».
Наблюдения проводили по пяти станциям: четыре по периметру и одна в центре озера (рис. 1). На станции «Центр» пробы отбирали в трех горизонтах: поверхность (пов.) – зона прозрачности – дно. По остальным станциям в двух горизонтах: пов. – дно.
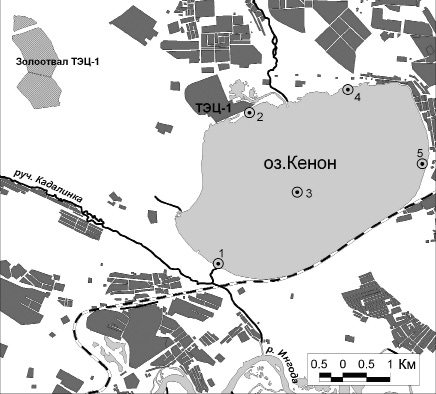
Рис. 1. Карта-схема мест отбора проб воды [6]. Станции: 1 – Усть-Кадалинка, 2 – район сброса ТЭЦ, 3 – центр, 4 – КСК, 5 – Нефтебаза
Результаты исследования и их обсуждение
Общая сумма минеральных форм азота показана на рис. 2. Наибольшее количество ионов аммония, нитритов и нитратов отмечается в июле 2011 г., когда их концентрация изменяется от 0,132 до 0,197 мг/л с наибольшим его содержанием на станции «КСК», наиболее пологий берег озера.
В период осеннего половодья происходит значительное возрастание минеральных форм азота. Из неорганических соединений азота преобладают ионы аммония. В августе 2011 г. береговая линия была насыщена аммонийными формами азота и соответствовала: на ст. Усть-Кадалинка – 0,075 мг/л (пов.) и 0,060 (дно) мг/л, на ст. «Нефтебаза» – 0,010 (пов.) и 0,075 (дно) мг/л. ПДК ионов аммония для рыбохозяйственных водоемов составляет 0,5 мг/л [7]. Повышенная концентрация ионов аммония на данных станциях по сравнению с остальными результатами наблюдений показывает об активных внутриводоемных биохимических процессах.
Повышенное содержание аммонийного азота отмечается и в августе 2010 г., когда в среднем концентрация аммонийных ионов соответствовала 0,110 мг/л за счет его высокого содержания в воде наблюдаемых станций: «ТЭЦ» – 0,090 (пов.) и 0,040 (дно) мг/л; «Центр» – 0,110 (пов.), 0,300 (1,5 м), 0,105 (3,0 м) и 0,085 (дно) мг/л; «Нефтебаза» – 0,040 (пов.) и 0,90 (дно) мг/л.
Минеральные формы азота соответствует следующим соотношениям: 57 %– на ионы аммония, 22 %– на нитраты и 6 %– на нитриты. В исследованиях 1970-х годов [9] данное соотношение приблизительно соответствует нашим результатам: 66 % ионов аммония, 31 %нитратов и 9 % нитритов. Высокое содержание аммонийных форм азота указывает на способность экосистемы к разложению органических веществ. Таким образом, в экосистеме не происходит дальнейшего накопления органических веществ. Повышение содержания аммонийного азота указывает на усиление процессов распада накопившегося за лето органического вещества, подтверждением которого может служить высокая ферментативная активность воды, особенно с июня по сентябрь 2010 г. (рис. 3).
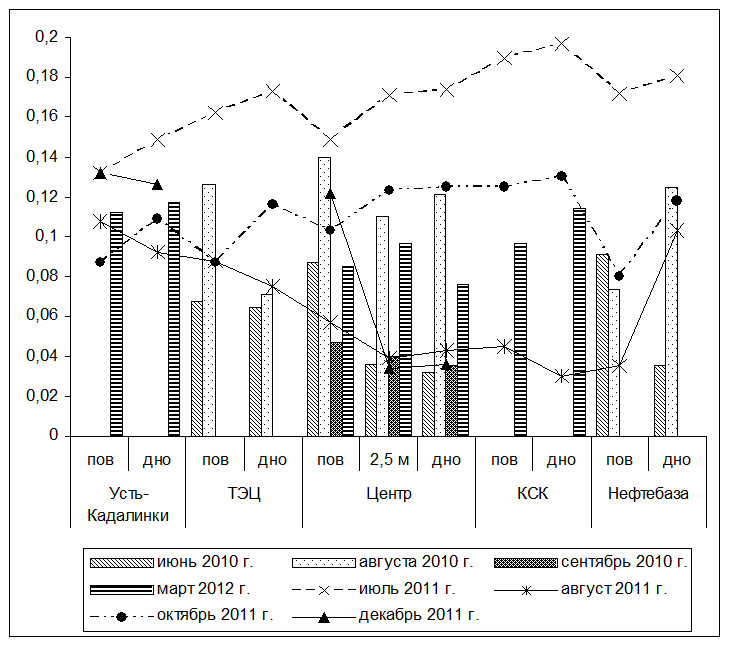
Рис. 2. Концентрация сумм минеральных форм азота в оз. Кенон (мг/л)
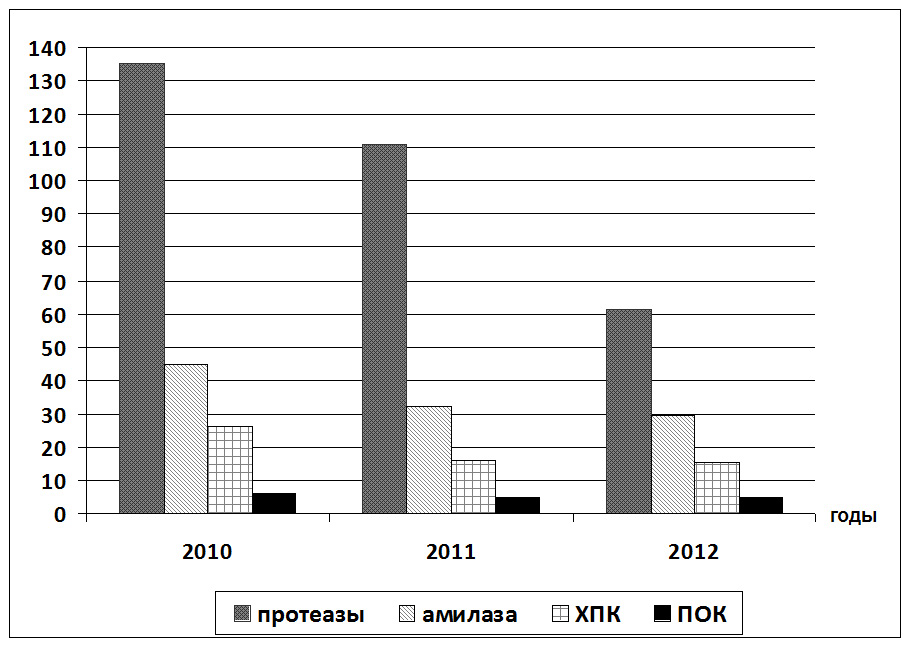
Рис. 3. Ферментативная активность воды (ф. ед. – ферментативные единицы) и окисляемость органических веществ (мг/л) в воде оз. Кенон
Повышенное значение активности амилазы мы отмечаем в августе 2010 г. в районе нефтебазы, в августе 2011 г. – на станции «Усть-Кадалинка». Возможно, это связано с ростом и распадом макрофитов [1]. В 2012 г. за исследованные месяцы (март, май и июнь) в среднем амилолитическая активность не превышает среднего уровня активности за предыдущие годы.
Протеолитическая ферментативная активность в 2011-2012 гг. варьирует от 0 до 251 ф.ед. Почти по всем станциям наблюдений летом и осенью она увеличивается в придонных слоях воды, что связано с процессами биохимического разложения органических веществ. Это указывает на интенсивность процессов седиментации. Отмечаемые по некоторым станциям увеличение значения протеолитической активности поверхностных слоев воды может быть связано с повышенной плотностью фито- и бактериопланктона в данных горизонтах, например, в августе 2011 г. на станции «ТЭЦ», в июне 2010 г. и июль 2011 г. на станции «Нефтебаза». Процессы превышения привноса органических веществ (ОВ) с водосборной площади в летнее время 2010-2012 гг., которые могли иметь место при высоких концентрациях ОВ, принимать во внимание не приходится, так как соотношение перманганатной окисляемости к бихроматной не превышает 40 : в 2010 г. оно составляет в среднем 23 и в 2011-2012 гг. – 31 (рис. 3). Таким образом, органическое вещество в воде оз. Кенон автохтонного происхождения.
В соответствии с требованиями к составу и свойствам воды водоемов в пунктах питьевого водопользования величина ХПК не должна превышать 15 мг/л; в зонах рекреации водных объектов допускается величина ХПК до 30 мгО/л [5]. В оз. Кенон бихроматная окисляемость варьирует от 12,8 до 31,82 мг/л. Высокое содержание бихроматной окисляемости в наших исследованиях коррелирует с высоким содержанием аммонийных ионов. Исходя из представленных значений ХПК, вода озера характеризуется как «грязная» в 2011 г. и в марте 2012 г., «очень грязная» – в 2010 г. В работе [2] отмечены более высокие концентрации органического вещества (бихроматная окисляемость 60-80 мгО/л) в воде оз. Кенон. По результатам наших исследований 2010-2012 гг. данный показатель примерно в 3 раза меньше в виду того, что органическое вещество автохтонного происхождения, а не за счет поступления из водосбора. Это связано с засушливым периодом исследованных лет, когда отмечается пониженный уровень атмосферных осадков и снижение стока из водосборной площади
Содержание органических веществ по перманганатной окисляемости (ПОК) выше 2 мг/л свидетельствует о содержании в воде легко окисляющихся органических соединений. При этом окисляемость перманганатная должна быть не выше 5-7 мг/л для рыбохозяйственных водоемов [5]. По нашим исследованиям 2010 г. среднее значение ПОК находятся в пределах ПДК для данных водоемов.
Анализ данных по атмосферным осадкам, выпавшим на водосборный бассейн оз. Кенон показал, что наибольшее количество осадков наблюдалось за 1997-1998 гг. и 2000-2003 гг. (рис. 4).
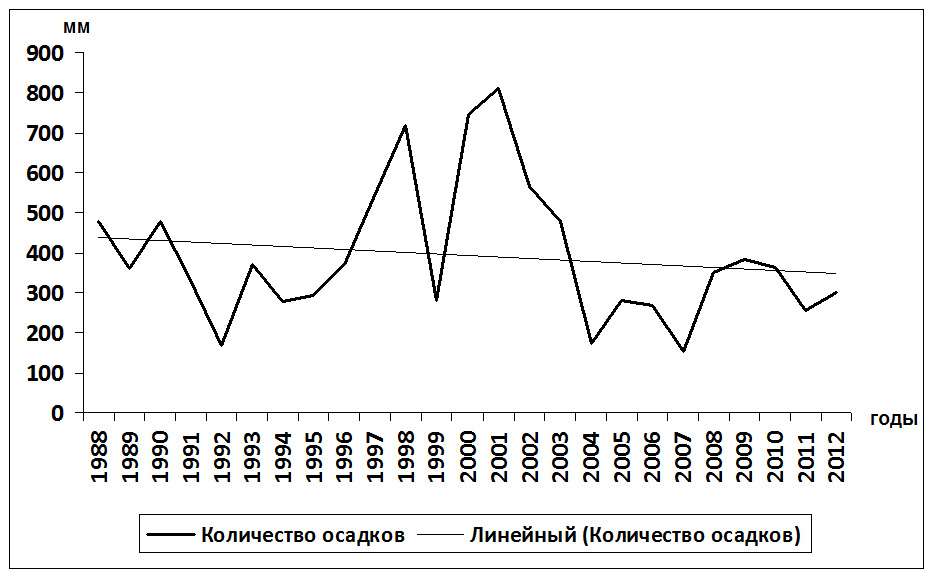
Рис. 4. Количество атмосферных осадков
Сравнение количества атмосферных осадков, выпавших на водосборный бассейн и изменение концентрации общего фосфора в воде оз. Кенон показывает, что высокие содержания их отмечаются в периоды наибольших осадков (рис. 5).
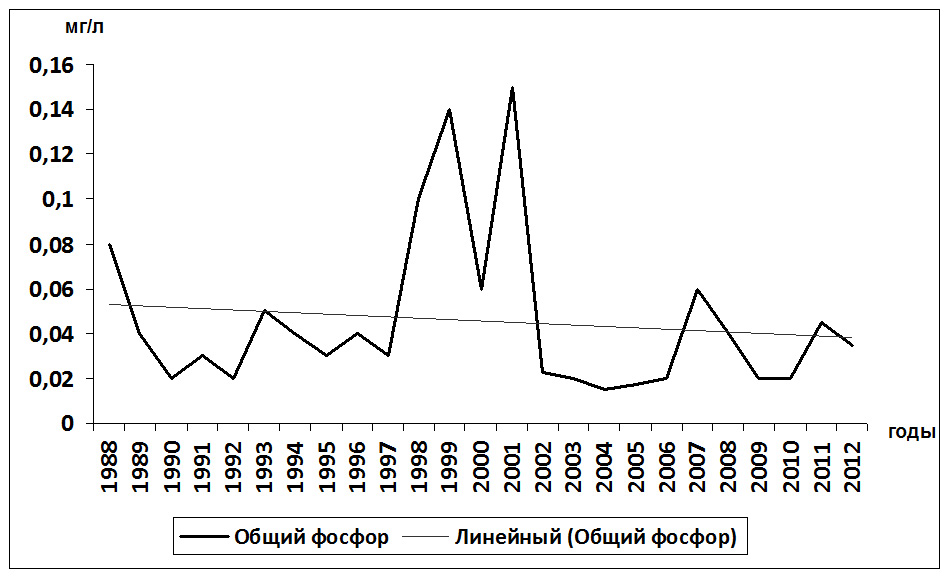
Рис. 5. Изменение концентрации общего фосфора
По исследованиям 70-х годов 20 в. [9] отмечено в воде преобладание почти в два раза органического фосфора, чем минерального (отношение их концентрации составляло 1,9). По нашим исследованиям 2010-2012 гг. данное соотношение соответствовало 1,02, т.е. практически равное содержание как органического, так и минерального фосфора. Таким образом, в равной степени происходят продукционно-деструкционные процессы, что характерно для стабильной экосистемы.
Заключение
Циклические климатические изменения, проявляющиеся как многоводные и маловодные годы, отражаются на экологическом состоянии водоема. В маловодные годы уровень содержания азота и фосфора в водоеме всецело зависит от внутриводоемных биохимических процессов разложения органического вещества. В многоводные годы привнос органических веществ с водосборной площади водоема увеличивает концентрации азота и фосфора, зачастую превышающих ПДК веществ рыбохозяйственных водоемов.
Исследования ферментативной активности воды показывают, что повышение амилолитической и протеолитической активности мы отмечаем в большей степени в придонных и в меньшей степени в поверхностных горизонтах. Следовательно, в придонных слоях воды происходят активнее процессы разложения и образования органических веществ как растительного, так и животного происхождения.
Также нами установлено, что в 2010-2012 гг. органическое вещество в большей степени автохтонного характера, что коррелирует с уровнем осадков, выпавших на водосборную площадь водоема.
Работа выполнена при финансовой поддержке проекта РФФИ № 14-05-98013 р_Сибирь_а.
Библиографическая ссылка
Цыбекмитова Г.Ц. СОДЕРЖАНИЕ БИОГЕННЫХ ЭЛЕМЕНТОВ (АЗОТ И ФОСФОР) В ВОДЕ ОЗЕРА КЕНОН – ВОДОЕМА-ОХЛАДИТЕЛЯ ТЭЦ-1 // Международный журнал прикладных и фундаментальных исследований. 2014. № 7. С. 39-43;URL: https://applied-research.ru/en/article/view?id=5385 (дата обращения: 12.05.2026).

