Scientific journal
International Journal of Applied and fundamental research
ISSN 1996-3955
ИФ РИНЦ = 0,556
OSMOTIC ACTIVITY AND CELLULAR TOXICITY OF UROGRAFIN
Растворы рентгеноконтрастных средств давно известны высокой вероятностью развития острых постинъекционных осложнений: при внутривенных инъекциях они способны вызывать коллаптоидные состояния, анафилактические и анафилактоидные реакции, аритмии, флебиты и нефропатии [2,7], которые могут завершиться смертью пациентов [10]. В связи с этим проблема повышения безопасности рентгеноконтрастных средств остается актуальной и поиск новых более безопасных рентгеноконтрастных средств продолжается. Изменены протоколы и стандарты их применения. Но опасность развития побочных эффектов и осложнений сохраняется [9].
Для повышения безопасности рентгеноконтрастных средств предлагалось сочетать их с антиоксиданами, аскорбиновой кислотой, статинами, аминофиллином и рядом других лекарственных средств. Однако эти попытки не увенчались успехом [9,10,11].
Новым направлением в повышении локальной безопасности лекарств является изменение их физико-химических свойств [1, 3, 4, 13, 15]. Показано, что осмотическая активность, кислотность (щелочность), температура и ряд других физико-химических факторов оказывают существенное влияние на состояние тканей на путях введения антисептических, нестероидных противовоспалительных, химиотерапевтических и противогистаминных средств при их подкожных, внутримышечных и внутривенных инъекциях [8,12,14]. В частности, выявлено, что физико-химическая агрессивность многих современных растворов для инъекций может быть причиной таких локальных повреждений, как сворачивание крови, тромболизис, флебиты, тромбозы вен, кровоподтеки, воспалительные инфильтраты, некрозы, абсцессы в местах инъекций, а также гемолиз и сморщивание эритроцитов при введении в кровь [3, 4, 5, 6, 8].
Самые опасные растворы рентгеноконтрастных средств не являются изотоническими. Более того, некоторые из них имеют чрезмерно высокую гиперосмотическую активность, по величине которой уподобляются гипертоническому раствору натрия хлорида. Поэтому не случайно, что рентгеноконтрастные средства разделяют по осмотической активности на следующие группы: на высокоосмолярные (~ 2000 мосм / кг воды), низкоосмолярные (600 до 800 мОсм / кг воды) и изоосмолярные (290 мосм / кг воды) [11,12].
В связи с этим, изменения размеров и форм эритроцитов, происходящие при взаимодействии крови с растворами рентгеноконтрастных средств при различной их осмотической активности, могли бы пролить свет на данную проблему. Тем не менее, до сих пор отсутствуют убедительные данные о контраст-индуцированных изменениях в клетках крови при взаимодействии их с рентгеноконтрастными средствами [2,9].
Цель исследования – изучение основ осмотической токсичности рентгеноконтрастных средств.
Материалы и методы исследования
Осмотическая активность растворов рентгеноконтрастных средств определена криоскопическим методом с помощью осмометра марки VAPRO 5600 (USA). В работе использован раствор для инъекций урографин, произведенный в Германии – Bayer Schering Pharma AG (Серия МА00IT8) до и после разведения водой для инъекции в 2, 3, 4 и 5 раз.
Мазки крови готовили по стандартной методике и окрашивали азур-эозином по Романовскому-Гимзе. Морфологическое состояние эритроцитов изучено при 1000-кратном иммерсионном увеличении с помощью микроскопа «Leica DM 2500» в мазках крови, приготовленных до и после смешивания и инкубирования in vitro на протяжении 3 минут при температуре 24 – 25 °С порции венозной крови здоровых добровольцев (n=5) с порцией раствора рентгеноконтрастного средства в равных объемах. В качестве контроля использован раствор 0,9 % натрия хлорида с осмотической активностью 306,6 ± 4,5 мОсмоль/л воды. Снимки выполнены с помощью камеры Leica DFC 450. Диаметр эритроцитов измерялся с помощью микрометра МОВ-1-15х на микроскопе БИОЛАМ-ЛОМО при увеличении 40 нм. Кровь для исследования была взята из подкожных вен верхних конечностей взрослых здоровых добровольцев.
С помощью статистической программы BIOSTAT на персональном компьютере Samsung NC 110 (China) вычисляли среднюю арифметическую (M), ошибку средней арифметической (m), коэффициент достоверности (±). Степень различий показателей определяли в каждой серии по отношению к исходным показателям в контрольной серии. Разницу значений считали достоверной при Р ≤ 0,05.
Результаты исследования и их обсуждение
Результаты исследований осмотической активности показали, что качественный раствор 74 % урографина обладает осмотической активностью в пределах 2150,5 ± 12,6 мОсм/л воды (Р < 0,05, n = 5). После его разведения водой для инъекции в 2, в 3, в 4 и в 5 раз осмотическая активность составила соответственно 1080 ± 9,5, 755,0 ± 8,2, 560,0 ± 7,5 и 430 ± 5,5 мОсмоль/л воды.
Исследование мазков крови до и после взаимодействия ее с растворами лекарств показало, что в норме эритроциты здоровых людей имеют симметричную дисковидную форму с диаметром 7, 40 ± 1, 3 мк (Р<0, 05, n=5). При этом большинство эритроцитов имеет равномерную окраску с небольшим просветлением в центре и (рис. 1).
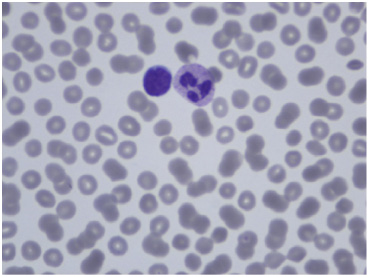
Рис. 1. Микропрепарат венозной крови здорового добровольца (контроль)
Через 3 минуты после начала взаимодействия крови с раствором 0,9 % натрия хлорида in vitro в равных объемах мазок крови демонстрировал ее разведение. При этом диаметр эритроцитов составил 7,48 ± 1, 4 мк (Р < 0,05, n = 5) и большинство эритроцитов имело правильную дисковидную форму и размер (рис. 2).
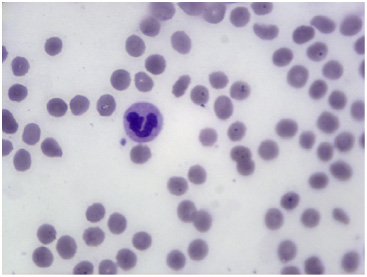
Рис. 2. Микропрепарат венозной крови здорового добровольца через 3 минуты после начала взаимодействия крови с раствором 0,9 % натрия хлорида в равных объемах in vitro при температуре 24 – 25°С.
Другие результаты получены после взаимодействия крови с рентгеноконтрастным средством. Показано, что рентгеноконтрастные средства, имеющие высокую осмотическую активность, изменяют размер и форму эритроцитов. Причем, степень морфологических изменений эритроцитов зависела от осмотической активности растворов и была тем выше, чем более высокой была гиперосмотическая активность лекарства.
Наиболее значительные изменения в размерах и формах эритроцитов наступали под действием раствора 76 % урографина, имеющего самую высокую осмотическую активность, а именно – 2150 мОсмоль/л воды. (рис. 3).
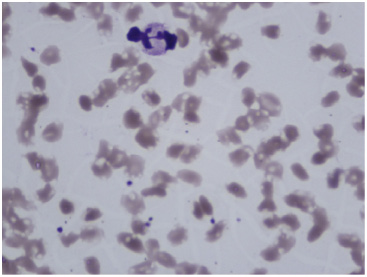
Рис. 3. Микропрепарат венозной крови здорового добровольца через 3 минуты после взаимодействия ее с раствором 76 % урографина при осмотической активности 2150 мОсмоль/л воды
При этом эритроциты теряли симметричную дисковидную форму, уменьшались в размерах, выглядели сморщенными, в них появлялись вакуоли, занимающие до 3/4 площади цитоплазмы. Причем, форма значительной части эритроцитов в мазках напоминала собой шестеренки, а диаметр эритроцитов уменьшился до 7,0 ± 1,6 мк (Р < 0,05, n = 5).
Этот же раствор урографина после его разведения водой в 3 раза приобретал осмотическую активность, равную 755 мОсмоль/л воды. Через 3 минуты взаимодействия крови с таким раствором препарата диаметр эритроцитов составил в среднем 7,2 ± 1,5 мк (Р < 0, 05, n = 5). При этом в эритроцитах происходило исчезновение центрального просветления, все кровяные клетки приобрели форму шестеренок и имели зазубренные контуры и «шипики» рис. 4).
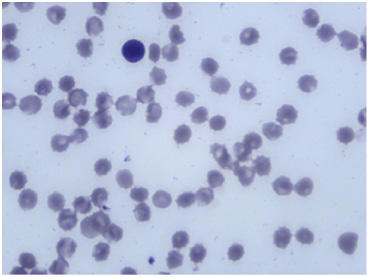
Рис. 4. Микропрепарат венозной крови здорового добровольца через 3 минуты после взаимодействия с раствором урографина, разведенного водой в 3 раза до осмотической активности 755 мОсм/л воды
Более значительное разведение урографина практически полностью лишало его острой клеточной токсичности. Так, при разведении раствора 76 % урографина водой в 5 раз препарат переставал изменять форум и размер эритроцитов. Результаты показали, что через 3 минуты после начала взаимодействия порции крови здорового добровольца с равным объемом раствора 15 % урографина, имеющего осмотическую активность 430,0 мОсмоль/л воды, эритроциты имели диаметр 7,3 ± 1,2 мк (Р<0, 05, n=5), а их форма не имела отличия от эритроцитов крови после взаимодействия ее с раствором 0,9 % натрия хлорида в аналогичных условиях (рис. 5).
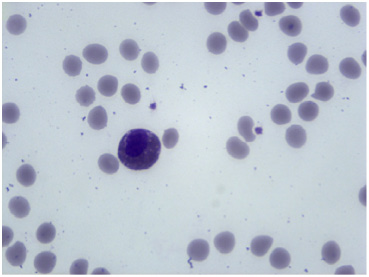
Рис. 5. Микропрепарат венозной крови здорового добровольца через 3 минуты после взаимодействия с раствором урографина, разведенного в 5 раз водой для инъекции до придания осмотической активности 430 мОсмоль/л воды
Следовательно, растворы урографина, обладающие чрезмерно высокой осмотической активностью, способны изменять форму и размер эритроцитов крови человека при физическом взаимодействии друг с другом в равных соотношениях. Происходящие в эритроцитах изменения могут быть охарактеризованы таким термином, как сморщивание. Можно предположить, что это происходит, из-за обезвоживания красных клеток крови, возникающего под влиянием гиперосмотической активности растворов урографина.
Следовательно, полученные нами данные подтвердили результаты предыдущих исследований, показавших увеличение степени повреждающего действия растворов нестероидных противовоспалительных, химиотерапевтических и анестезирующих лекарственных средств с увеличением их концентрации, осмотической активности и длительности взаимодействия [17].
Таким образом, введение в кровь растворов урографина, имеющих чрезмерно высокую гиперосмотическую активность, способно привести к контраст-индуцированным изменениям в крови человека, степень которых прямо пропорциональна их осмотической активности. Более того, повреждение эритроцитов имеет не столько контраст-индуцированную, сколько дегидратирующую природу возникновения.
Полученные данные указывают на то, что современные фармакопейные требования, предъявляемые к качеству лекарств, допускают законный дефект фармацевтического производства лекарств, который проявляется производством растворов для инъекций с суммарной концентрацией ингредиентов более 10 %. Наличие такой высокой концентрации ингредиентов придает всем растворам лекарственных средств чрезмерно высокую гиперосмотическую активность и локальную токсичность. Поэтому растворы 67 % и 76 % урографина являются ГИПЕРТОНИЧЕСКИМИ, а точнее – ГИПЕРОСМОТИЧЕСКИМИ. В связи с этим внутривенные инъекции этих препаратов могут вызвать дегидратацию клеток крови, эндотелия кровеносных сосудов, а также многих других клеток организма, включая клетки коры головного мозга. В последнем случае возможно развитие гиперосмотической комы. Особенно велика такая опасность у больных с сахарным диабетом или с иными болезнями и состояниями, повышающими осмотическую активность плазмы крови.
В связи с этим, разведение растворов 76 % урографина в 5 раз водой для инъекций нормализует осмотическую активность лекарства (уменьшает ее слабого гиперосмотичсекого уровня, равного 430 мОсмоль/л воды) и устраняет его клеточную токсичность. Поэтому разведение раствора 76 % урографина и других рентгеноконтрастных средств водой для инъекции вплоть до придания им изоосмотической активности может рассматриваться в роли универсального способа их фармацевтической коррекции (фармдезинтоксикации), поскольку устраняет дефект фармацевтического производства, повышает качество лекарства, устраняет его неспецифическую фармакологическую активность, лежащую в основе клеточной токсичности.
Поэтому перед введением в кровь разведению раствора 76 % урографина в 5 раз водой для инъекций нет альтернативы.
Библиографическая ссылка
Ураков А.Л., Ураков А.Л., Лукоянов И.А. ОСМОТИЧЕСКАЯ АКТИВНОСТЬ И КЛЕТОЧНАЯ ТОКСИЧНОСТЬ УРОГРАФИНА // Международный журнал прикладных и фундаментальных исследований. 2014. № 8-4. С. 65-68;URL: https://applied-research.ru/en/article/view?id=5697 (дата обращения: 16.05.2026).

