Scientific journal
International Journal of Applied and fundamental research
ISSN 1996-3955
ИФ РИНЦ = 0,556
REGARDING THE FEATURES OF THE PROBLEM OF ATOMIC PHYSICS, THE ROLE AND IMPORTANCE OF NUCLEAR INTERACTIONS OF ELEMNTARY PARTICLES
При изучении квантовой теории проблема атома водорода играет такую же роль, как проблема движения планет в классической механике. Естественно проблема атома водорода первоначально была очень сложной, сейчас когда прошло много времени, теория атома развивается очень интенсивно мы можем говорить как о решенной проблеме. Это аналогично например решению очень сложнейшей задачи, когда не знаешь решение задачи проблема кажется очень сложной, когда знаешь ход решение задачи все становится ясно. Все гениальное оказывается очень простым, но в то время проблема атома водорода волновало умы всех ученых того времени, это задача все таки была решена благодаря работам Н. Бора, Э. Резерфорда, А. Эйнштейна, М. Планка.
Все окружающие нас тела в конечном итоге построены из мельчайщих частиц, называемых атомами. Атомы определенным образом соединяются в молекулы и упорядоченные обьединения атомов или молекул – кристаллы, соединения маленьких кристалликов образуют скалы и другие горные породы, таким образом из атомов и молекул строятся всевозможные тела.
Следовательно, изучение строения атомов – первый шаг к изучению структуры вещества. Именно сделать первый шаг бывает всегда очень тяжело. Поэтому не удивительно, что в конце девятнадцатого и начале двадцатого веков различных гипотез насчет атомных структур было очень много. Одной из первых моделей была модель атома Томсона. Хотя по расчетам этой модели размеры атомы совпадают с размерами газокинетических размеров атома, она в истории физики осталась как историческая модель. Сейчас известно, что строение атома напоминает нам Солнечную систему, где все планеты движутся вокруг Солнца по круговым орбитам. Диаметры орбит электронов согласно эксперименту составляют величины около одной стомиллионной доли сантиметра.Вещество образовано различными комбинациями 92 химических элементов, таких, как водород, кислород, железо и т.д. Соответственно имеется 92 вида атомов: атом водорода, атом кислорода и т.д. Среди них самый простой – атом водорода, в котором вокруг ядра обращается единственный электрон.
В данное время известно, что для устранения недостатка планетарной модели датский физик Нильс Бор ввел в нее ограничения, получивших название квантовых условий, ограничениям подчиняются орбиты, по которым электрон может вращаться вокруг ядра [3–5].
Сделать такой вывод в начале двадцатого века было великим подвигом, так как в то время хорошо развивалась только классическая теория, а эти выводы находились в противоречии с теорией классической механики.
Оказалось, что условие стабильности дебройлевских орбитальных волн в точности совпадает с боровскими квантовыми условиями. Это примирило с последними почти всех критиков, ранее сетовавших на неясность физического смысла квантования орбит электрона в атоме [3, 4].
По мысли Бора, устойчивы только орбиты, удовлетворяющие квантовым условиям, при движении по устойчивой орбите электрон, несмотря на колебания заряда, не излучает элетромагнитные волны, и он может пребывать на орбите сколь угодно долго.Излучение же ( или поглощение) света атомом происходит при перескоках электрона с одной устойчивой орбиты на другую, при перескоке электрон отдает ( или поглощает) порцию энергии – квант. Такая модель нам известна как модель атома Бора.
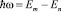
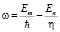 .
.
Принятая Бором картина испускания и поглощения света атомами согласуется с учением Эйнштейна о фотонах, также формулой Планка об электромагнитном излучении отдельных порций энергии, т.е. энергии фотонов. Эти формулы Планка полностью и досконально обьясняют все законы теплового излучения.
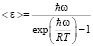
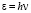
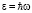
Постулаты Бора нашли экспериментальное подтверждение в опытах Франка и Герца при упругом взаимодействий свободных электронов с атомами ртути.
Своей моделью Бор прекрасно разьяснил взаимосвязь между стабильностью атомов и тайной рождения света. Но физический смысл боровской модели был непонятен. Основное требование Бора о том, чтобы движущийся по стабильной орбите электрон, несмотря на колебания заряда, не излучал электромагнитные волны, выглядело как произвольное утверждение, противоречащее классической электродинамике. Особенно раздраженные критики Бора говорили, про его обьяснение о стабильности атома водорода. Спасли боровскую модель от упреков в непонятности дебройлевские волны и естественно квантовая механика.
Де Бройль постулировал, что элементарные частицы (из которых, как из материала, в конечном итоге строится все вещество), так же как и свет, имеет двойственную природу. Теперь конечно известно, что любой микрочастице сопоставляется волна с частотой, пропорциональной энергии частицы.
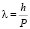
Энергия микрообьекта, рассматриваемого как корпускула, и частота того же обьекта, рассматриваемого как волна, связаны таким же соотношением, каким, по Эйнштейну, связана энергия фотона с частотой последнего. В этом сущность дебройлевской идеи о волнах вещества.Здесь можно добавить что корпускулярно – волновой дуализм в движении микрочастиц относиться к кругу явлений, в которых проявляются кванто-механические закономерности. Построение модели такого движения привело к формулировке уравнения Шредингера, которое является новым уравнением физики и не может быть «выведено» из ранее известных уравнений.
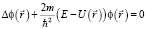
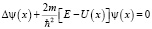
Однако в физике давно было известно, что любые волны описываются соответствующим волновым уравнением. Исторически и логически уравнение Шредингера возникло как уравнение для волн де Бройля. Такой подход к уравнению Шредингера является наиболее простым и естественным в рамках индуктивной формулировки физической модели в курсе общей физики. Именно с рассмотрения атома водорода и простейших случаев движения микрочастиц следует рассматривать лишь как подготовку к кванто-механическому анализу более реальных случаев движения частиц в микромире.
Первое экспериментальное подтверждение гипотезы де Бройля получено в 1927 году (после создания квантовой механики) в опытах американских физиков Дэвиссона и Джермера, установивших, что электроны дифрагируют на кристалл как волны с длиной волны, определяемой соотношением де Бройля [4, 5].
Гениальность Нильса Бора заключается в том, что он решил теорию атома водорода нестандартным путем, заявляя о двух своих постулатах, которые в корне противоречили известной классической теории. Но в конце концов эта безумная и нестандартная теория оказалась справедливой, что подтвердилось позднее многочисленными экспериментами крупнейших ученых в начале двадцатого века. Вот в чем заключается гениальность теории атомной модели Нильса Бора!
Проблема атома водорода допускает строгое решение, а результаты ее решения можно непосредственно сравнить с опытом, все правила здесь четко определены, никаких сил трения нет,а следствия настолько хорошо согласуются с экспериментальными результатами, что нам ничего не остается делать, как поверить в их истинность. В этом смысле анализ атома водорода служит проверкой всей квантовой физики. Каждую деталь этой проблемы можно рассчитать и сравнить с опытными данными. Некоторые фундаментальные открытия наших дней были сделаны на основании анализа энергетических уровней именно атома водорода. И некоторые чрезвычайно точные совпадения между теорией и экспериментом были получены именно тогда, когда предсказания квантовой теории сравнивались с наблюдениями за тем же водородным атомом [1–3].
Информация, которую мы получаем при анализе строения атома водорода, легко извлекается с помощью квантовой теории, и вместе с тем она представляет интерес для атомной физики. Квантовая теория, чтобы можно было считать ее согласованной и полной, обязана обьяснить результаты любого опыта, проведенного с атомом водорода. В этом же смысле понятие, скажем, о стуле, – т.е. совокупность наших знаний о свойствах этого предмета, включая его жесткость, цвет, присутствие в комнате даже в том случае, когда мы не смотрим на него, и т.д., – обязано содержать всю возможную опытную информацию о стуле.
В данном случае можно подвести некоторые итоги вышесказанным суждениям. Выше говорилось, что вследствие двойственности природы электрона, также в связи с дуализмом волна – частица сложные вопросы относятся только к внутриатомному миру и не имеют отношение к окружающей нас макроскопической действительности. Иначе говоря, в макромире по –прежнему эффективна ньютонова механика.
Квантовая механика продемонстрировала свою мощь и добилась огромных успехов при решении задач внутриатомного мира, это стимулировала ее применение к анализу устройства атомных ядер. Задачи атомной физики,теория взаимодействия элементарных частиц описываются квантовой механикой. Квантовая теория поля, до настоящего времени продолжает быть крупной теорией современности, занимающихся элементарными частицами, так как является единственным в своем роде, незаменимым инструментом построения теории элементарных частиц.
Библиографическая ссылка
Абекова Ж.А., Оралбаев А.Б., Ермаханов М.Н., Космуратова А.Т. ОБ ОСОБЕННОСТЯХ ЗАДАЧИ АТОМНОЙ ФИЗИКИ, О РОЛИ И ЗНАЧЕНИИ АТОМНЫХ ВЗАИМОДЕЙСТВИЙ ЭЛЕМЕНТАРНЫХ ЧАСТИЦ // Международный журнал прикладных и фундаментальных исследований. 2014. № 11-3. С. 369-371;URL: https://applied-research.ru/en/article/view?id=6135 (дата обращения: 10.05.2026).

