Введение
Лечение и профилактика клинических проявлений аллергии является одним из актуальных вопросов современной медицины, которые имеют большое социальное значение.
Одним из проявлений аллергии являются дерматозы. Наиболее распространенными в общей структуре аллергических болезней кожи является атопический дерматит (АтД) и хроническая крапивница. Из Клинические проявления аллергодерматозов характеризуется различным набором и сочетанием первичных морфологических элементов (папула, везикула, волдырь, пузырь и т.д.). Основным симптомом, объединяющим эту группу заболеваний, является кожный зуд.
В настоящее время в Государственном реестре ЛС зарегистрировано 173 наименованияантигистаминных препаратов из 26 стран. Из них 64% составляют отечественные антигистаминные ЛС, представленные твердыми (70,6 %), жидкими (24,5 %), газообразными (2,6 %) и мягкими (2,3 %) лекарственными формами [5]. Учитывая небольшой процент мягких лекарственных форм на фармацевтическом рынке, разработка новых дерматологических антиаллергических лекарственных форм является актуальной. В качестве объекта исследования нами был выбран димебон.
Димебон - оригинальный антигистамин-ный препарат синтезирован в МГУ им. М. В. Ломоносова. Его фармакологическое действие обусловлено блокированием Н1 -гистаминовых рецепторов, а также частично м-холино- и се-ротониновых рецепторов. Также оказывает местноанестезирующее и седативное действие, и обладает противоанафилактической активностью, антиаритмическим действием [8]. Препарат рекомендован многими авторами для лечения аллергических заболеваний и аллергических осложнений, вызванных лекарственными средствами, зудящих дерматозов, косметологических дерматитов, лучевых и ожоговых поражений кожи, аллергических и воспалительных заболеваниях век, конъюнктивитах; поллинозах, крапивнице, сенной лихорадки, пищевой и косметической аллергии, лекарственной аллергии, ангионевротическом отеке, атопическом дерматите, диффузном дерматите; при симптоматических аллергических реакциях: отек, зуд, экзема; реакции, связанные с укусами насекомых [2, 3, 4, 6, 7, 9]. Учитывая опыт применения димебона, мы остановили свой выбор на таких мягких лекарственных формах, как гель и крем.
одним из важных аспектов исследования при конструировании гелей и кремов является выбор доминирующего вспомогательного вещества - основы-носителя. Нами для исследований был использован следующий набор основ-носителей:
Иолиэтиленгликоль 400, 4000. Полимеры этиленгликоля. Растворим в воде, а также во многих органических растворителях. Нетоксичен [1].
Карбопол-940. Группа карбоксиакриловых и карбоксивиниловых полимеров. Хорошо растворяется в воде, легко смешивается с любыми активными ингредиентами, не расслаивается, не комкуется, не меняет цвет [1].
Коллаген. Биоадекватный полимер, представляющий собой белок соединительной ткани. Нетоксичен, всасывается и полностью утилизируется организмом, хорошо высвобождает лекарственные вещества, обладает сорбционной способностью, репаративными свойствами [1].
Хитозан. Аминосахарид. обладает антибактериальным, противогрибковым и антивирусными, а также противовоспалительными свойствами, способствует регенерации тканей [1].
Метилцеллюлоза. Эфир целлюлозы. Не имеет раздражающего и сенсибилизирующего действия, безвреден, обладает мягкой осмотической активностью и используется в мазях для заживления ран [1].
Биофармацевтические исследования in vitro.
Диализ в среде 0,01 М HCl
Навеску 0,6 г. каждой мягкой лекарственной формы на различных основах (карбопол, хитозан, метилцеллюлоза (МЦ), полиэти-ленгликоль (ИЭГ), коллаген) помещали на целлофановую мембрану. В 5 диализаторов, соответствующих каждой основе, наливали по 30 мл 0,01 М HCl. Проводили диализ, отбирав пробы по 5 мл через 20, 40, 50, 70 и 90 минут соответственно. Измеряли оптическую плотность на СФ-2000 при длине волны 270 ± 2 нм в кювете с толщиной слоя 10 мм. Т.к. в процессе исследования получился большой разброс показателей данной величины, то в целях получения более достоверных результатов, было проведено разведение проб диализа 0,01 М Hd в соотношении 1:1.
Параллельно, согласно методике при идентичных условиях, провели определение оптической плотности каждой из основ без действующего вещества также в среде 0,01 М HCl. Спектрофотометрическое исследование основ показало, что определенную оптическую плотность имеет основа с хитозаном. Остальные же основы (коллаген, ПЭГ, МЦ, карбопол) не обладают оптическими плотностями, влияющими на результаты исследований. В связи с чем, проводили расчеты количества высвобождаемого действующего вещества с учетом показателя оптической плотности основы с хитозаном в данных условиях. Результаты представлены на рис. 1.
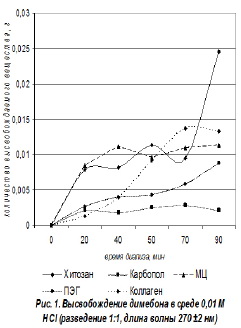
Как видно из рис. 1, наибольшее высвобождение димебона обеспечивает основа с хи-тозаном, достигая максимума (0,02453 г.), по сравнению с другими основами, за 90 минут диализа в среде 0,01 М HCl. Основа с метил-целлюлозой (МЦ) обеспечивает максимальное высвобождение действующего вещества (0,01133 г.) за 90 мин диализа. Что касается основ с карбополом и полиэтиленгликолем (ПЭГ) - диализ происходит равномерный, постепенный, но без достижения желаемых нами результатов. Высвобождение димебо-на из основы с коллагеном происходит медленнее, достигая своего пика в точке 70 мин (0,01372 г.).
В связи с этим, из рис. 1 можно сделать вывод, что несмотря на самое медленное, по сравнению с другими основами, высвобождение димебона из основы с хитозаном, высвобождение из данной основы происходит в 2 и более раза полнее (больше).
2. Диализ в среде 0,01 МNaOH.
Навеску 0,6 г. каждой мягкой лекарственной формы на различных основах (карбопол, хитозан, метилцеллюлоза (МЦ), полиэтилен-гликоль (ПЭГ), коллаген) помещали на целлофановую мембрану. В 5 диализаторов, соответствующих каждой основе, наливали по 30 мл 0,01 М HCl. Проводили диализ, отбирав пробы по 5 мл через 20, 40, 50, 70 и 90 минут соответственно. Измеряли оптическую плотность на СФ-2000 при длине волны 275 ± 2 нм и 288 ± 2 нм (фармакопейная статья на димебон предполагает наличие двух максимумов поглощения) в кювете с толщиной слоя 10 мм.
Параллельно, согласно методике при идентичных условиях, провели определение оптической плотности каждой из основ без действующего вещества также в среде 0,01 М
NaOH. Спектрофотометрическое исследование основ показало, что определенную оптическую плотность имеет хитозан. Остальные же основы (коллаген, ПЭГ, МЦ, карбопол) в среде 0,01 М NaOH не обладают оптическими плотностями, которые могут повлиять на результаты исследования. В связи с чем, проводили расчеты количества высвобождаемого действующего вещества с учетом показателя оптической плотности основы с хитозаном в данных условиях. Результаты представлены на рис.2. и рис. 3.
Сравнивая рис. 2 и 3, видно, что показатель количества высвобождаемого димебона, рассчитанный при спектрофотометрическом определении с длиной волны 275 ± 2 нм, больше, чем показатель, рассчитанный при измерении с длиной волны 288 ± 2 нм. Можно сделать вывод, что при спектрофотометрическом определении высвобождаемого димебона из основ в условиях 0,01 М NaOH, более точное при определении с длиной волны 275 ± 2 нм. Соответственно, представляется рациональным руководствоваться показателями рис. 2.
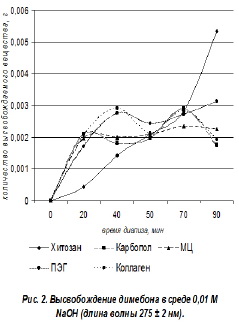
Анализируя рис. 2, можно сказать, что основа с хитозаном обеспечивает более полное высвобождение действующего вещества (0,005345 г.) в данных условиях к 90 минутам диализа. Что касается других основ (коллаген, карбопол, полиэтиленгликоль и микроцеллюлоза), то диализ происходит более равномерный, достигая своего пика в точке 70 мин). Следует отметить, что высвобождение диме-бона из основ с коллагеном, карбополом, ме-тилцеллюлозой, полиэтиленгликолем в среде 0,01 М NaOH, как и в среде 0,01 М HCl, в 2 и более раза меньше, чем высвобождение из основы с хитозаноме
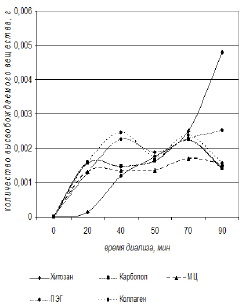
Также на рис. 2 и 3 видно, что высвобождение димебона из представленных нами основ в среде 0,01 М NaOH менее полное по сравнению с данными показателями в среде 0,01 М HCl (рис.1, 2)
Выводы
Таким образом, нами в качестве оптимальной основы выбран хитозан, который обеспечивает максимально возможное высвобождение димебона, имеет элленгацию и является достаточно технологичной основой, т.к. получение крема на этой основе не длительно и не сложно.
Список литературы
1. http://ru.wikipedia.org/
2. Доклиническое изучение безвредности антигистаминного препарата димебон. М.И. Голубева, Л.Ф. Шашкина, В.А. Пройнова и др. // Фармакология и токсикология, 1985, №3, C.114-119.
3. Ильюченок Т. И., Матвеева И. А. Димебон - новый антигистаминный препарат // Новые лек. препараты. - 1989. - №4. С.12-16.
4. Киселева Э.Э., Захаревский А.С., Никифорова И.Н. Противоаллергическая активность и механизм действия производных гамма-карболина // Фармакология и токсикология. - 1990. - Т. 53, №3. - С. 22-24.
5. Маркетинговые исследования рынка антигистаминных лекарственных средств / Ю.В. Ханин, Т.И. Кабакова, С.А. Михайлова, А.Л. Захарян, Х.Н. Насрулаева // Человек и лекарство Тез. докл. 12 Рос. нац. конгр. 18-2 апр. 2005 г. М., 2005 - С. 810.
6. Матвеева И.А. О действии димебона на гистаминовые рецепторы. // Фармакология и токсикология. - 1983. - №4. - С. 27-29.
7. Противоаллергические свойства диме-бона, фенкарола и кетотифена при сенсибилизации пыльцевой амброзии. Галенко-Ярошевский П.А., Шадурский К.С., Ильюченок Т.И. и др. // Фармакология и токсикология. - 1984. - №3. - С. 75-78.
8. Сравнительная характеристика антиаритмической эффективности фенкарола и димебона при нейрогенной фибрилляции
предсердий. П. А. Галенко-Ярошевский, И.Л. Чередник, В.В. Барташевич и др. // Бюл. Экспер. Биологии и медицины. - 1997. -
Т. 124, №7. - C. 81-85.
9. Шадурский К.С., Матвеева И.А., Ильюченок Т.Ю. Лечебные и защитные свойства димебона при ожоговой болезни. // Фармакология и токсикология. - 1983. - №5. - С. 90-92.

