Scientific journal
International Journal of Applied and fundamental research
ISSN 1996-3955
ИФ РИНЦ = 0,556
SOME REGULARITIES OF PHASEFORMATION CHARACTER AND THERMODYNAMIC FUNCTIONS OF FORMATION OF TERNARY THALLIUM CHALCOSTIBNITES AND CHALCOBISMUTITES
Халькостибниты и хальковисмутиты таллия относятся к числу важных функциональных материалов. Еще в 70-х годах прошлого века были изучены [19] оптические свойства TlSbS2 и показана перспективность его для создания малоинерционных приемников импульсов излучения в видимой области спектра. Результаты дальнейших исследований [24, 25, 34, 35] показали, что тиостибниты таллия Tl3SbS3, TlSbS2, Tl3SbS4 и TlSb3S5, а также TlBiS2 обладают интересными фотоэлектрическими и акустооптическими свойствами и являются перспективными для применения в качестве соответствующих материалов. Соединение Tl3SbS3 [31] считается перспективным материалом в качестве детектора ядерного и g-излучения. В [27] показано, что TlSbSе2 проявляет эффект переключения с напряжением.
Тройные соединения, образующиеся в системах Tl-Bi-Se, Tl-Sb-Te и Tl-Bi-Te, являются объектами многочисленных исследований в связи с их перспективностью использования в качестве низкоомных полупроводников с высокими термоэлектрическими показателями [20, 26, 28, 29, 33]. Наилучшие термоэлектрические свойства демонстрирует соединение Tl9BiTe6 [37, 38].
Соединения типа TlBVX2 (где BV-Sb, Bi; X-S, Se, Te) являются перспективными кандидатами на роль топологических изоляторов [14, 21-23, 30, 32]. Отличительной особенностью данных материалов является то, что они, будучи изоляторами в объёме, обладают бесщелевыми состояниями на поверхности, благодаря которым возможно протекание спин-поляризованного тока практически без потерь энергии. Такие необычные свойства топологических изоляторов дают потенциальную возможность для их использования в новых спинтронных и магнетоэлектрических приборах, а также для создания квантовых компьютеров.
Как следует из вышеуказанного, халькостибниты и хальковисмутиды таллия являются перспективными материалами и разработка физико-химических основ получения этих соединений и многокомпонентных фаз на их основе актуально.
Разработка методов направленного синтеза многокомпонентных фаз, как правило, связана с исследованиями фазовых равновесий и термодинамических свойств в соответствующих системах.
Фазовые равновесия в тройных системах Tl-Sb-Te [1], Tl-Bi-S [4,5], Tl-Bi-Se [3,6] изучены достаточно подробно. Построены фазовые диаграммы этих систем и определены термодинамические свойства обнаруженных тройных фаз. Литературные сведения относительно этих систем не вызывают особого сомнения и достаточно корректны, что нельзя сказать относительно тройных систем Tl-Sb-S(Se) и Tl-Bi-Te. Анализ имеющихся данных показывает их противоречивость и недостаточность для установления полной взаимосогласованной картины фазовых равновесий в указанных системах.
Учитывая это, нами предприняты повторные комплексные исследования фазовых равновесий и термодинамических свойств этих систем [2, 9–13]. Определены области первичной кристаллизации и области гомогенности обнаруженных тройных фаз. Построены фазовые диаграммы некоторых политермических разрезов, изотермических сечений при 400К и проекции поверхности ликвидуса. Установлены типы и координаты нон- и моновариантных равновесий. Из измерений ЭДС вычислены парциальные и интегральные термодинамические функции тройных фаз.
Наличие экспериментальных данных по всем системам Tl-BV-X (BV-Sb, Bi; X-S, Se, Te) позволяет провести сравнительный анализ их фазовых диаграмм (рисунок) и термодинамических функций образования промежуточных фаз в этих системах (таблица).
Основной характеристикой фазообразования в системах Tl-BV-X является число промежуточных фаз, которые в указанных системах изменяются следующим образом (рис.1): Tl-Sb-S (6), Tl-Sb-Se (4), Tl-Sb-Te (2), Tl-Bi-S (2), Tl-Bi-Se (2), Tl-Bi-Te (2). Как видно, в сурьмасодержащих системах число промежуточных фаз при переходе от сульфидов к селенидам и далее к теллуридам постепенно уменьшается, а в висмут содержащих системах остается постоянным.
Как известно [16], оба 6s2-электрона атома таллия подвержены сильному эффекту проникновения через двойной экран d- и f-электронных облаков. В результате затрудняется участие s-электронов в образовании химических связей. Поэтому у таллия валентным часто является 6р-электрон, а степень окисления + 1 более стабильна, чем характеристическая + 3. Это сказывается в закономерном уменьшении термической и термодинамической устойчивости халькогенидов таллия в сульфидах, селенидах и теллуридах с увеличением степени окисления таллия [36].
Наличие заполненных предвнешних (n-1) d (для Bi еще (n-2)f) – уровней обуславливают уменьшение устойчивости высшей степени окисления (+5) у сурьмы и висмута. В силу этого все халькогениды 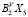 (BV-Sb, Bi; X-S, Se, Te) являются неустойчивыми. Термодинамическая стабильность халькогенидов
(BV-Sb, Bi; X-S, Se, Te) являются неустойчивыми. Термодинамическая стабильность халькогенидов 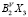 , как следовало ожидать по разностям электроотрицательностей, при переходе S → Se → Te уменьшается, а при переходе Sb → Bi увеличивается [15].
, как следовало ожидать по разностям электроотрицательностей, при переходе S → Se → Te уменьшается, а при переходе Sb → Bi увеличивается [15].
Так как в двойных системах Tl(BV)-X более устойчивыми являются соединения Tl2X и 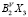 во всех системах Tl-BV-X разрезы Tl2X-
во всех системах Tl-BV-X разрезы Tl2X-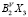 являются практически квазибинарными и характеризуются образованием промежуточных соединений. Все образующиеся тройные фазы подчиняются закону простых кратных отношений. Во всех системах Tl2X-
являются практически квазибинарными и характеризуются образованием промежуточных соединений. Все образующиеся тройные фазы подчиняются закону простых кратных отношений. Во всех системах Tl2X-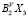 при эквимолярном соотношении исходных компонентов образуются соединения состава TlBVX2 . С увеличением различия в кислотно-основных свойствах между Tl2X и Sb2X3 происходит заметное усложнение химического взаимодействия в системах, которое сказывается в закономерном увеличении количества образующихся соединений: Tl3SbS3, TlSbS2, TlSb3S5, TlSb5S8 в системе Tl2S-Sb2S3; Tl9SbSe6, Tl3SbSe3, TlSbSe2, TlSb3Se5 в системе Tl2Se-Sb2Se3; Tl9SbTe6, TlSbTe2 в системе Tl2Te-Sb2Te3.
при эквимолярном соотношении исходных компонентов образуются соединения состава TlBVX2 . С увеличением различия в кислотно-основных свойствах между Tl2X и Sb2X3 происходит заметное усложнение химического взаимодействия в системах, которое сказывается в закономерном увеличении количества образующихся соединений: Tl3SbS3, TlSbS2, TlSb3S5, TlSb5S8 в системе Tl2S-Sb2S3; Tl9SbSe6, Tl3SbSe3, TlSbSe2, TlSb3Se5 в системе Tl2Se-Sb2Se3; Tl9SbTe6, TlSbTe2 в системе Tl2Te-Sb2Te3.
В соединениях TlSbX2 и TlBiX2 с увеличением электроотрицательности халькогена увеличивается доля ионной составляющей химической связи, что приводит к закономерному изменению характера плавления (TlSb(Bi)Te2 плавятся инконгруэнтно, остальные – конгруэнтно, сульфиды образуют более острые максимумы, чем селениды), повышению температур плавления конгруэнтно плавящихся соединений и повышению термодинамической стабильности халькогенидов. В этом случае, для халькостибнитов наблюдается уменьшение симметрии кристаллической структуры соединений: гексагональная для TlSbTe2, моноклинная для TlSbSe2, триклинная для TlSbS2. Все хальковисмутиды TlBiX2 образуют ромбоэдрическую кристаллическую структуру с Пр.гр.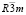 . При переходе S → Se → Te параметры кристаллической решетки увеличиваются.
. При переходе S → Se → Te параметры кристаллической решетки увеличиваются.
В системах Tl2S(Se)-Sb2S(Se)3 вблизи халькогенидов сурьмы образуются тройные соединения TlSb3S5, TlSb5S8 и TlSb3Se5. Образование этих соединений, видимо, связано с заменой в структуре Sb2S3 и Sb2Se3 части атомов сурьмы атомами таллия, что приводит к дефициту атомов в подрешетке халькогена и вызывает перестройку кристаллической структуры из ромбической в моноклинную в случае сульфидов, а в селенидной системе лишь увеличивается параметр кристаллической решетки.
В селен- и теллурсодержащих системах Tl-BV-X по разрезу Tl2X-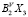 образуются соединения с общей формулой Tl9BVX6. Это объясняется кристаллической структурой Tl2Se и Tl5Te3. Как известно [18], в кристаллической структуре Tl2Se между слоями Se и Tl могут внедряться атомы селена с образованием фазы переменного состава Tl2Se-Tl5Se3.
образуются соединения с общей формулой Tl9BVX6. Это объясняется кристаллической структурой Tl2Se и Tl5Te3. Как известно [18], в кристаллической структуре Tl2Se между слоями Se и Tl могут внедряться атомы селена с образованием фазы переменного состава Tl2Se-Tl5Se3.
Кристаллохимический анализ кристаллических структур Tl2Se и Tl5Te3 показывает, что в их структуре тетраэдры таллия могут быть заполнены халькогеном или металлом, а слои могут быть составлены не только из одного сорта атомов, но и из атомов металла и халькогена. Это положение дает возможность предположить новые структурные варианты на основе структур Tl2Se и Tl5Te3 путем замещения атомов таллия различными металлами, обладающими той же валентностью и близкими ионными радиусами. Нами проведен сравнительный анализ дифрактограмм Tl2Se, Tl5Te3 и Tl9BVX6. Установлено, что дифрактограммы тройных соединений Tl9BVX6 лучше согласуются с данными для Tl5Te3. Сопоставление формул Tl5Te3 и Tl9BVX6 показывает, что если в структуре 4(Tl5Te3) два атома таллия заменить на атомы BV, то получим 2(Tl9BVX6).
Образование в указанных системах соединений типа Tl9BVX6 может быть объяснено также с точки зрения валентного состояния таллия в Tl5Te3. Как и в других халькогенидах в этом соединении теллур находится в валентном состоянии Te2-. Для того, чтобы в структуре 4(Tl5Te3) 20 атомов таллия предоставляли 24 электрона, атомы таллия должны находиться в различных валентных состояниях. Так как для таллия характерны валентные состояния Tl+и Tl3+, то можно предположить, что из двадцати атомов таллия восемнадцать находятся в состоянии Tl+, а два – в состоянии Tl3+, т.е. формулу 4(Tl5Te3) можно представить в виде 2(Tl93+Tl3+Te6). С этой точки зрения в кристаллической структуре Tl5Te3 положения 4с равномерно заняты атомами Tl+и Tl3+. Заменой Tl3+ трехвалентными атомами сурьмы и висмута образуются тройные соединения Tl9SbTe6 и Tl9BiTe6 соответственно, в селенидных системах Tl9SbSe6 и Tl9BiSe6.
Изоструктурность теллуридов Tl9BVTe6 с Tl5Te3 и селенидов Tl9BVSe6 с Tl5Se3 и Tl2Se выражается в образовании в тройных системах Tl-BV-Se(Te) непрерывных рядов твердых растворов между соответствующими двойными и тройными соединениями (рисунок).
В теллурсодержащих системах между твердыми растворами на основе Tl2Te (a) и Tl9BVTe6 (d) наблюдаются (рис. 1, в, е) морфотропные фазовые переходы (Tl2Te кристаллизуется в моноклинной структуре, а Tl9BVTe6 – в тетрагональной)
Следует отметить, что в системах Tl-BV-X термодинамическая и термическая стабильность изоформульных промежуточных фаз при переходе Te → Se → S и Sb → Bi увеличивается, что связано с увеличением разности электроотрицательностей составляющих их компонентов.
Стандартные термодинамические функции образования и стандартные энтропии тройных фаз в системах Tl-BV-X [2, 3, 7, 9, 12]
|
Соединение |
|
|
|
|
кДж/моль |
|||
|
TlSb3S5 |
311,9 ± 7,9 |
315,6 ± 8,1 |
348,4 ± 7,5 |
|
TlSbS2 |
143,2 ± 2,7 |
146,0 ± 3,1 |
164,1 ± 4,0 |
|
Tl3SbS3 |
251,6 ± 2,9 |
255,9 ± 4,2 |
319,4 ± 7,7 |
|
TlSb3Se5 |
264,9 ± 12,4 |
270,6 ± 11,0 |
392,5 ± 18,5 |
|
TlSbSe2 |
130,6 ± 4,4 |
134,3 ± 4,7 |
181,8 ± 11,8 |
|
Tl3SbSe3 |
238,8 ± 4,8 |
242,3 ± 6,7 |
352,9 ± 17,6 |
|
Tl9SbSe6 |
558,1 ± 5,9 |
566,0 ± 12,0 |
840,9 ± 34,0 |
|
TlSbTe2 |
76,9 ± 2,3 |
73,5 ± 2,2 |
197,5 ± 8,6 |
|
Tl9SbTe6 |
421,3 ± 6,9 |
402,9 ± 10,2 |
858,3 ± 30,8 |
|
TlBiS2 |
163,5 ± 4,1 |
170,0 ± 4,6 |
206,7 ± 13,8 |
|
TlBiSe2 |
141,5 ± 0,9 |
139,7 ± 3,0 |
211,4 ± 6,7 |
|
Tl9BiSe6 |
578,1 ± 2,2 |
573,9 ± 9,1 |
873,2 ± 25,7 |
|
TlBiTe2 |
91,2 ± 2,4 |
89,8 ± 2,1 |
235,0 ± 8,6 |
|
Tl9BiTe6 |
441,4 ± 5,8 |
434,4 ± 8,3 |
955,4 ± 25,0 |
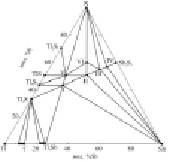

а) б)

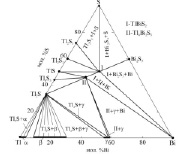
в) г)


д) е)
Диаграмма твердофазных равновесий систем Tl-Sb-S (a) [9, 13], Tl-Sb-Se (б) [10], Tl-Sb-Te (в) [1], Tl-Bi-S (г) [4, 5], Tl-Bi-Se (д) [6], Tl-Bi-Te (е) [11, 12]
Среди систем Tl-BV-X только в Tl-Sb-S образуются тройные соединения, в которых BV имеет степень окисления +5: Tl3SbS4 и TlSbS3. Отсутствие тройных фаз со степенью окисления BV(+5) в системах Tl-Sb-Se(Te) можно объяснить уменьшением разности электроотрицательностей BV-X, а в системах Tl-Bi-X – наличием у висмута внутренних d- и f-оболочек, экранирующих внешние электроны. В результате для сурьмы степень окисления +5 оказывается более стабильной, чем для висмута. Отметим, что среди двойных сульфидов сурьмы соединения, содержащие Sb(+3) более стабильны. Это проявляется в их конгруэнтном плавлении (Tl3SbS3 и TlSbS2) или сравнительно высокой температуре разложения (TlSb3S5 -693К, TlSb5S8 -683К). Тройные соединения, содержащие Sb(+5) плавятся инконгруэнтно и имеют более низкие температуры разложения (Tl3SbS4 -570К, TlSbS3 -673К). Свободная энергия образования (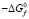 на г×атом-1) уменьшается в ряду: TlSbS2, Tl3SbS3, TlSb3S5, TlSb5S8, Tl3SbS4, TlSbS3. Стабильность Tl3SbS4 относительно TlSbS3, по-видимому, связана с числом атомов серы, приходящихся на один атом сурьмы.
на г×атом-1) уменьшается в ряду: TlSbS2, Tl3SbS3, TlSb3S5, TlSb5S8, Tl3SbS4, TlSbS3. Стабильность Tl3SbS4 относительно TlSbS3, по-видимому, связана с числом атомов серы, приходящихся на один атом сурьмы.
Во всех исследованных системах Tl-BV-X разрезы TlBVX2-X (BV, TlX), Tl9BVX6 (Tl3BVX3)-TlX(BV) являются квазибинарными или стабильными ниже солидуса. Только в системе Tl-Sb-S разрез Tl3SbS3-TlS не является стабильным ниже солидуса, что связано с образованием в системе Tl-Sb-S промежуточного соединения Tl3SbS4 и наличием в граничной системе Tl-S соединения Tl4S3.
В системах Tl-Sb-X поверхность ликвидуса сурьмы охватывает большую часть фазовой диаграммы, что объясняется большой термической стабильностью сурьмы по сравнению с другими фазами. В этих системах значительная часть сурьмы первично кристаллизуется монотектически.
Во всех системах Tl-Bi-X поверхность ликвидуса элементарного висмута практически вырождена ввиду его низкой температуры плавления.
Во всех системах Tl-BV-X значительную часть поверхности ликвидуса занимают поля первичной кристаллизации соединений TlBVX2, Tl9BVX6, что связано с их большой термодинамической и термической стабильностью.
В системах Tl-BV-X при переходе S → Se → Te наблюдается закономерное увеличение площади поверхности ликвидуса элементарного халькогена.
Площади полей первичной кристаллизации тройных соединений-аналогов при переходах Te → Se → S и Sb → Bi увеличиваются, что связано с увеличением термической и термодинамической устойчивостью этих фаз при соответствующих переходах.
Нами с помощью метода наименьших квадратов проведен корреляционный анализ зависимости термодинамических функций образования тройных соединений в системах Tl-BV-X от различных физико-химических характеристик образующих их элементов. Выборочный коэффициент корреляции оказался близким к единице, т.е. сильная корреляционная связь оказалась между ∆fG0(298K), ∆fH0(298K) тройных соединений – аналогов типа TlBVX2, Tl9BVX6 и разностью электроотрицательностей (∆ЭО) и силовых характеристик (∆γорб) элементов BV и X. Полученные уравнения регрессии, отвечающие корреляционной связи, имеют следующие линейные зависимости:
для соединений типа TlBVX2
– ∆fG0(298K) = 68,53 + 128,6∆ЭО,
– ∆fG0(298K) = – 63,75 + 148,2∆γорб,
– ∆fН0(298K) = – 65,04 + 139,1∆ЭО,
– ∆fН0(298K) = – 81,52 + 163,0∆γорб;
для соединений типа Tl9BVX6
– ∆fG0(298K) = 399,1 + 285,3∆ЭО,
– ∆fG0(298K) = – 199,3 + 607,3∆γорб,
– ∆fН0(298K) = 383,8 + 315,9∆ЭО,
– ∆fН0(298K) = – 268,2 + 663,1∆γорб.
При вычислениях нами использованы значения электроотрицательностей элементов по Полингу [17] и силовые характеристики атомов (gорб), приведенные в [8].
Библиографическая ссылка
Джафаров Я.И. НЕКОТОРЫЕ ЗАКОНОМЕРНОСТИ ХАРАКТЕРА ФАЗООБРАЗОВАНИЯ И ТЕРМОДИНАМИЧЕСКИХ ФУНКЦИЙ ОБРАЗОВАНИЯ ТРОЙНЫХ ХАЛЬКОСТИБНИТОВ И ХАЛЬКОВИСМУТИДОВ ТАЛЛИЯ // Международный журнал прикладных и фундаментальных исследований. 2015. № 7-1. С. 34-39;URL: https://applied-research.ru/en/article/view?id=6955 (дата обращения: 14.05.2026).


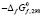
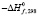
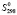 ,
,