Scientific journal
International Journal of Applied and fundamental research
ISSN 1996-3955
ИФ РИНЦ = 0,556
PREVENTING THE DEVELOPMENT OF NECROSIS IN THE FROSTBITE WITH TISSUE GLACIATION
Общее охлаждение и отморожения являются одними из тяжелых видов холодовой травмы, зачастую они приводят к высокому уровню инвалидизации и летальному исходу пострадавших [5,11,12,18,20,21]. В России 50 % из общего числа охлаждений и отморожений регистрируется на территории Якутии (инвалидность до 60 %, смертность – 11,5 чел. на 100 тыс. населения). Республика Саха (Якутия) – самый крупный регион России (3103,2 тыс.км²), расположена в северо-восточной части Сибири (105º-165º в.д.; 55,3º-77º с.ш.), однако население составляет всего 955 360 чел., что делает плотность населения одной из самых низких в России – 0,31 чел/км2. По абсолютной величине минимальной температуры и по суммарной продолжительности периода с отрицательной температурой (от 6,5 до 9 месяцев в год) республика не имеет аналогов в Северном полушарии. На территории Якутии расположено село Оймякон, где зарегистрирована рекордно низкая температура (–71ºС) [1,2].
Одной из особенностей холодовой травмы в условиях сверхнизких температур Якутии (ниже – 45 С) является прижизненное оледенение тканей, температура тканей при этом может доходить до – 29,8ºС. Отморожение с оледенением тканей относятся к наиболее тяжелым видам холодовой травмы, которое требует особой лечебной тактики. Имеющиеся методы оказания первой врачебной помощи при отморожениях без учета степени охлаждения тканей и глубины промерзания не могут сохранить пораженные ткани от развития некроза [13, 15, 16, 22, 23]. До недавнего времени развитие прижизненного оледенения тканей полностью отрицалась [6,7,10,13,16,18], однако, результаты нашего исследования доказывают обратное [3,4,5,8,9]. Целью работы является разработка способа предупреждения развития некроза при отморожениях в дореактивном периоде с оледенением тканей.
Материалы и методы исследования
Нами обследовано 6556 больных, из них 637 больных поступили в дореактивном периоде, 478 больных – с оледенением тканей, 1583 – с общим охлаждением.
С целью объективизации клинических признаков отморожений и выявления оледенения тканей нами использованы следующие методы, констатирующие характер нарушений кровообращения в пораженной конечности: капилляроскопия, реозовазография, ангиография, инфракрасная термография и разработанный нами метод определения внутритканевой температуры игольчатым термодатчиком. Применен новый способ размораживания тканей путем введения в наркоз с миорелексацией и искусственной вентиляцией легких.
Результаты исследования и их обсуждение
Развернутая клиническая картина глубины поражения появляется только после согревания конечностей, в так называемый, реактивный период. В скрытом, дореактивном периоде определить глубину поражения тканей, по мнению большинства авторов, невозможно [6,10,13,14]. Вместе с тем, определение тяжести отморожения в дореактивном периоде имеет огромное значение для прогнозирования и проведения раннего адекватного лечения.
Нами выявлено, что наиболее характерными симптомами глубокого отморожения, в дореактивном периоде, являются: побеление кожных покровов (98 ± 2 %); деревянистая плотность кожи (100 %); отсутствие активных движений в межфаланговых суставах (100 %); невозможность пассивных движений (100 %); «щипкообразная боль»; полная потеря чувствительности (91 ± 4 %); ощущение «как будто не мои руки (ноги)» – (89 ± 3 %); перкуторно – тупой, «деревянистый» звук (80 ± 6 %); ощущение похолодания конечностей (78 ± 8 %); жжение, или покалывание в пораженных участках (57 ± 4 %); ощущение ползания мурашек (31 ± 5 %); тяжести проксимального сегмента (25 ± 6 %); мраморный оттенок кожи (26 ±7 %). У 97 % больных с глубокими отморожениями отмечается сочетание следующих симптомов: побеление кожи на пораженном участке, полная анестезия, окоченение, деревянистая плотность периферических сегментов конечностей, невозможность активных и пассивных движений в межфаланговых суставах кисти или стопы, тупой деревянистый звук при поколачивании. Все эти признаки позволяют заподозрить у человека глубокое отморожение.
Однако только по клиническим признакам дореактивного периода холодовой травмы крайне трудно прогнозировать исход отморожений. Эта особенность диктует необходимость применения более достоверных и объективных методов диагностики тяжести холодовой травмы. С этой целью нами были использованы параклинические методы.
Метод капилляроскопии выявил, что у 100 % обследованных лиц в дореактивном периоде капилляры не определяются и как метод контроля восстановления кровотока и жизнеспособности тканей в раннем реактивном периоде оказалось неубедительной по причине выраженного отека тканей. Обработка реовазограмм показала, что амплитуда основного зубца (А) и реовазографического индекса резко снижена. Существенным недостатком этого метода является затруднение наложения пальцевых датчиков на раневую поверхность и следовательно, невозможность контроля за восстановлением жизнеспособности тканей. Применение метода ангиографии в дореактивный период показало резкое сужение основных сосудов предплечья и голени и отсутствие кровенаполнения пальцевых артерий. Применение термографии является наиболее эффективной для оценки динамики изменения площади жизнеспособных и некротизированных тканей в области поражения. Однако она значительно уступает визуальной оценке течения раневого процесса.
Учитывая недостатки вышеперечисленных методов, и тот факт, что основным этиологическим фактором глубины поражения тканей, несомненно, является степень снижения температуры тканей, мы разработали и использовали термопарный термометр для измерения кожной и внутритканевой температуры. Иглу термометра вводили на глубину 4-5 мм, при увеличении плотности тканей в случаях оледенения тоннель для введения датчика термометра формировали инъекционной иглой. Термометрия позволяет объективно оценить состояние трофики тканей, глубины и степени поражения, выявления оледенения ткани.
Данную методику апробировали на 79 пациентах поступивших в дореактивный период холодовой травмы. Ретроспективный анализ зависимости глубины отморожения от снижения температуры тканей в дореактивный период установил следующую закономерность. Если значения температуры тканей не ниже +14°С, то развивается отморожения I – II степени (достоверность прогноза 100 %). Снижение температуры тканей от + 14°С до +8ºС (достоверность 73 ± 6 %) развивается отморожение II-III степени, а при более низких температурах развиваются только глубокие поражения. Если температура тканей была снижена от +7ºС до + 1°С (достоверность 70 ± 5 %), то глубина поражения соответствовала III – IV степени отморожения. Оледенение тканей наступала при температуре –1°С и ниже (достоверность 97 + 3 %) и соответствовала только IV степени отморожения.
Таким образом, разработанный нами метод термометрии позволил с наибольшей достоверностью прогнозировать тяжесть отморожения уже в дореактивном периоде. Именно этим критерием мы руководствовались при оценке тяжести поражения и эффективности лечения отморожений в дореактивном периоде.
Наша тактика лечения глубоких поражений в дореактивном периоде на протяжении времен менялась. На первом этапе мы применяли наружное согревание в ваннах (температура воды равнялась + 37ºС) с постепенным повышением в течение 1 часа до +41º – +42°С. Параллельно проводили внутривенное введение литических смесей. После ванны назначалась УВЧ – терапия и проводили периневральную блокаду. Инфузионная терапия назначалась для нормализации свертывающей системы крови и купирования ангиоспазма. Анализ результатов и эффективности такой тактики лечения показал, при наружном согревании тканей, температура которых исходно была снижена до +7 ºС – + 1°С, развитие некрозов и последующих ампутаций отмечено у 82,1 ± 3 % больных а у больных с оледенением тканей – у 97 % . Следует отметить, что дополнительная пролонгированная (до 7 дней) внутриартериальная инфузия, состоящая из глюкозо-новокаиновая смеси и реополиглюкина, оказало более благоприятный эффект при отморожениях без оледенения. У этой группы больных некроз был ограничен только дистальными фалангами пальцев, а у больных с оледенением тканей эффект терапии был недостаточным, хотя удалось снизить уровень ампутации. У группы больных с прогнозируемыми глубокими отморожениями нижних конечностей согревание в ванне сочетали с пролонгированной (до 6 дней) эпидуральной анестезией. Предположение о положительном эффекте эпидуральной блокады не подтвердилось. При снижении тканевой температуры ниже +8°С повышалась частота глубоких некрозов.
Мы разделяем точку зрения тех авторов, которые считали, что согревание отморожений снаружи приводит к выходу из анабиоза поверхностных тканей, тогда как глубоколежащие структуры не в состоянии обеспечить их адекватное кровоснабжение. Это является одной из причин, способствующих некрозообразованию. Поэтому наиболее перспективным является согревание отмороженных тканей в направлении «изнутри – кнаружи».
Наш опыт показал, что попытка активных или пассивных движений в сегментах с глубоким поражением приводит к повреждению мелких сосудов и усугублению некротических изменений. Поэтому движения в отмороженных кистях, стопах в дореактивном периоде противопоказаны, напротив – необходима иммобилизация.
Для задержки согревания тканей снаружи мы использовали несколько вариантов термоизолирующих повязок. Лучшими оказались комбинированные, многослойные (с включением фольги) бахилы или бахилы из оленьей шкуры мехом внутрь. Бахилы из оленей шкуры использовались только в районах Крайнего Севера. Комбинированные многослойные бахилы имеют преимущество в том, что легко поддаются санитарной обработке и могут использоваться многократно.
Методика лечения с использованием термоизолирующих повязок заключается в следующем. После измерения температуры в концевых фалангах выполняют туалет кожных покровов и проводниковую анестезию. Без коррекции положения ригидных пальцев кистей, стоп накладывают контурные фиксирующие шаблоны. На пораженный сегмент надевают термоизолирующую бахилу и параллельно начинают инфузионную терапию. Оптимальный состав инфузата для внутривенной терапии: реополиглюкин – 400 мл; глюкоза 10 % – 200 мл; новокаин 0,1 % – 200 мл; папаверин 2 % – 4 мл; никотиновая кислота 1 % – 2 мл; витамин С 5 % – 10 мл; гепарин – 10000 ЕД; бикарбонат натрия 4 % – 300 мл. Инфузат вводится внутривенно, каждый день в течение 4 суток с последующей коррекцией по состоянию больного. В последующем, через каждые 4 часа под кожу живота вводят 2500 ЕД гепарина. Продолжительность согревания конечностей в теплоизолирующей повязке – 10-14 часов. Повязку снимают при достижении температуры в концевых фалангах до +21ºС – 24°С и выполняют первичную обработку раневой поверхности, а потом вновь проводят иммобилизацию пораженных сегментов конечностей.
При поражении кисти иммобилизацию проводят в положении возможного разгибания пальцев для профилактики развития сгибательной контрактуры в реактивном периоде. Данная методика лечения отморожений в дореактивном периоде оказалась действенной только применительно к больным со II, II-III и III степенью отморожения, т. е. при снижении температуры тканей до +5ºС – +9°С. Таким образом, медленное согревание тканей в теплоизолирующей повязке относительно благоприятно отражается на течение реактивного периода при отморожениях III и IV степени без оледенения тканей, и тем самым существенно снижает риск развития глубоких некрозов.
Оледенение тканей с понижением температуры ниже – 5°С значимо чаще заканчивается их мумификацией. Снижение глубокой температуры в пределах от – 1,5°С до – 3°С сопровождается некрозом в области дистальных фаланг пальцев. Промежуточные показатели температуры в пределах до -5°С не исключают развития глубоких некрозов, но границей их являются пальцы кисти или стопы.
Таким образом, при лечении с использованием термоизолирующих повязок впервые нам удалось достичь значительного ограничения зоны развития некроза, а также избежать его развития при прогнозируемом поражении III-IV степени без оледенения. В то же время в случаях оледенения кистей и стоп сохраняется риск развития гангрены. В связи с этим, мы решили, что данная методика лечения отморожений в дореактивном периоде недостаточно эффективна в случаях оледенения тканей. Следует отметить, что у некоторых больных с оледенением тканей и общим охлаждением исход лечения в термоизолирующих повязках был значительно лучше. Всем этим больным по поводу общего охлаждения проводился лечебный наркоз.
Нами разработан уникальный способ лечения отморожений в дореактивном периоде (патент РФ № 2152806 от 08.10.2001 г.), позволяющий восстановить жизнедеятельность, значительно улучшить результаты лечения и снизить уровень инвалидизации. Суть метода заключается в блокаде стойкого спазма периферических сосудов использованием длительного (до 24 и более часов) глубокого эндотрахеального наркоза в сочетании с постепенным согреванием конечностей теплоизолирующими повязками. Использование нашей методики значительно снижает вероятность развития сухой гангрены пальцев до 30 %, когда как без применения методики сухая гангрена развивается в 100 %. Методика позволяет всем пострадавшим избежать ампутации кистей или стоп, а ограничивается только ампутацией фаланг пальцев, тем самым существенно сокращая степень инвалидности. Кроме того согревание больного в состоянии наркоза снижает риск развития острой почечной недостаточности. Данная методика апробирована на 79 пациентах, нигде больше не применяется.
Лечение по этой методике показало следующие результаты. У 70 ± 7 % больных с отморожениями (оледенение с температурой от –1 º до – 14 °С) некрозов не было или они ограничивались поверхностными тканями. При температуре оледенения ниже –14°С развивались глубокие некрозы тканей (30 ± 7 %), но их протяженность не превышала фаланг пальцев. Ни в одном случае оледенения не было гангрены кистей или стоп.
Заключение
Подводя итоги многолетней работы по лечению отморожений, следует еще раз обратить внимание на то, что широко используемые клинические и параклинические методы не позволяют достаточно убедительно прогнозировать глубину поражения в дореактивном периоде. Только метод локальной термометрии тканей позволяет сделать это с высокой достоверностью. Вместе с тем, снижение температуры тканей не является фатальным и в значительной степени зависит от проводимого лечения. Особенно наглядно это подтверждается на примере лечения оледенений. Так, при согревании снаружи (в ванне) сухая гангрена кистей, стоп и пальцев почти неизбежна и составляет 90 ± 5 %. Длительная внутриартериальная инфузия снижает частоту таких исходов до 84 ± 9 %. Нами установлено, что наиболее эффективным является применение модифицированных термоизолирующих повязок в сочетании с лечебным интратрахеальным наркозом с релаксантами. При этом вероятность некроза кистей и стоп равна 0, а частота сухой гангрены пальцев снижается до 30 ± 7 %.
При прогнозируемом глубоком поражении без оледенения тканей наиболее перспективен метод лечения, включающий согревание изнутри с наложением модифицированных термоизолирующих повязок, проводниковую анестезию, иммобилизацию и инфузионную терапию.
|
Правая рука |
Левая рука |
|||||||||
|
Пальцы |
1 |
2 |
3 |
4 |
5 |
1 |
2 |
3 |
4 |
5 |
|
Температура области |
-5° |
-5° |
-4° |
-6° |
-4° |
-6° |
-6° |
-5° |
-5° |
-5° |
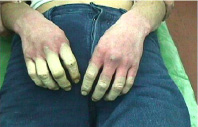
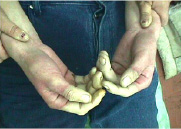
В первый день
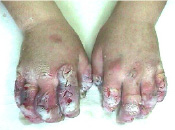
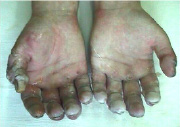
На 3-й день
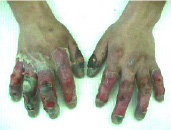
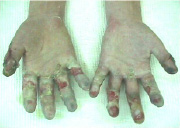
На 21-й день
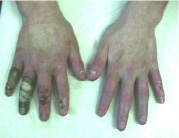
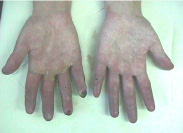
На 56-й день
Рис. 1. Верхние конечности в динамике с помощью нашего метода лечения
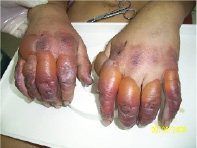
На следующий день после травмы
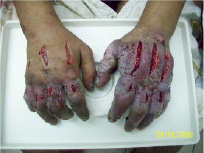
На 14-й день
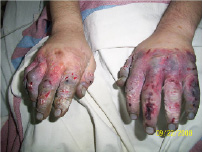
На 18-й день
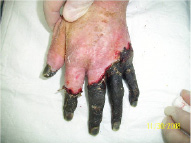
На 63-й день
Рис. 2. Без использования нашего метода лечения
Ежегодно в России по данным статистики от общего переохлаждения организма умирает более 200, а в Якутии – до 110 человек. На практике замерзшие люди считаются погибшими и без проведения каких-либо реанимационных мероприятий направляются в морг. Возможно, что в течение первых 2-х суток пострадавшие находятся в состоянии холодового анабиоза (очень редкий пульс, низкое АД) и вероятность восстановления жизнедеятельности организма не исключается (отмечаются случаи сохранения жизнедеятельности сердца и других органов у замерзших животных). Результаты нашего метода позволяют предположить теоретическую вероятность восстановления замороженных тканей, органов, а также оживления замерзших от общего переохлаждения.
Библиографическая ссылка
Алексеев Р.З., Томский М.И., Гольдерова А.С., Потапов А.Ф., Алексеев Ю.Р., Семенова С.В. ПРЕДУПРЕЖДЕНИЕ РАЗВИТИЯ НЕКРОЗА ПРИ ОТМОРОЖЕНИЯХ С ОЛЕДЕНЕНИЕМ ТКАНЕЙ // Международный журнал прикладных и фундаментальных исследований. 2015. № 8-1. С. 35-41;URL: https://applied-research.ru/en/article/view?id=7035 (дата обращения: 14.05.2026).

