Scientific journal
International Journal of Applied and fundamental research
ISSN 1996-3955
ИФ РИНЦ = 0,556
THE USE OF COMPOSITE OSTEOPLASTIC MATERIAL DEPROTEX IN ORTHOPAEDICS: CLINICAL CASE REPORT
Введение
Композиционные остеопластические материалы на основе тканей биологического происхождения достаточно широко используются в реконструктивной хирургии для восстановления структурной целостности тканей опорно-двигательного аппарата [7, 9, 11, 12, 14]. Потребность в биотканях для реконструкции скелета, при костных опухолях, артропластике в хирургической травматологии увеличилась за последнее десятилетие. И это связано с недавними успехами в понимании биологических процессов при трансплантации кости [7, 20]. Изыскание возможности управления репаративными процессами, изучение закономерностей новообразования костной ткани при пластике дефектов костно-пластическими материалами, сокращение сроков перестройки за счет адекватного выбора материалов или создания и использования материалов с заданными набором свойств являются актуальными вопросами как анатомии, так и травматологии и ортопедии [7, 9].
Характер регенераторных процессов в значительной мере определяется свойствами материалов, используемых для заполнения дефектов кости. Современный уровень медицины трудно представить без биологических имплантатов, с помощью которых выполняются реконструктивные хирургические вмешательства в травматологии и ортопедии [4, 7- 9, 13, 15, 16, 19, 20], челюстно-лицевой хирургии [2, 11, 12, 14], костной онкологии [1, 3, 10, 15]. Необходимость проведения операций по восстановлению строения и функции кости в различных областях медицины приоритетным определяет поиск и создание материалов на основе кости аллогенного происхождения [2, 6-9, 17, 18].
Целью публикации является описание клинического случая использования у пациентки с ортопедической патологией композиционного костно-пластического материала (ККПМ) «Депротекс» для остеопластики.
Задачи исследования
Обобщить литературный обзор о структурно-функциональных характеристиках композиционного костно-пластического материала «Депротекс».
Использовать ККПМ «Депротекс» при лечении пациентки и проанализировать результат.
Материал исследования: данные научной литературы, анамнестические, клинические, рентгенологические, морфологические данные, результаты анкетирования.
Композиционный костно-пластический материал «Депротекс» приготовлен из аллогенных костных фрагментов после депротеинизации, коллагенсодержащего раствора и антибактериальных препаратов по авторской методике [6, 7, 9].
Морфология поверхности композиционного ККПМ «Депротекс» на основе депротеинизированной кости (ДПК), т.е. ДПК опилок, коллагеновой добавки и антибактериальных препаратов приведена на рис. 1. ККПМ «Депротекс» визуально воспринимается как единое целое. Местами поверхность выглядит как бы «оплавленной» со сглаженными контурами; местами встречаются участки с шероховатой поверхностью, что характерно для опилов кости. Сглаженные участки характерны для коллагенсодержащего раствора, являющегося связующим компонентом в ККПМ. Участки с шероховатой поверхностью характерны для ДПК – опилок. В местах соединения нескольких плотно прилегающих друг к другу фрагментов ДПК - опилок образуются гребнеобразные выступы. В участках, где фрагменты недостаточно плотно подходят друг к другу, формируются углубления различной степени выраженности. Оценка соотношения кальция к фосфору (Ca/P) показала, что депротеинизация приводит к повышению соотношения Ca/P до 2,8, что обусловлено коагуляцией и экстрагированием белков при ферментативной обработке и, как следствие, к частичной потере микроэлементов, что и приводит к изменению соотношения Ca/P после депротеинизации [6].

Рис. 1. РЭМ – изображения поверхности ККПМ «Депротекс» на основе ДПК-опилок
Материал «Депротекс» являются композиционным резорбируемым костно-пластическим материалом, т.к. содержит более 2 компонентов и подвергается остеокластической резорбции [6, 7]. Вокруг эктопически имплантированного костно-пластического материала «Депротекс» отсутствует соединительно-тканная капсула, что свидетельствует о биосовместимости и биоактивности материала. Композиционный костно-пластический материал «Депротекс» не обладает остеоиндуктивными свойствами, что подтверждено тестами по эктопической имплантации [6]. Из публикаций по изучению репаративной регенерации губчатой кости при использовании костно-пластического материала «Депротекс» в эксперименте [5-7] известно, что использование ККПМ «Депротекс» для остеопластики губчатой кости приводит к остеогенезу с формированием костного регенерата в срок наблюдения 30 суток. В 90 суток наблюдали полное замещение дефекта органотипической костной тканью и ремоделирование в срок наблюдения 180 суток.
Материал прошёл обязательную в России токсикологическую экспертизу в ИЛ ФГУ «ВНИИМТ», г. Москва; приемочно-технические испытания в ИЛ медицинской техники ЗАО «Сибирский научно-исследовательский и испытательный центр медицинской техники»; процедуру экспериментальных и клинических испытаний. Клинические испытания были проведены на трех клинических базах:
- в Центральной стоматологической поликлинике федерального управления медико-биологических и экстремальных проблем при МЗ РФ (г. Москва);
- в Новосибирской государственной медицинской академии (г. Новосибирск);
- в Кемеровской государственной медицинской академии (г. Кемерово). Получено регистрационное удостоверение Росздравнадзора на изделие медицинского назначения № ФСР 2009/05555 «Депротекс», Приказом Росздравнадзора от 20 августа 2009 г. №6679 – Пр/09 и в соответствии с регистрационным досье №РД-2153/38514 от 28.10.2013 г. разрешено к производству, продаже и применению на территории Российской Федерации [7].
Использование данного материала при лечении стоматологической патологии у пациентов подтвердило эффективность материала при клиническом использовании [12].
Пример клинического использования
В нашу клинику обратился пациент К.. 32 года с диагнозом остеобластокластома (ОБК) основной фаланги III пальца кисти (рис.2). Основными жалобами являлись утолщение основной фаланги III пальца, болезненность только при максимальном сжатии кисти в кулак. Перечисленные ощущения пациент отмечал около 5 лет.
Пациент поступил на оперативное лечение. Во время операции пациенту выполнен линейный разрез по тыльно-локтевой стороне проксимальной части основной фаланги III пальца кисти. Выполнено разведение мягких тканей в стороны без повреждения капсуло-связочного аппарата сустава. При визуализации костной ткани отмечается неровность кортикальной пластинки, выраженный локальный остеопороз. При помощи скальпеля выполнено рассечение фрагмента кортикальной пластинки. Костной ложечки выполнено удаление желеобразного содержимого фаланги до ощущения кортикальной пластинки. Содержимое отправлено на гистологическое исследование. Полость проксимальной фаланги заполнена ККПМ «Депротекс». Послойное ушивание раны, асептическая повязка. Учитывая сохранность капсульно-связочного аппарата пястно-фалангового сустава, пациенту с первого дня после операции рекомендованы активные движения в суставах кисти.
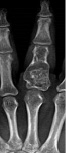
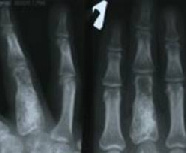
Рис. 2. Рентгенограммы пациента К, 32 г.
Диагноз: ОБК основной фаланги III пальца кисти: а-до операции, б – через 6 месяцев после операции
В ходе операции был забран операционно-биопсийный материал для гистологического исследования. В микропрепаратах визуализировалась ткань, приближающаяся к типу зрелого гиалинового хряща (рис.3). Однако, отличалась беспорядочным расположением клеток, неравномерностью их величины, формы, неправильным соотношением клеток и основного вещества (т.е. клетки располагаются местами одиночно, а местами группами; участки богатые клетками чередовались с участками, иногда почти бесклеточными, межклеточное вещество имеет характер гиалинового хряща).
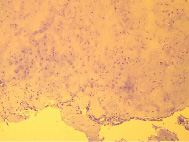
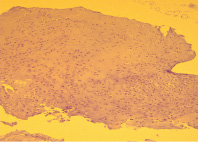
Рис. 3. Микропрепараты пациента К, 32 г.
Диагноз: Энхондрома основной фаланги III пальца кисти. Окр.по Ван Гизон. Ув. х 100
Послеоперационный период без особенностей. При контрольном рентгенологическом исследовании определяется перестройка ККПМ «Депротекс», отсутствие полости в основной фаланге III пальца кисти. Движения в суставах кисти не ограничены, безболезненны.
Таким образом, использование композиционного костно-пластического материала «Депротекс» у пациентов при ортопедической патологии приводит к восстановлению анатомической структуры и функции кости и материал может быть рекомендован к использованию и при лечении подобной патологии у пациентов.
Библиографическая ссылка
Александров Т.И., Подорожная В.Т., Чорний С.И., Серпенинова Н.Н. ИСПОЛЬЗОВАНИЕ КОМПОЗИЦИОННОГО КОСТНО-ПЛАСТИЧЕСКОГО МАТЕРИАЛА «ДЕПРОТЕКС» В ОРТОПЕДИИ (ОПИСАНИЕ КЛИНИЧЕСКОГО СЛУЧАЯ) // Международный журнал прикладных и фундаментальных исследований. 2015. № 9-4. С. 630-633;URL: https://applied-research.ru/en/article/view?id=7561 (дата обращения: 16.05.2026).

