Scientific journal
International Journal of Applied and fundamental research
ISSN 1996-3955
ИФ РИНЦ = 0,556
RESULTS OF SURGICAL TREATMENT OF PATIENTS WITH HEMANGIOMAS OF THE THORACIC AND LUMBAR SPINE (EXPERIENCE OF THE NOVOSIBIRSK NRITO)
Первое описание гемангиомы тела позвонка относится к 1867 году. Р. Вирхов представил выявленную на секции сосудистую опухоль, которую и назвал гемангиомой. Данная патология встречается у 10–12 % людей. Только 0,9–1,2 % всех позвоночных гемангиом являются симптоматическими [1, 2, 7]. Гемангиома у женщин встречается чаще, чем у мужчин и редко встречаются у молодых. Гемангиомы могут находиться в любом отделе позвоночного столба, включая крестец, но чаще возникают в грудном и поясничном отделе позвоночника. В 30 % случаях диагностируются единичные гемангиомы. Примерно в 30 % случаев повреждаются тела двух-трех позвонков, еще в 30 % – повреждается до 5 позвонков. В 10 % случаев выявляются повреждения более 5 позвонков. Гемангиомы чаще поражают тела позвонков, реже – задние их структуры. В некоторых случаях диагностируются мягкотканые паравертебральные компоненты, которые могут стать причиной компрессии спинного мозга [8]. Тактика лечения при агрессивных гемангиомах направлена на прекращение роста опухоли [2, 10].
По мнению ряда авторов, лечение гемангиом позвонков является дискуссионным вопросом. При капиллярных формах гемангиом тел позвонков в большинстве случаев требуется динамическое наблюдение [10]. При кавернозных формах гемангиом позвонков без неврологического дефицита и мягкотканого компонента выбором метода лечения являются вертебропластика или кифопластика тел поврежденных позвонков. В публикациях многих авторов отмечен положительный эффект вертебропластики гемангиом тел позвонков [3, 5, 8, 14]. Однако, тактика выбора метода лечения агрессивных гемангиом позвонков с наличием неврологического дефицита и мягкотканого компонента во многих случаях является дискутабельной. По мнению ряда авторов, гемангиомы с экстравертебральным ростом и наличием неврологического дефицита требуют направленной лучевой терапии [6, 11]. По нению других авторов, при наличии неврологического дефицита необходима декомпрессивная операция на уровне повреждения [3, 13, 6].
Следует помнить, что сами по себе оперативные вмешательства представляют серьезное испытание для пациента, т.к. они сопровождаются риском интра- и послеоперационных осложнений. Поэтому при выборе объема хирургического лечения пациентов необходимо решить несколько первоочередных вопросов: возможно ли радикальное удаление опухоли, сможет ли операция существенно улучшить качество их жизни, не приведет ли вмешательство к декомпенсации сопутствующих заболевания и какой объем операции перенесет больной. Основой, определяющей тактику хирургического лечения, является максимальное улучшение качества жизни пациентов. Хирургическое лечение, включает в себя два основных момента: полное или частичное удаление патологического очага, фиксацию поврежденных сегментов. Это может выполняться как одномоментно, так и в несколько этапов. В некоторых случаях стабилизация поврежденного участка позвонка может являться окончательной.
В стремлении улучшить результаты лечения гемангиом позвонков важной задачей является определение оптимального объема хирургического лечения в зависимости от форм, распространенности и локализации гемангиом.
Цель исследования
Определить эффективность хирургического лечения солитарных и множественных гемангиом с локализацией в телах грудных и поясничных позвонков и с поражением их задних структур.
Материалы и методы исследования
За период с 2009 по 2014 годы в отделении патологии позвоночника Новосибирского НИИТО наблюдалось 49 больных с прогрессирующим ростом гемангиомами тел позвонков грудного и поясничного отелов позвоночника в возрасте от 28 до 65 года (средний возраст 54,1). В группе исследования женщин было 39, мужчин – 10. В 32 случаях диагностированы солитарные гемангиомы, в 17 случаях – множественные гемангиомы тел позвонков. Локализация гемангиомы в шейном отделе позвоночника диагностирована у 3 больных, в грудном отделе позвоночника – у 32, в поясничном отделе – у 14 больных. Также у 16 больных диагностированы поражение задних структур и у девяти – паравертебральные мягкотканые компоненты с признаками патологического перелома тел позвонков.
В каждом случае методами исследования служили клинические и объективные методы исследования: рентгенография позвоночника, МРТ, МСКТ и денситометрия. Оценивались выраженность болевого синдрома и степень нарушения дееспособности по индексу Освестри до и после операции, а также в отдаленном периоде наблюдения.
Результаты исследования и их обсуждение
В первую группу были включены больные с солитарными гемангиомами без повреждения задних структур. В эту группу вошли 29 (59 %) пациентов. Во вторую группу были включены больные с множественными гемангиомами, также без повреждения задних структур – 11 (22 %). Третью группу составили пациенты с гемангиомати тел и задних структур позвонков с наличием паравертебрального и интраканального мягкотканого опухолевого компонента 9 (18 %) с признаками компрессионного перелома у 2 из них. У трех больных выявлен в различной степени выраженности неврологический дефицит, обусловленный компрессией спинного мозга. В 40 случаях операция была закончена пластикой тел позвонков костным цементом и в девяти случаях проведены декомпрессивно-стабилизирующие операции на позвоночнике после пластики тела поврежденного позвонка костным цементом.
Оценка субъективных критериев проводилась до вмешательства, после вмешательства, а также в период 4, 8, и 12 мес. после операции. Выраженность болевого синдрома у пациентов с солитарными гемангиомами до операции составляла 5,2 ± 0,3 баллов, степень нарушения дееспособности 42 ± 7,8 %. Выраженность болевого синдрома у пациентов с множественными гемангиомами и гемангиомами с паравертебральными и интраканальным мягкоткаными компонентами до операции составляла 6,2 ± 0,7 и 5,3 ± 0,2 баллов, степень нарушения дееспособности 42 ± 7,8 % и 44 ± 6,2 % соответственно. Оценка данных показателей в раннем постоперационном периоде во всех группах соответствовала 1 и 2 баллам по ВАШ-10. При этом степень удовлетворенности больных по индексу Освестри составила 28 ± 1,2 %. В позднем периоде наблюдения выраженность болевого синдрома у больных первой группы по визуально-аналоговой шкале (ВАШ-10) составила 2,1 ° ± 0,1 баллов, индекс Освестри – 22,3 ± 11,8. Выраженность болевого синдрома во второй и третьей группе больных по ВАШ-10 составила в среднем 2,7 ± 0,5 и 2,5 ± 0,3 баллов соответственно, и степень нарушения дееспособности больных по индексу Освестри составила 22 ± 0,8 %, 20 ± 1,0 % и 23 ± 1,0 % соответственно в 1, 2 и 3 группах. Прогрессирование опухолевого процесса в периоде наблюдения не отмечено ни в одном случае. Полный регресс неврологической симптоматики наступил только у 2 пациентов, у одного сохранился нижний парапарез со снижением моторных функций до 4 баллов.
Клинический пример. Пациент П., 25 лет, считает себя больным в течение трех лет. Беспокоят боли в грудном отделе позвоночника. Отмечает усиление болевого синдрома в течение последних двух лет. Боли в грудном отделе преимущественно слева и в ночное время. Был обследован у невролога и нейрохирурга по месту жительства. Лечился по поводу остеохондроза грудного отдела позвоночника. В связи сохраняющимися болями обратился на консультативный прием. Проведено обследование (рис. 1–2). Диагностировано объемное образование Th8 позвонка. Проведена биопсия тела Th8 позвонка. Результат гистологического исследования: доброкачественная опухоль мезенхимального происхождения сосудистого генеза.
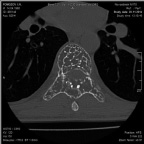
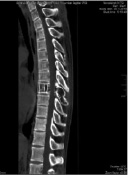
а б
Рис. 1. МСКТ грудного отдела позвоночника до операции (а – аксиальная проекция, б – сагиттальная реконструкция)
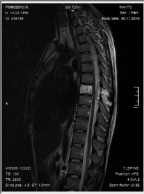
Рис. 2. МРТ грудного отдела позвоночника до операции
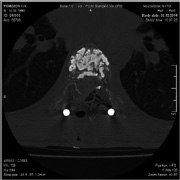
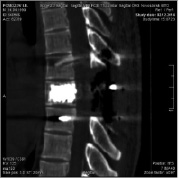
а б
Рис. 3. МСКТ грудного отдела позвоночника после операции (а – аксиальная проекция, б – сагиттальная реконструкция)
Проведено хирургическое лечение. Под общим обезболиванием проведена пункция опухоли через корни дуг слева и справа, отмечено «фонтанирование» крови из игл. Осуществлена чрезкожная пластика тела Th8 позвонка костным цементом, в результате чего кровотечение прекратилось. После полимеризации костного цемента (через 30 мин.), произведен хирургический доступ к задним структурам грудных позвонков, проведена резекция задних структур Th8 позвонка, задняя декомпрессия спинного мозга на уровне Th8 позвонка, транспедикулярная фиксация на уровне Th7-Th9 позвонков (рис. 3). Общая интраоперационная кровопотеря составила 450 мл. Послеоперационный период без особенностей. Заживление раны первичным натяжением. Болевой синдром купирован. На 10 сутки после операции пациент был выписан на амбулаторное лечение.
Гемангиомы – доброкачественные медленнорастущие сосудистые опухоли, состоящие из венозных сосудов. Позвоночник является распространенным по встречаемости местом гемангиом в костях. Большая часть гемангиом локализуются единичными очагами и во многих случаях обнаруживаются случайно, при рентгенологическом исследовании. Однако, локальная боль, наличие неврологического дефицита могут быть признаками агрессивных форм гемангиом позвонков. При обследовании этих больных, нередко диагностируется наличие мягкотканого компонента опухоли. В этом исследовании, нами было изучено результаты лечения трех групп больных. Особое место занимает больные третьей группы, у которых выявлены гемангиомы с наличием мягкотканого компонента. При изучении анамнеза и динамики прогрессирования заболевания нами было отмечено, что все пациенты страдали местными болями в области локализации опухоли не менее года и в дальнейшем, по мере возникновения неврологического дефицита, обращались за медицинской помощью. При обследовании у всех 9 пациентов этой группы выявлено наличие мягкотканого компонента опухоли с компрессией спинного мозга и спинномозговых корешков. Агрессивные гемангиомы с неврологическим дефицитом, чаще локализовались в грудном отделе позвоночника, где позвоночный канал узкий и резервные пространства минимальны. Исторически хирургическое лечение гемангиом позвонков сводилась к симптоматическому лечению или частичному удалению опухолевой массы в области повреждения. Удаление опухоли нередко заканчивалась большими кровопотерями, или усугублением неврологического дефицита [4]. Ляминэктомия на уровне поражения позвонков приводила к относительно положительным результатом. В некоторых исследования описаны положительные результаты ведения этанола в область опухоли позвонка [4, 9]. Во всех случаях не было достигнута продолжительная ремиссия болевого синдрома и неврологического дефицита. Также описаны случаи усугубления неврологического дефицита, возникновения инфекции в области хирургического вмешательства, прогрессирование гемангиом тел позвонков и возникновения патологического перелома (4).
Не смотря на риск возникновения осложнений, предпочтительным является хирургическое лечение агрессивных гемангиом позвонков с неврологическим дефицитом. Многими авторами была предложена тактика хирургического лечения в объеме удаления опухоли до здоровой ткани [4, 3]. Однако, в связи большой кровопотерей, в основном проводилась декомпрессия спинного мозга на уровне повреждения. После предварительной трансмагистральной эмболизации опухоли Aich и соавт. (2010), осуществляют декомпрессию спинного мозга и удаление опухоли. Однако операции после эмболизации питающих ее сосудов проводились при минимальной агрессивности и отсутствия мягкотканого интраканального компонента опухоли [4].
Радиотерапию используют после резекции опухоли и для лечения солитарных гемангиом с выраженными местными болями. После этого лечения Fox MW, Onofrio BM (1993) описали в 3-х из 10 случаев рецидив опухолей [9].
Проведенное хирургическое лечение больных с солитарными и множественными гемангиомами тел позвонков без неврологического дефицита, привело к стойкой ремиссии болевого синдрома и не наблюдалось случаев рецидивов. Несомненно, больные с гемангиомами тел позвонков при наличием неврологического дефицита, должны быть прооперированы. Выполненные нами декомпрессивно-стабилизирующие операции при агрессивных гемангиомах привели к положительными результатами. По нашему мнению, при гемангиомах без повреждения задних структур и без неврологичесокого дефицита, применение вертебропластики является оптимальным методом лечения. При агрессивных гемангиомах с наличием мягкотканого компонента и неврологического дефицита, необходима применения декомпрессию спинного мозга со стабилизацией. С целью уменьшения кровопотеря вовремя операции и для восстановления опороспособности вентральной колонны необходимо проведение вертебропластики с максимально плотным заполнением костным цементом в области поражения тела и корней дужек позвонка.
Выводы
При солитарной гемангиоме с поражением задних структур позвонка, локальный болевой синдром выражен значительней, чем при деструкции только тела. Наличие стеноза позвоночного канала, обусловленного, в том числе мягкотканым компонентом опухоли, определяет необходимость последовательного проведения пластики тела позвонка костным цементом, декомпрессии и стабилизации. При солитарных и множественных гемангиомах тел позвонков пластика костным цементом является достаточной и предпочтительной.
Библиографическая ссылка
Рерих В.В., Рерих В.В., Рахматиллаев Ш .Н., Пендюрин И.В. РЕЗУЛЬТАТЫ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ПАЦИЕНТОВ С ГЕМАНГИОМАМИ ГРУДНЫХ И ПОЯСНИЧНЫХ ПОЗВОНКОВ (ОПЫТ НОВОСИБИРСКОГО НИИТО) // Международный журнал прикладных и фундаментальных исследований. 2015. № 11-1. С. 55-59;URL: https://applied-research.ru/en/article/view?id=7672 (дата обращения: 23.05.2026).

