Scientific journal
International Journal of Applied and fundamental research
ISSN 1996-3955
ИФ РИНЦ = 0,556
THERMODYNAMIC MODELLING SILICON REDUCTION FROM SILICON OXIDE BY ALUMINIUM
Развитие солнечной энергетики в настоящее время является одной из важнейших задач, стоящих перед человечеством [2]. В связи с этим, в развитых странах мира, активно ведутся разработки экологически чистых преобразователей солнечной энергии в электрическую на основе особо чистого кремния. Мировой рост производства солнечных элементов составляет до 30 % ежегодно. Однако развитие в этом направлении сдерживается высокой себестоимостью продукции на базе «солнечного» кремния по сравнению с традиционными источниками энергии [4].
В настоящее время имеется множество методов производства «солнечного» поликристаллического кремния. При всем разнообразии методов промышленное производство осуществляется по традиционному «Сименс-методу» или методами восстановления трихлорсилана [3]. Из известных нам процессов, предлагаемых в качестве альтернативы «Сименс-методу» [1], экологически чистых и экономичных проектов нет.
Нами предлагается получать кремний экологически чистым и безотходным металлотермическим методом, в котором в качестве основных сырьевых материалов используется мелкодисперсный высокочистый диоксид кремния (кварцевое стекло) и алюминиевая пудра. Процесс описывается суммарной экзотермической реакцией:
3SiO2+4Al=3Si+2Al2O3, (1)
которая с термодинамической точки зрения возможна уже при температуре 373K (табл. 1).
Таблица 1
Влияние температуры на ΔGT (кДж) и ΔHT (кДж) реакции (1)
|
Параметр |
Температура, K |
||||||
|
373 |
573 |
773 |
973 |
1173 |
1373 |
1573 |
|
|
ΔGT |
-589,1 |
-572,3 |
-555,2 |
-534,9 |
-500,1 |
-476,7 |
-447,2 |
|
ΔHT |
-619,9 |
-620,9 |
-623,0 |
-671,8 |
-678,7 |
-679,0 |
-678,3 |
В настоящей статье приводятся результаты термодинамического моделирования восстановления кремния алюминием из SiO2 в системах 3SiO2-nAl (n=4–8).
Цель исследования – термодинамическое моделирование взаимодействия SiO2 с алюминием в темперутурном интервале от 500-2500°С и давлении 0,1 МПа.
Материалы и методы исследования
Исследования проводились при помощи программного комплекса HSC-5.1 Chemistry разработанного Outokumpu Research Oy (Финляндия [6]). Разработчики комплекса основывались на идеологии консорциума SGTE (Scientific Group Thermodata Europe), которая занимается созданием, поддержкой и распространением высококачественных баз данных, предназначенных для расчета равновесного состава химически реагирующих систем; объединение усилий исследователей разных стран с целью унификации термодинамических данных и методов их получения. В состав SGTE входят специализированные научные центры Германии, Канады, Франции, Швеции, Великобритании и США (www.sgte.org). В нашей работе мы использовали подпрограмму Equilibrium Compositions комплекса HSC-5.1 для расчета равновесия на основе принципа минимума энергии Гиббса исходя из выражения:
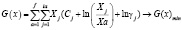 , (2)
, (2)
при ограничениях в виде системы линейных уравнений баланса массы вещества:
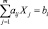 , (3)
, (3)
и условии нормировки:
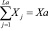 , (4)
, (4)
где f – общее число фаз системы; Bi – общее число независимого компонента i в системе; ja – масса чисел, показывающих число -тых независимых компонентов в фазе а системы; n – число независимых компонентов системы; Cj – эмпирическая термодинамическая функция; Xa – общее число молей фазы а в системе; 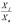 – мольная доля зависимого j компонента в фазе а; Yy – коэффициент активности j компонента. Параметры равновесия термодинамической системы определяются решением математической задачи о нахождении экстремума с учетом всех ограничений с использованием функций Лангранжа и метода последовательных приближений Ньютона.
– мольная доля зависимого j компонента в фазе а; Yy – коэффициент активности j компонента. Параметры равновесия термодинамической системы определяются решением математической задачи о нахождении экстремума с учетом всех ограничений с использованием функций Лангранжа и метода последовательных приближений Ньютона.
При работе с комплексом HSC – 5.1 первоначальная информация представлялась в виде количественного (кг) распределения веществ в исследуемой системе. Затем определялась равновесная степень элемента (α, %) по продуктам взаимодействия. Для этого расчеты проводили по формуле
αэл= [Gэл(прод)/Gэл(исх)]100, (5)
где Gэл(исх) – масса элемента в исходной системе, кг; Gэл(прод) – масса элемента в образующемся продукте, кг
Результаты исследования и их обсуждение
В системе 3SiO2-4Al в температурном интервале 500–2500°С основными веществами являются Si, Al2SiO5, SiO2, SiO(г), Al2O3, Al, Al2O(г) (рис. 1).
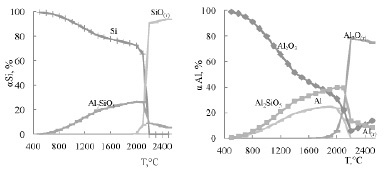
Рис. 1. Влияние температуры на степень распределения кремния и алюминия в системе 3SiO2-4Al
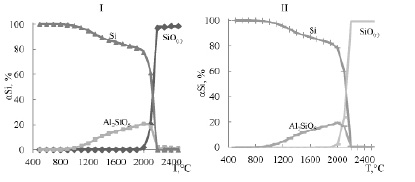
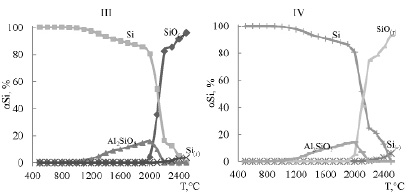
Рис. 2. Влияние температуры и количества Al на степень распределения кремния ɑSi в системе 3SiO2-nAl: I – n=4,6; II – n=6; III – n=7,4; IV – n=8
При 400°С с термодинамической точки зрения SiO2 полностью взаимодействует с алюминием. При увеличении температуры степень восстановления кремния уменьшается и образование Si прекращается при Т ≥ 2200°С. Ввиду образования в степени Al2SiO5, взаимодействие (например при 1000°С) происходит по схеме:
3Si+2Al2O3=
=2,7Si+0,3Al2SiO5+1,5A2O3+0,4Al (6)
При 2200°С кремний в системе исчезает и продуктами взаимодействия являются Al, Al2O3, SiO, Al2O3, Al2SiO5, Al2O5.
Процесс описывается уравнением:
2,7Si + 0,3Al2SiO5 + 1,5Al2O3 + 0,4Al =
= 2,4SiO(г) +0,3Si +0,3Al2SiO5 +
+1,5Al2O(г) +0,2Al2O3. (7)
Из рис. 2 следует, что изменение в системе n от 4 до 8 приводит к увеличению температурной области полного восстановления кремния. Так, при n=4 полный переход кремния из SiO2 в Si наблюдается при 500°С (затем степень образования Si уменьшается), а при n=8 эта область расширяется до 1000°C.
На рис. 3 приведена информация о распределении алюминия в системе 3SiO2-nAl из которой следует, что при увеличении в системе алюминия наблюдается накапливание его, что является неблагоприятным для последующего разделения кремния от алюминия.
Исследование влияния давления на систему 3SiO2-4Al показало, что увеличение давления в системе 3SiO2-4Al от 0,01 МПа до 0,2 МПа не оказывает существенного влияния на поведение кремния, за исключением лишь того, что при 0,01 МПа элементный кремний существует до 2300°С, а при 0,2 МПа – до 1900°С (рис. 4).
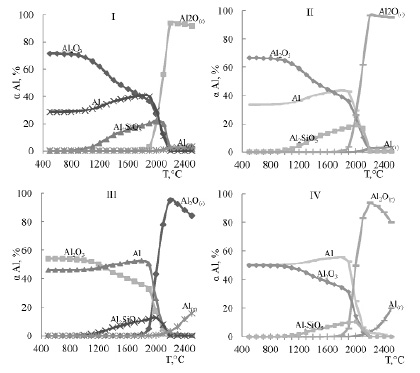
Рис. 3. Влияние температуры и количества алюминия на степень распределения алюминия (ɑAl) в системе 3SiO2-nAl: I – n=4,6; II – n=6; III – n=7,4; IV – n=8
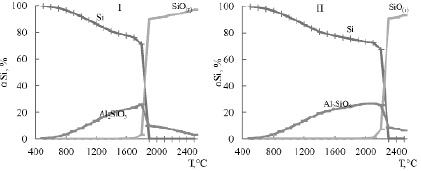
Рис. 4. Влияние температуры и давления на степень распределения кремния в системе 3SiO2-4Al: I – p=0,01 МПа II – p=0,2 МПа
Определение оптимальных технологических параметров восстановления кремния в системе 3SiO2-nAl определялось посредством рототабельного планирования исследовании второго порядка, с получением адекватного уравнения регрессии и графической оптимизацией процесса посредством горизонтальных разрезов поверхности отклика – αSi [5]. Независимыми переменными являлись температура (кодированный – Х1, натуральный – Т, °С), количество алюминия (кодированный вид – Х2, натуральный – n, кат).
В табл. 2 приведена матрица планирования исследований по определению влияния температуры и количества алюминия на αSi.
На основании данных табл. 2 получены следующее адекватное уравнение регрессии в натуральном виде:
αSi =107,549 – 0.02184∙T + 0,00307∙n+ +0,0039∙Т∙n – 0,00000551∙T2 – 0,1882∙n2 (8)
Используя уравнения регрессии (8) по программе Mathcad построена поверхность отклика и ее горизонтальные сечения (рис. 5). Из рис. 5 следует, что высокая степень образования кремния (≥97 %) может быть достигнута в области ABCDEF, т.е. при 500 – 1000°С и n = 4-8 кат).
Цифры на линиях – степень образования кремния, %.
Таблица 2
Матрица планирования исследований по взаимодействию SiO2 и алюминия
|
№ п/п |
Факторы |
Эксп. (αSi, %) Х1 |
Расч. (αSi, %) Х2 |
|||
|
Кодированный вид |
Натуральный вид |
|||||
|
Х1 |
Х2 |
Т |
n |
|||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|
1 |
- |
- |
616,3 |
1 |
99,5 |
99,06 |
|
2 |
+ |
- |
1183,7 |
4,6 |
91,5 |
91,21 |
|
3 |
- |
+ |
616,3 |
7,4 |
99,3 |
99,46 |
|
4 |
+ |
+ |
1183,7 |
7,4 |
97,5 |
97,81 |
|
5 |
+1,41 |
0 |
1300 |
6 |
93,5 |
93,45 |
|
6 |
-1,41 |
0 |
500 |
6 |
100 |
100,16 |
|
7 |
0 |
+1,41 |
900 |
8 |
99,8 |
99,43 |
|
8 |
0 |
-1,41 |
900 |
4 |
94 |
94,48 |
|
9 |
0 |
0 |
900 |
6 |
97,8 |
97,7 |
|
10 |
0 |
0 |
900 |
6 |
97,6 |
97,7 |
|
11 |
0 |
0 |
900 |
6 |
98 |
97,7 |
|
12 |
0 |
0 |
900 |
6 |
97,4 |
97,7 |
|
13 |
0 |
0 |
900 |
6 |
97,7 |
97,7 |
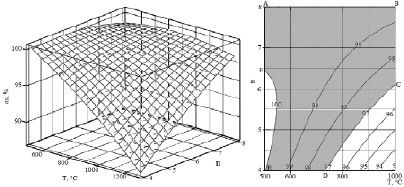
Рис. 5. Влияние количества алюминия и температуры на форму поверхности отклика (степени образования элементного кремния) и её горизонтальные сечения
Заключение
Таким образом, проведенные исследования позволили установить, что:
– В системе 3SiO2-4Al при 400°С SiO2 полностью взаимодействует с алюминием образуя кремний и Al2O3; при увеличении температуры в системе образуются Al2SiO5, SiO2, SiO(г), Al, Al2O(г).
– В системе 3SiO2-nAl увеличение n от 4 до 8 позволяет увеличить температуру полного перехода Si из SiO2 от 500°С до 1000°C.
– Изменение давления в системе 3SiO2-4Al не оказывает существенного влияния на поведение кремния и алюминия.
– Найдено, что степень образования кремния на уровне 97–100 % может быть достигнута в температурной области 500 – 1000°С и количестве алюминия 4-8 кат.
Библиографическая ссылка
Сержанов Г.М., Шевко В.М., Лавров Б.А., Аманов Д.Д. ТЕРМОДИНАМИЧЕСКОЕ МОДЕЛИРОВАНИЕ ВОССТАНОВЛЕНИЯ КРЕМНИЯ ИЗ ОКСИДА АЛЮМИНИЕМ // Международный журнал прикладных и фундаментальных исследований. 2015. № 11-2. С. 161-166;URL: https://applied-research.ru/en/article/view?id=7698 (дата обращения: 02.06.2026).

