Scientific journal
International Journal of Applied and fundamental research
ISSN 1996-3955
ИФ РИНЦ = 0,556
FEATURES OF A CIRCULATION IN THE FEMORAL CONDYLE AND IN THE TIBIA IN A 2ND DEGREE GONARTHROSIS
Гонартроз – одна из медико-социальных проблем современного общества: на 10 000 жителей России приходится 99,6 случаев заболевания. Патологию чаще регистрируют у лиц старше 55 лет (10 %), снижение качества жизни отмечают до 80 %, инвалидизацию – 10-21 % пациентов [4,10].
Причинами первичного (идиопатического) гонартроза считают дисплазию (врождённые особенности, приводящие к «плохой» биомеханике), перегрузку сустава и нарушения кровообращения в его компонентах. Сначала заболевание проявляется в одном, в последующем – в обоих суставах. Патологические изменения выражаются в дегенерации суставного хряща, склерозировании субхондральной кости и вялотекущей воспалительной реакции. Тяжесть заболевания в 12-24 % увеличивают метаболические остеопатии, появляющиеся вследствие приёма лекарственных препаратов, климакса и так далее [7].
Обычно пациенты игнорируют проявления гонартроза 1 степени («стартовые» боли и утомляемость сустава) и обращаются с клинической картиной, характерной для гонартроза 2 степени: болями, ограничивающими нагрузки, и болями покоя, проходящие после отдыха, приёма аналгетиков. Обследование выявляет болезненность по ходу суставной щели и в области остеофитов (следствие сдавления тканей и раздражения надкостницы), ограничение движений (чаще разгибания на 10-15 °), отёки, увеличение заворотов и сумок сустава (следствие хронического воспаления синовиальной оболочки и явного или скрытого синовита). На рентгенограммах обнаруживают неравномерное сужение суставной щели из-за потери части суставного хряща, субхондральный остеосклероз и остеофитоз [1, 5]. Изменения в области наружных и внутренних мыщелков костей отличаются по выраженности, поэтому в современных классификациях, например, AMERICAN COLLEGE OF RHEUMATOLOGY (Altman R.D. et al., Brandt K.D. et al. 1986), или АРУ (2000), выделяют медиальный и латеральный тибиофеморальные, а также пателлофеморальный отделы сустава.
В ФГБУ «РНЦ «ВТО» им. акад. Г.А. Илизарова» разработан способ оперативного лечения гонартроза 2 степени, включающий туннелизацию мыщелков костей спицами, введение в туннели аутологичной крови с элементами костного мозга, и лаваж сустава [6,8]. Асимметрия изменений в отделах сустава предполагает различия регионального кровообращения и его реакций, спицы можно использовать как электроды, и было решено изучить изменения кровообращения в мыщелках бедренной и большеберцовой костей пациентов на этапах оперативного вмешательства.
Цель исследования: выявить особенности кровообращения в мыщелках бедренной и большеберцовой костей пациентов с гонартрозом 2 степени перед началом туннелизации.
Материалы и методы исследований
Обследованы 42 пациента возрастом 63,1 ± 0,9 года, из которых 6 (15 %) были мужчины. Характерные изменения выявляли в обоих коленных суставах, сторону оперативного вмешательства определял болевой синдром, который преобладал в правом коленном суставе у 18 (43 %), в левом – у 24 (57 %) пациентов.
Критерии включения в исследование: идиопатический гонартроз 2 степени, РС II (Kellgren J.H., Lawrence J.S.), ФН-I. На рентгенограммах – потеря суставного хряща в медиальном тибиофеморальном отделе до 50 %, субхондральный остеосклероз в наиболее нагружаемой части мыщелков костей, остеофитоз в области межмыщелкового возвышения и суставных концов костей.
Критерии исключения: последствия травм, разрывы связок и менисков, гонартроз 3 степени (деформации мыщелков костей, нарушение оси конечности).
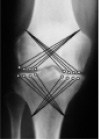
Применяемый для туннелизации способ введения спиц не позволял проводить исследования в отдельном мыщелке кости (рисунок, а), поэтому, был разработан особый способ введения спиц. Известно, что интрамедуллярные и окружающие кость (параоссальные) ткани разделяет компактная кость, имеющая высокое электрическое сопротивление, и электрический ток по этим тканям течёт раздельно [5]. Электрический ток течёт преимущественно через проводник с низким сопротивлением, и для его замыкания в интрамедуллярных тканях стали снижать их электрическое сопротивление, уменьшая межэлектродное расстояние относительно параоссальных тканей.
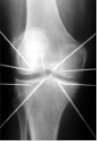
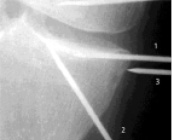
Оперативное вмешательство проводили под спинномозговой анестезией, начинали с введения спиц для исследований. Первую спицу вводили с помощью электродрели, отступив от суставной поверхности мыщелка кости 10-15 мм и под углом к ней 10 ° на глубину 20 мм. Вторую спицу – из основания метафиза того же мыщелка кости так, чтобы она не достигла субхондральной кости. Затем осторожными ударами внедряли вторую спицу в субхондральную кость: при продвижении в губчатом веществе удар приводил к появлению глухого звука, контакт со склерозированной субхондральной костью – к повышению тональности звука. Положение спиц уточняли с помощью рентгенографии (рисунок, б). Затем, отступив от первой спицы 1 см кзади, в мягкие ткани до упора в каждый мыщелок кости вводили третью спицу (рисунок, в).
Для регистрации изменений кровенаполнения применяли биполярную реовазографию. Электродами для регистрации импеданса интрамедуллярных тканей служили первая и вторая спицы; параоссальных тканей – вторая и третья спицы. Исследования проводили с помощью полианализатора РГПА-6/12 «РЕАН-ПОЛИ» (МЕДИКОМ-МТД, г. Таганрог). Частота зондирующего тока 56 кГц. Одновременно регистрировали электрокардиограмму во II стандартном отведении, импеданс, реовазограммы интрамедуллярных (РВГи) и параоссальных (РВГп) тканей и их первые производные. Регистрацию и расчёт величин с учётом калибровочного сигнала обеспечивал полианализатор.
а б в
Рис. а. Схема. Применяемый способ введения спиц при туннелизации мыщелков костей. б. Рентгенограмма. Введены спицы для исследований интрамедуллярных тканей нагружаемых участков мыщелков костей. в. Рентгенограмма. В наружный мыщелок большеберцовой кости введены спицы 1 и 2 для исследований интрамедуллярных тканей, в мягкие ткани – спица 3 для обеспечения исследований параоссальных тканей
Для количественного анализа были выбраны следующие параметры [3, 5]. Базисный импеданс интрамедуллярных (БИи, Ом) и параоссальных (БИп, Ом) тканей, зависит от количества электролита, в основном, кровенаполнения межэлектродного пространства. Время распространения пульсовой волны от зубца Q ЭКГ до начала пульсовой волны (ВРПВ, с), определяется плотностью стенок артерий. Амплитуда быстрого кровенаполнения пульсовой волны (АБКН, Ом), эквивалент пульсового кровенаполнения, отражающий приток крови до влияния резестивных сосудов. Показатель периферического сосудистого сопротивления (ППСС, %), характеризует упругость стенок резистивных сосудов. Реографический индекс (РИ, Ом), эквивалент максимального пульсового кровенаполнения. Объёмная скорость кровотока (Vq100, мл/мин) – количество крови, проходящей через 100 см3 тканей в минуту. Vq100 = (6000 * tg а * Тиз. * к) / (RR * БИ * Ак), где 6000 – коэффициент; tg a – амплитуда первой производной (амплитуда / время быстрого кровенаполнения пульсовой волны), Ом/с; Тиз. – период изгнания по Карпману (Тиз. = 0,109 х (RR + 0,159), с; RR – продолжительность пульсовой волны на ЭКГ, с. Реографический показатель РП (ед) – эквивалент пульсового кровенаполнения тканей с сопротивлением 1 Ом. Индекс венозного оттока (ИВО, %) и диастолический индекс (ДСИ, %), амплитудный и частотный показатели венозного оттока. Дикротический индекс (ДКИ, %), характеризует капиллярный кровоток.
Из полученных данных составляли не взвешенные вариационные ряды. Анализ с помощью программы Мicrosoft Exel 2010: вычисляли среднюю арифметическую и её ошибку. Достоверность различий между средними определяли с помощью парного критерия t-Стъюдента.
Результаты исследований и их обсуждение
Межэлектродное расстояние в интрамедуллярных тканях мыщелков костей не превышало 1,5 см, в параоссальных тканях составляло 6-7 см: в интрамедуллярных тканях было в 4 раза меньше. Величина БИи составляла в наружных мыщелках бедренных костей 73 % (p < 0,01), внутренних мыщелках бедренных костей 66 % (p < 0,001), наружных мыщелках большеберцовых костей 80 % (p < 0,05), внутренних мыщелках большеберцовых костей 63 % (p < 0,001) от величины БИп соответственно.
В мыщелках большеберцовых костей различия между параметрами кровообращения были статистически недостоверны. Во всех мыщелках костей различия между ВРПВ, ДКИ, ЖСИ и ИВО были статистически недостоверны (табл. 1 и 2).
Таблица 1
Параметры кровообращения в мыщелках бедренных и большеберцовых костей, n = 42
|
Параметры |
Наружные мыщелки бедренных костей |
Внутренние мыщелки бедренных костей (100 %) |
% |
p < |
|||||
|
1 |
ВРПВ, мс |
0,201 |
± |
0,005 |
0,197 |
± |
0,004 |
102 |
- |
|
2 |
БИ и, Ом |
88,68 |
± |
6,06 |
95,37 |
± |
7,32 |
93 |
- |
|
3 |
БИ п, Ом |
121,23 |
± |
8,37 |
145,43 |
± |
11,28 |
83 |
- |
|
4 |
ППСС, % |
98,95 |
± |
3,35 |
77,88 |
± |
3,63 |
127 |
0,001 |
|
5 |
АБКН, Ом |
0,0093 |
± |
0,0012 |
0,0159 |
± |
0,0028 |
58 |
0,05 |
|
6 |
РИ, Ом |
0,0216 |
± |
0,0025 |
0,0347 |
± |
0,0053 |
62 |
0,05 |
|
7 |
Vq100, см3 в 100 мл ткани |
3,069 |
± |
0,230 |
5,634 |
± |
1,279 |
69 |
0,05 |
|
8 |
Рп, промилле |
0,235 |
± |
0,017 |
0,347 |
± |
0,028 |
68 |
0,01 |
|
9 |
ДКИ, % |
35,57 |
± |
2,90 |
35,78 |
± |
3,29 |
99 |
- |
|
10 |
ДСИ, % |
39,45 |
± |
3,65 |
37,10 |
± |
3,05 |
106 |
- |
|
11 |
ИВО, % |
17,83 |
± |
2,18 |
13,24 |
± |
1,64 |
135 |
- |
|
Наружные мыщелки большеберцовых костей |
Внутренние мыщелки большеберцовых костей (100 %) |
||||||||
|
12 |
ВРПВ, мс |
0,207 |
± |
0,004 |
0,205 |
± |
0,003 |
101 |
- |
|
13 |
БИ и, Ом |
125,85 |
± |
8,34 |
110,81 |
± |
7,91 |
114 |
- |
|
14 |
БИ п, Ом |
156,63 |
± |
10,02 |
175,31 |
± |
13,25 |
89 |
- |
|
15 |
ППСС, % |
88,98 |
± |
3,40 |
88,33 |
± |
3,56 |
101 |
- |
|
16 |
АБКН, Ом |
0,0219 |
± |
0,0035 |
0,0218 |
± |
0,0028 |
100 |
- |
|
17 |
РИ, Ом |
0,0597 |
± |
0,0069 |
0,0525 |
± |
0,0058 |
114 |
- |
|
18 |
Vq100, см3 в 100 мл ткани |
4,516 |
± |
0,645 |
4,743 |
± |
0,388 |
95 |
- |
|
19 |
Рп, промилле |
0,453 |
± |
0,041 |
0,449 |
± |
0,025 |
101 |
- |
|
20 |
ДКИ, % |
33,00 |
± |
2,36 |
43,52 |
± |
7,22 |
84 |
- |
|
21 |
ДСИ, % |
37,71 |
± |
3,19 |
34,88 |
± |
2,49 |
108 |
- |
|
22 |
ИВО, % |
15,45 |
± |
2,48 |
14,39 |
± |
1,21 |
107 |
- |
Таблица 2
Соотношение параметров кровообращения в мыщелках бедренной и большеберцовой костей, n = 42
|
Строки |
Наружные мыщелки бедренных / большеберцовых костей |
% |
p < |
Внутренние мыщелки бедренных / большеберцовых костей |
% |
p < |
|
1-12 |
ВРПВ, мс |
97 |
- |
ВРПВ, мс |
96 |
- |
|
2-13 |
БИ и, Ом |
70 |
0,001 |
БИ и, Ом |
86 |
- |
|
4-15 |
ППСС, % |
111 |
0,05 |
ППСС, % |
88 |
0,05 |
|
5-16 |
АБКН, Ом |
42 |
0,01 |
АБКН, Ом |
73 |
- |
|
6-17 |
РИ, Ом |
36 |
0,001 |
РИ, Ом |
66 |
0,05 |
|
7-18 |
Vq100, см3 в 100 мл ткани |
68 |
0,05 |
Vq100, см3 в 100 мл ткани |
94 |
- |
|
8 – 19 |
Рп, промилле |
52 |
0,001 |
Рп, промилле |
77 |
0,01 |
|
9 – 20 |
ДКИ, % |
108 |
- |
ДКИ, % |
91 |
- |
|
10 – 21 |
ДСИ, % |
105 |
- |
ДСИ, % |
106 |
- |
|
11 – 22 |
ИВО, % |
115 |
- |
ИВО, % |
92 |
- |
Различия между БИи наружного и внутреннего мыщелков бедренных костей, а также наружного и внутреннего мыщелков большеберцовых костей, не имели статистически достоверных различий (табл. 1). В наружных мыщелках бедренных костей БИи составил 70 % (p < 0,001) от величины в наружных мыщелках большеберцовых костей; во внутренних мыщелках бедренных костей – 86 % от величины во внутренних мыщелках большеберцовых костей (табл. 2).
В наружных мыщелках бедренных костей ППСС составил 126 % (p < 0,001) от величины во внутренних мыщелках этих костей (табл. 1). В наружных мыщелках бедренных костей ППСС составил 111 % (p < 0,05) от величины в наружных мыщелках большеберцовых костей; во внутренних мыщелках бедренных костей – 88 % (p < 0,05) от величины во внутренних мыщелках большеберцовых костей (табл. 2).
В наружных мыщелках бедренных костей составили АБКН 58 % (p < 0,05), РИ – 62 % (p < 0,05), Vq100 69 % (p < 0,05), РП 68 % (p < 0,01) от величин во внутренних мыщелках этих костей (табл. 1). В наружных мыщелках бедренных костей составили АБКН 42 % (p < 0,01), РИ – 36 % (p < 0,001), Vq100 68 % (p < 0,05), РП 52 % (p < 0,001) от величин в наружных мыщелках большеберцовых костей. Во внутренних мыщелках бедренных костей составили АБКН 73 %, РИ 66 % (p < 0,05), РП 77 % (p < 0,01) от величин во внутренних мыщелках большеберцовых костей (табл. 2).
Базисный импеданс интрамедуллярных тканей был меньше базисного импеданса параоссальных тканей. Так как электрический ток замыкается по проводнику, сопротивление которого меньше, его замыкание происходило в интрамедуллярных тканях и обеспечивало проведение исследований.
Сопоставления выявили асимметрию параметров пульсового кровотока в мыщелках бедренных костей и отсутствие таковой в мыщелках большеберцовых костей. При этом различия между параметрами, характеризующими микроциркуляцию и венозный отток, во всех мыщелках костей были статистически недостоверны. Из этого следует, что при клинико-рентгенологических проявлениях гонартроза 2 степени сначала появилась асимметрия пульсового кровенаполнения в мыщелках бедренных костей, которая обеспечивала соответствие микроциркуляции в мыщелках этих костей таковой в мыщелках большеберцовых костей.
Известно, что в зависимости от сокращения и расслабления гладкой мускулатуры стенок артерий меняется сопротивление току крови; время распространения пульсовой волны зависит от плотности стенок артерий [2]. Так как различия между ВРПВ до всех мыщелков костей были статистически недостоверны: плотность стенок артерий, обеспечивающих приток крови, не имела значимых различий, артерии не создавали асимметрию притока крови.
Известно, что показатель периферического сосудистого сопротивления характеризует упругость стенок резистивных сосудов; уменьшение упругости стенок приводит к увеличению просвета (вазодилатация) этих сосудов, и давление крови в микроциркуляторном русле повышается, ток крови усиливается [2, 3]. Во внутренних мыщелках бедренных костей ППСС был меньше, чем в наружных мыщелках этих костей. Из этого следует, что резистивные сосуды внутренних мыщелков бедренных костей были в состоянии дилатации и обеспечивали относительное усиление тока крови. И во внутренних мыщелках бедренных костей регистрировали увеличение объёмной скорости кровотока и реографического показателя относительно величин в наружных мыщелках костей.
В наружных мыщелках бедренных костей ППСС был больше, чем в наружных мыщелках большеберцовых костей. Во внутренних мыщелках бедренных костей – меньше, чем во внутренних мыщелках большеберцовых костей. В мыщелках большеберцовых костей ППСС не имел статистически достоверных различий, поэтому, относительно резистивных сосудов большеберцовых костей в наружных мыщелках бедренных костей резистивные сосуды были в состоянии спазма, во внутренних мыщелках бедренных костей – в состоянии дилатации. Резистивные сосуды перераспределяли кровоток между мыщелками бедренных костей, создавали его асимметрию.
При реографии базисный импеданс обратно пропорционален кровенаполнению тканей [3]. Между базисным импедансом интрамедуллярных тканей мыщелков бедренных костей, а также большеберцовых костей соответственно, различия были статистически недостоверны. Однако базисный импеданс интрамедуллярных тканей мыщелков бедренных костей был меньше, чем большеберцовых костей: кровенаполнение мыщелков бедренных костей было больше. На основании этого, асимметрия параметров пульсового кровотока была на фоне «общего» увеличения кровенаполнения мыщелков бедренных костей. Так как при гонартрозе одной из причин ноющих болей служит внутрикостная гипертензия, появляющаяся вследствие повышения венозного давления крови [9], вероятно, увеличение кровенаполнения мыщелков бедренных костей отражало наличие венозной гиперемии.
В наружных мыщелках бедренных костей параметры, характеризующие пульсовой приток крови, были меньше, чем в мыщелках большеберцовых костей. Во внутренних мыщелках бедренных костей – тоже меньше или приближались до недостоверных отличий к величинам в мыщелках большеберцовых костей. Несмотря на то, что резистивные сосуды ограничивали приток крови к наружным мыщелкам бедренных костей и создавали условия для его увеличения во внутренних мыщелках бедренных костей, его компенсация во внутренних мыщелках бедренных костей была недостаточна. Вероятно, только в покое она обеспечивала соответствие микроциркуляции и венозного оттока крови в мыщелках бедренных костей таковой в мыщелках большеберцовых костей.
Приведенные данные обосновывают предположение, что появление асимметрии тока крови было следствием ограничения притока крови к интрамедуллярным тканям внутренних мыщелков бедренных костей. В условиях покоя компенсация недостаточности кровообращения была достаточна, что выражалось в соответствии микроциркуляции и венозного оттока в мыщелках бедренных костей таковым в мыщелках большеберцовых костей. Однако при нагрузках спазм резистивных сосудов наружных мыщелков бедренных костей и недостаточная компенсация пульсового тока крови во внутренних мыщелках бедренных костей могли стать причинами недостаточности кровообращения – ишемии, которая проявляется болью, в частности, в суставном конце кости. В покое микроциркуляция постепенно восстанавливалась, и боль исчезала. В условиях ишемии возрастает свёртываемость крови, появляются тромбозы венозного русла, служащие причиной венозной гиперемии и повышения давления интерстициальной жидкости, которое клинически проявляется стойкими болями покоя [2, 9].
Таким образом, у пациентов с гонартрозом 2 степени в условиях покоя и спинномозговой анестезии выявлена асимметрия параметров пульсового тока крови в интрамедуллярных тканях мыщелков бедренных костей при отсутствии таковой в мыщелках большеберцовых костей. Причиной асимметрии был спазм резистивных сосудов наружных мыщелков бедренных костей и дилатация резистивных сосудов внутренних мыщелков бедренных костей. И результатом было соответствие микроциркуляции и венозного оттока в мыщелках бедренных костей таковым в мыщелках большеберцовых костей в покое.
Выводы
Предлагаемый способ введения спиц позволяет проводить исследования в интрамедуллярных тканях, в частности, мыщелков бедренной и большеберцовой костей.
При гонартрозе 2 степени изменения кровообращения в мыщелках большеберцовых костей не выражены.
В бедренной кости за счёт резистивных сосудов происходит перераспределение тока крови, которое в покое обеспечивает компенсацию недостаточности кровообращения во внутреннем мыщелке бедренной кости за счёт ограничения кровообращения в наружном мыщелке бедренной кости.
Библиографическая ссылка
Свириденко А.С., Бунов В.С., Бирюкова М.Ю., Люлин С.В., Мещерягина И.А. ОСОБЕННОСТИ КРОВООБРАЩЕНИЯ В МЫЩЕЛКАХ БЕДРЕННОЙ И БОЛЬШЕБЕРЦОВОЙ КОСТЕЙ ПРИ ГОНАРТРОЗЕ 2 СТЕПЕНИ // Международный журнал прикладных и фундаментальных исследований. 2016. № 3-1. С. 94-99;URL: https://applied-research.ru/en/article/view?id=8679 (дата обращения: 03.05.2026).

