Scientific journal
International Journal of Applied and fundamental research
ISSN 1996-3955
ИФ РИНЦ = 0,556
MODELING SPREADING MATERIAL IN UNDER-STRATUM OF ATMOSPHERE
Примесь называется пассивной, если вплоть до выпадения на поверхность земли она не изменяется. Если же она в процессе распространения в атмосфере вступает в химические реакции с водяным паром или с другими компонентами атмосферы или же переходит из одного химического состояния в другое, то такую примесь будем называть активной.
Рассмотрим случай двумерного распространения вещества (аэрозоля) в нижнем слое атмосферы, где цепочка его превращения из одного химического состояния в другое согласно теории Михаэлса-Ментена состоит из трех звеньев. Принимаем, что свободное химическое вещество в воздухе (субстрат) сначала создают в ходе обратимой реакции воздушную смесь (комплекс), которая, в свою очередь, необратимо распадается, образуя вновь свободное химическое вещество и продукт [1].
Под активным понимается только такое количество реагентов, которое фактически участвует в реакции. Если обозначить через s, e, st, p, соответственно концентрацию субстрата, химического вещества, смеси и продукта, то согласно закону действующих масс имеем
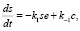
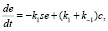
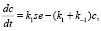
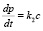 (1)
(1)
где k1, k2 – скорости прямой и обратной реакции: k2 – скорость реакции распада смеси.
Система (1) может быть записана с учетом диффузии, для описания которой используется баланс реагента Φ:
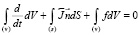 (2)
(2)
Здесь первый интеграл описывает скорость изменения реагента (p в объеме V), второй интеграл – поток (за единицу времени) (p из V через поверхность dS), третий интеграл – скорость уменьшения (p в V в результате реакции), n – единичная внешняя нормаль к поверхности S. Из (2)
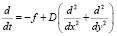
где D – коэффициент диффузии. Рассмотрим двумерный слой единичной толщины, где происходит диффузия химического вещества. В примеси имеется компонет воздуха который обратимо соединяется с веществом.
Обозначим через Dr и Df коэффициенты диффузии компонента воздуха и реагента соответственно. Уравнения баланса для концентрации компоненты воздуха, реагента и смеси реагент – воздуха записываются в виде
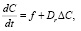
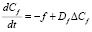
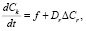
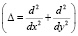
где Cr и Cf – концентрации реагента и смеси воздух – реагент. Функцию согласно (1) можно представить в виде (k3 = 0).
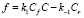
Если учитывать перенос вещества течением воздуха по направлениям осей ОХ и ОY со скоростями u и v соответственно, то
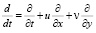
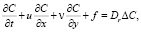 (3)
(3)
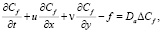
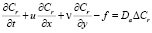
Система (3) описывает процесс распространения активной примеси с учетом диффузии, химической реакции и переноса вещества течением воздуха.
Иной подход к описанию перехода части аэрозольных соединений в другие формы (под действием химической реакции) предложен в работе Г.И. Марчука [2]. При этом механизм реакции перехода детально не рассматривается, а используется только последовательность звеньев цепочки превращения. Например, для трехзвенной цепочки в двумерном случае имеем
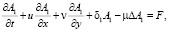
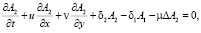 (4)
(4)
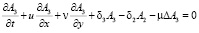
где А – коэффициент турбулентной диффузии; F – интенсивность источника появления аэрозольного соединения.
Если использовать уравнения кинетики обмена вещества между химическими реагентами в составе воздушной массы, где скорости обмена будут пропорциональны разности концентрации.
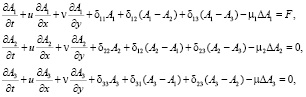 (5)
(5)
Системы уравнения (4) и (5) в отличие от 3 являются линейными, что существенно упрощает математическое описание процесса распространения и превращения аэрозольного соединения в атмосфере.
При расчете выбросов вредных веществ в атмосферу для каждого вещества, выбрасываемого источниками проверяется условие [3].
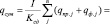
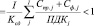 (6)
(6)
где Спр.j – приземная концентрация j – вещества; Сф.j – фонофая концентрация этого вещества.
В случае когда гигиеническое воздействие вредных веществ зависит от совместного присутствия группы веществ, обладающих эффектом «суммарного воздействия», введено дополнительное требование Минздрава:
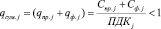 (7)
(7)
где Kсд – коэффициент комбинации совместного гигиенического действия группы веществ.
Таким образом, не только систематизация известных физика-химических свойств и закономерностей аэрозолей, но и необходимость более глубоких дальнейщих исследований аэрозоля как актуальную проблему в ряде смежных отраслей науки и техники. Наличие взвешенных примесей является нежелательным фактом и на определенном этапе возникает необходимость осаждения и извлечение того или иного количественного изменения, либо, наконец, ее полного или частично уничтожения.
Библиографическая ссылка
Абдула Ж., Галагузова Т.А., Аяпбергенова А. МОДЕЛИРОВАНИЕ РАСПРОСТРАНЕНИЕ ВЕЩЕСТВА В НИЖНЕМ СЛОЕ АТМОСФЕРЫ // Международный журнал прикладных и фундаментальных исследований. 2016. № 3-1. С. 174-176;URL: https://applied-research.ru/en/article/view?id=8697 (дата обращения: 03.05.2026).

