Scientific journal
International Journal of Applied and fundamental research
ISSN 1996-3955
ИФ РИНЦ = 0,556
REGULARITIES OF SORPTION OF MANGANESE IONS (II) BY KAOLINITE
Актуальной задачей современности является повышение степени эффективности извлечение тяжелых металлов из сточных вод. Известно, что тяжелые металлы являются стойкими химическими загрязнителями, обладающие специфическими токсическими свойствами. В сточных водах, а также в природных подземных водах, как правило, содержатся соединения марганца [2].
При очистке сточных вод от ионов цветных и тяжелых металлов практическая задача заключается в подборе местных природных материалов. В связи с этим целью настоящей работы явилось изучение сорбционной способности каолинита при извлечении ионов марганца из водных растворов.
Материалы и методы исследования
Исследована сорбционная способность каолинита по отношению к ионам марганца (II) на природном сорбенте. Для изучения процесса сорбции использовали природный минерал – каолинит. Для исследования брали фракцию каолинита с размером частиц 2,5÷3,5 мм.
Эксперимент проводили при температурах 298, 318 и 333 К. Сорбцию ионов марганца на каолините изучали в статических условиях из нитратных растворов с концентрациями от 0,05 М до 0,16 М. Сорбент в количестве 1 г заливали 50 мл растворами. Контакт сорбента с раствором продолжался до установления равновесия в течение 7 суток [6]. Затем сорбент и раствор отделяли и анализировали на содержания ионов марганца и измеряли рН среды. Концентрацию ионов марганца в растворе определяли по методике [5].
Количество вещества, сорбированного единицей массы сорбента Г, ммоль/г, рассчитывали по формуле:
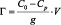 ,
,
где С0 – концентрация марганца в исходном растворе, ммоль/л; Ср – равновесная (остаточная) концентрация извлекаемого иона марганца в растворе, ммоль/л; V – объем раствора, мл; g – масса сорбента, г.
По полученным результатам строили изотермы сорбции, дающие основные сведения о сорбционных свойствах материала и характере сорбции на нем определенных веществ.
Результаты исследования и их обсуждение
Перед рассмотрением и анализом экспериментальных данных по изучению основных закономерностей сорбции ионов Mn (II), рассмотрим ионное состояние исходных растворов. В водных растворах свободные ионы марганца (II) практически не существуют вследствие сильной гидратации. При образовании исходных растворов нитратов марганца происходит гидратообразование с выделением плохо растворимого гидроксида Mn(OH)2, а также гидролиз ионов марганца. Оба этих эффекта способны оказывать влияние на результаты сорбции. В 1М растворах начальная величина водородного показателя среды при начале гидратообразования рНгидр. для Mn2+ равна 7,8 [4], в случае 0,01М растворов Mn2+ 8,8 [4], а при полном осаждении, где автор принимает концентрацию 10–5 М, рНгидр. составляет 10,4 [4].
В связи со снижением в процессе сорбции концентраций Mn2+, гидролизующихся по уравнению
Mn 2+ + HOH ↔ MnOH+ + H+ ,
происходит непрерывное изменение водородного показателя среды. Величина рН может быть рассчитана из зависимости (КW = 10-14)
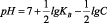 ,
,
где lgKВ и С – соответственно константа диссоциации слабого основания, образующего соль по второй ступени, равная для Mn(OH)2 (5·10-4) [4]. Результаты расчетов показали, что по мере снижения содержания ионов Mn2+ рН раствора существенно возрастает. Эти данные подтверждают и экспериментальные измерения рН растворов до и после сорбции ионов марганца (II) на каолините (рис. 1).
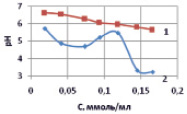
Рис. 1. Зависимость рН раствора нитрата марганца от концентрации ионов Mn (II): исходных растворов до сорбции (1) и растворов после сорбции (2)
Для установления закономерностей сорбции ионов марганца (II) на каолините было изучено влияние концентрации исходного раствора и температуры на величину сорбции. В результате было установлено, что с увеличением концентрации ионов марганца (II) возрастает величина удельной сорбции. Полученные данные показывают, что сорбционная емкость при температуре 298 К составляет 0,031 ммоль/г; при 318 К – 0,063 ммоль/г и при 333 К – 0,075 ммоль/г. Таким образом, сорбционная емкость возрастает с ростом температуры.
В результате сорбции наблюдается конкуренция двух видов межмолекулярных взаимодействий: гидратация ионов металлов и взаимодействие ионов металлов с сорбентом [1]. С увеличением концентрации сорбция на исходном каолините возрастает и в области 0,1 ммоль/мл наблюдается перегиб (рис. 2), указывающий на изменение механизма сорбции. На первой ступени сорбции марганца предельное значение не достигается и выше отмеченной концентрации сорбция проходит одновременно на различных активных центрах. Сорбция проходит по ионообменному механизму по схеме:
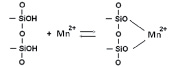
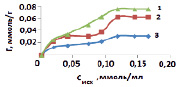
Рис. 2. Зависимость сорбции ионов марганца из растворов нитрата марганца (II) на каолините при температуре, К: 1 – 298, 2 – 318, 3 – 333
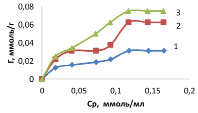
Рис. 3. Изотермы сорбции ионов марганца на каолините при температуре, К: 1 – 298; 2 – 318; 3 – 333
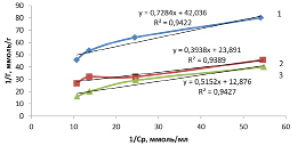
Рис. 4. Изотерма сорбции ионов марганца (вторая ступень) в линейных координатах уравнения Ленгмюра при температуре: 1 – 298; 2 – 318; 3 – 333
Расчеты изотерм сорбции ионов марганца на каолините
|
Температура, К |
1 ступень |
2 ступень |
||||
|
Г∞, ммоль/г |
КL, г/ммоль |
R2 |
Г∞, ммоль/г |
КL, г/ммоль |
R2 |
|
|
298 |
8,33 |
46,25 |
1,0 |
1,37 |
57,57 |
0,942 |
|
318 |
11,38 |
39,59 |
0,992 |
2,54 |
60,79 |
0,938 |
|
333 |
1,94 |
0,15 |
0,943 |
1,96 |
24,99 |
0,942 |
На второй ступени сорбции ионов марганца (II) также происходит по ионообменному механизму, но на менее доступных активных центрах, находящихся в участках каолинита с более высокой степенью дисперсности.
Изотермы сорбции ионов марганца (II) (рис. 3) принадлежат к изотермам IV типа по классификации БЭТ [3], которым характерна конечная адсорбция при приближении к насыщению концентрации.
Выявление сорбционных параметров предельной удельной сорбции Г∞ и константы, указывающей на сродство сорбата к сорбенту, проведено обработкой результатов в соответствии с линейной формой уравнения Ленгмюра [2]:
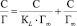 ,
,
где Г∞ – предельная емкость сорбента, ммоль/г; Г – количество сорбированных ионов Mn2+, ммоль/г; КL – константа сорбционного взаимодействия, характеризующая интенсивность сорбции, л/ммоль, С – равновесная концентрация, ммоль/л.
Линейная изотерма (рис. 4) позволяет графически определить оба постоянных параметра сорбционной изотермы Лэнгмюра (Г∞ и КL). Экстраполяция прямолинейной изотермы до оси ординат дает отрезок, равный 1/(Г∞·КL), а тангенс угла наклона прямой tg∞ = 1/Г∞ [7]. Рассчитанные значения постоянных уравнения Лэнгмюра приведены в таблице.
Параметр сорбционного взаимодействия (КL) характеризует энергию взаимодействия сорбата с сорбентом. Чем сильнее это взаимодействие, тем больше его величина. Как видно из таблицы, что чем выше температура процесса, тем больше ослабевает взаимодействие сорбата с сорбентом.
Заключение
Установлено, что каолинит обладает высокой сорбционной способностью по отношению к ионам марганца. Изотермы сорбции ионов марганца (II) в широком интервале концентраций раствора нитрата марганца подчиняется уравнению Ленгмюра; рассчитаны предельные значения сорбции.
Библиографическая ссылка
Пимнева Л.А., Королева М.Н., Казанцева А.В. ЗАКОНОМЕРНОСТИ СОРБЦИИ ИОНОВ МАРГАНЦА (II) КАОЛИНИТОМ // Международный журнал прикладных и фундаментальных исследований. 2016. № 4-3. С. 545-547;URL: https://applied-research.ru/en/article/view?id=9009 (дата обращения: 04.05.2026).

