Scientific journal
International Journal of Applied and fundamental research
ISSN 1996-3955
ИФ РИНЦ = 0,556
RADIOLYSIS OF PHENOL IN WATER SOLUTIONS IN THE PRESENCE OF NANO-Y-AL2O3
Несмотря на интенсивное исследование радиолитического разложения фенола в водных растворах [1-8], гетерогенный радиолиз этой системы изучен недостаточно. Особенно слабо изучено влияние нано частиц на радиолитическое разложение фенола в водных растворах [7-8].
В данной работе изучено изменение pH показателя, Химическое Потребления Кислорода (ХПК) и образование СО2 при радиолизе водного раствора фенола (10-2М) в присутствии нано-γ Al2O3 в интервале поглощенной дозы 0-400 кГр. Кроме того, изучена кинетика образования экзотермических эффектов при радиолизе водного раствора фенола (10-2М) в присутствии нано-γ Al2O3 под действием γ-излучения Со60.
Подготовлены образцы с концентрацией фенола 10-2 М. В раствор добавлены 0,2 г нано-γ Al2O3, которая имела следующие характеристики.
|
Чистота |
99.99 % |
|
Состав |
Нано-порошок, белый |
|
Размеры частицы D50 |
20нм |
|
Удельная поверхностная площадь |
262.09 м2/г |
|
Содержание гамма фазы |
99.32 % |
|
Содержание воды |
0.317 % |
|
Примеси |
Ca: 8.25 ppm Fe: 7.967 ppm K: 6.3 ppm Na: 4.707 ppm Si: 9.71 ppm |
Облучение проводилось в стеклянных ампулах, в статических условиях, при комнатной температуре под действием γ излучения от Со60. Мощность поглощенной дозы составляла 0,21 Гр/с. рН измеряли с прибором «РHS-25 pH METER», а Химическое Потребление Кислорода (ХПК) с титриметрическим методом.
После облучения подготовлены двух видов образцов. В первом случае анализирован жидкие фазы облученных образцов на ХПК и рН показателя. Во втором случае образцы помещали в центрифуге и отделяли нано частиц от жидкой фазы. Для выделения Al2O3 использована центрифуга «Centrifuge 5804R» фирмы «Eppendorf».Образцы (1 мл) поместили в цилиндрическую ячейку центрифуга объемом 50 мл, скорость вращения составляла 5000 оборот/мин. Время вращения 5 мин.
Жидкая фаза анализированы на ХПК и рН показателя.СО2 анализировали хроматографически. Al2O3 собранная на дне ячейки после окончания вращения удаляли механически, осушили в воздухе в течение 1 суток и анализировали на Дериватографе «Perlin Elmer» STA 6000.
В программе «Pyris Manger» из окно «PyrisSeries-STA6000 COM-1» создается рабочие связи с компьютерным прибором. При повышении температуры во время горения для создания гомогенности и выделения продуктов горения из система, обеспечивается подача азота со скоростью 20 мл/минут.
Площади эндо и экзотермических эффектов, вычисленные из термических кривых определяется как энтальпия, реакции горения.
На рис. 1. представлены кинетические кривые изменения рН облученных систем, включающие радиолиз гомогенной системы фенол-вода системы нано-γ-Al2O3 с вращением образцов и без вращения.
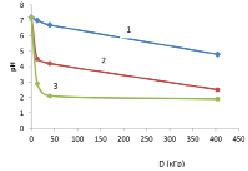
Рис. 1. Зависимости pH показателя от поглощенной дозы, 1 – после вращения, 2 – до вращения, 3 – без Al2O3 (гомогенная смесь)
Как видно, рН сильно уменьшается в случае гомогенной системы. При облучении системы в присутствии нано-γ Al2O3 рН изменяется относительно слабо. По видимому, часть жидких продуктов кислотного характера адсорбируется на поверхности нано-γ Al2O3. Неожиданное изменение рН наблюдается в случае вращения образцов. В этом случае уменьшение рН меньше, чем упомянутых выше двух случаях. Полученные результаты показывают о дополнительной адсорбции кислот на поверхности нано-γ Al2O3 при вращении на центрифуге.
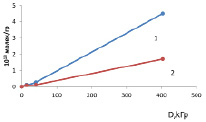
Рис. 3. Кинетика образования СО2 при радиолизе, 1 – гомогенной системы Ph + вода, 2 – системы Ph + Al2O3 + H2O
На рис. 2 показаны кинетические кривые изменения ХПК облученных систем, включающие радиолиз гомогенной системы фенол-вода, системы нано-γ-Al2O3 с вращением образцов и без вращения.
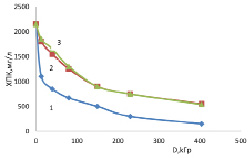
Рис. 2. Зависимости ХПК показателя от поглощенной дозы, 1 – после вращения, 2 – до вращения, 3 – без Al2O3 (гомогенная смесь)
Как видно, наличие нано-γ Al2O3 существенно не влияет на уменьшение ХПК с ростом дозы. Отличие наблюдается в случае вращения образцов на центрифуге. В этом случае происходит более сильное уменьшение ХПК с ростом дозы. Такая закономерность также подтверждает адсорбции жидких продуктов кислотного характера на поверхности нано-γ Al2O3 при вращении на центрифуге.
На рис. 3 показаны кинетика изменения концентрация углекислого газа при радиолизе гомогенной и гетерогенной системы.
Как видно, наличие нано-γ-Al2O3 приводит к уменьшению концентрации образовавшийся углекислого газа. Полученные результаты показывают на подавление окисление органических кислот – продуктов глубокого окисления фенола. Наблюдаемая тенденция в кинетике образования СО2 была наблюдена также в работе [7], где проводилось исследование влияние нано-γ Al2O3 на радиолитическое разложение фенола в водных растворах.
На рис. 4 представлены кривые изменения веса, ?H и площадь экзотермического эффекта.
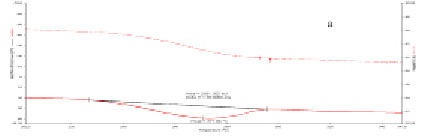
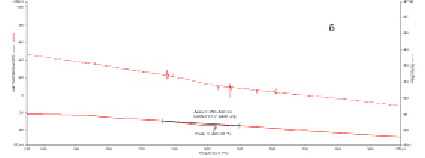
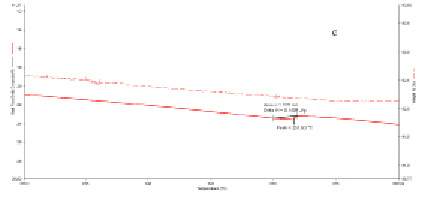
Рис. 4. Дериватограммы образцов при а – D = 0, б – D = 13 kГр, с – D = 38 kГр
Как видно, уменьшение веса образца наблюдается при t = 228-295 °C. Экзотермический эффект происходит с максимумом, зависящего от поглощенной дозы. Результаты представлены в таблице.
Характеристики экзотермического эффекта
|
D |
S, мДж |
?H, Дж /г |
Тмах, °С |
|
0 |
2101.153 |
69.600 |
275.06 |
|
13 kГр |
256.442 |
256.442 |
265.33 |
|
38 kГр |
1.729 |
0.1409 |
251.63 |
|
380kГр |
~ 0 |
~ 0 |
Не наблюдается |
Как видно, с ростом дозы теплота образования и площадь экзотермического эффекта сильно падает, что связано с разложением фенола и продуктов его превращения при больших дозах. Наблюдается также смешение Тмакс в сторону низких температур при больших дозах.
На DTA привой, снятой для не облученной нано-γ-Al2O3 наблюдается эффект при 470 °С.
Наблюдаемые закономерности показывают на эффективное участие активных частиц, образующихся на поверхности нано-γ Al2O3 в процессах разложения фенола и органической части продуктов его превращения при радиолизе системы вода – нано-γ-Al2O3 – фенол.
Библиографическая ссылка
Курбанов М.А., Кулиева У.А., Абдуллаев Е.Т., Махмудов О.М., Искендерова З.И. РАДИОЛИЗ ВОДНОГО РАСТВОРА ФЕНОЛА В ПРИСУТСТВИИ НАНО-Y-AL2O3 // Международный журнал прикладных и фундаментальных исследований. 2016. № 5-1. С. 21-24;URL: https://applied-research.ru/en/article/view?id=9174 (дата обращения: 11.05.2026).

