Scientific journal
International Journal of Applied and fundamental research
ISSN 1996-3955
ИФ РИНЦ = 0,556
DEVELOPMENT OF METHODS FOR IDENTIFICATION AND EVALUATION OF QUANTITATIVE CETYLPYRIDINIUM CHLORIDE
В последние годы четко наметилась тенденция поиска новых антимикробных средств, обладающих комплексным бактерицидным действием. В качестве таких веществ широко применяются четвертичные аммониевые соединения, высокая бактерицидная и поверхностная активность которых сочетается с низкой токсичностью, поэтому их применяют как эмульгаторы, смачиватели, стабилизаторы и дезинфицирующие средства в косметологии, медицине, бытовой химии. Среди четвертичных аммониевых солей в медицине применяется цетилпиридиния хлорид (ЦПХ) для местного лечения инфекционно-воспалительных процессов в полости рта и горла в составе пастилок и таблеток для рассасывания. Благодаря значительной увлажняющей способности и незначительному поверхностному натяжению ЦПХ деполяризует цитоплазматическую мембрану микроорганизмов, проникает в глубокие слои слизистой оболочки, оказывает бактерицидное действие [5].
Поэтому целью исследования явилась разработка методов идентификации и количественного определения цетилпиридиния хлорида.
Материалы и методы исследования
На первом этапе исследования проводили определение подлинности с помощью химических реакций. Выбор реакций обусловлен высокой чувствительностью, выраженным аналитическим эффектом реакций и доступностью реактивов. Было установлено, что ЦПХ взаимодействует с раствором калия иодида, спиртовым раствором йода, солями тяжелых металлов. Вступает в реакции окисления, комплексообразования и сплавления с фенолами.
Для идентификации и оценки степени чистоты цетилпиридиния хлорида использовали метод хроматографии в тонком слое сорбента (ТСХ), имеющий высокую чувствительность и селективность. Определение проводили на пластинках Сорбфил. Детектирование осуществляли парами йода и раствором реактива Драгендорфа. Для разработки методики спектрофотометрического определения ЦПХ предварительно были изучены спектры поглощения водных и спиртовых растворов препарата с различной концентрацией. Определение проводили на спектрофотомере СФ – 56 в кювете с толщиной рабочего слоя 10 мм в диапазоне длин волн 200 – 400 нм.
Для количественной оценки ЦПХ использовали титриметрические и физико- химические методы анализа. Аргентометрическое определение ЦПХ по методу Мора проводили по методике: около 0,05 г (точная навеска) препарата помещали в колбу для титрования, растворяли в 10 мл воды очищенной, добавляли 2 капли 5 % раствора калия хромата, тщательно перемешивали и титровали 0,1 М раствором серебра нитрата до кирпично – красного окрашивания осадка.
Кроме того, нами предложен вариант аргентометрического определения ЦПХ по методу Фольгарда, в модификации Кольтгоффа. Для этого около 0,05 г (точная навеска) препарата помещали в колбу для титрования, растворяли в 30 мл воды очищенной; добавляли 2 мл 10 % кислоты азотной, 1 мл железоаммонийных квасцов и 0,1 мл 0,1 М раствора аммония роданида, тщательно перемешивали и титровали 0,1 М раствором серебра нитрата до обесцвечивания. Параллельно проводили контрольный опыт.
Предварительные исследования показали возможность использования титрованных растворов йода в анализе препарата. Поэтому нами предложен вариант обратной йодиметрии. Титрование проводили по методике: около 0,05 г (точная навеска) препарата переносили в колбу с притертой пробкой. Добавляли 10 мл воды очищенной, 1 мл разведенной кислоты хлороводородной, взбалтывали, добавляли 5 мл 0,1 М раствора йода (УЧ 1/2), сразу закрывали пробкой, взбалтывали и оставляли на 15 минут в тёмном месте. Далее ополаскивали пробку водой и раствор титровали 0,1 М раствором натрия тиосульфата, до обесцвечивания раствора крахмала, который добавляли в конце титрования. Параллельно проводили контрольный опыт.
Для идентификации и количественной оценки содержания препарата в лекарственных формах изучили возможность использования УФ-спектрофотометрии [3] . Предварительно изучили характер УФ спектров поглощения в водных растворах. Для этого около 0,01 г (точная навеска) препарата помещали в мерную колбу вместимостью 50 мл, растворяли, доводили до метки водой очищенной и перемешивали. 2,5 мл аликвоты переносили в мерную колбу вместимостью 25 мл, доводили до метки водой очищенной, перемешивали и измеряли оптическую плотность полученного раствора на спектрофотометре СФ-56 при длине волны 258 ± 2 нм в кювете с толщиной слоя 10 мм. В качестве раствора сравнения использовали воду очищенную. Валидацию методики проводили по таким показателям, как линейность, повторяемость, воспроизводимость и правильность [1].
Результаты исследования и их обсуждение
Установлено, что при взаимодействии водного раствора ЦПХ с 10 % раствором калия йодида образуется фиолетовый осадок; с раствором йода образуется темно-зеленый хлопьевидный осадок. В реакции окисления с перманганатом калия в щелочной среде наблюдали окрашивание раствора в изумрудно-зелёный цвет, переходящий в светло-желтый. В кислой среде наблюдалось обесцвечивание раствора. При взаимодействии с бромной водой наблюдается выпадение белого осадка. Наличие хлорид – иона доказывали реакцией с раствором серебра нитрата. При сплавлении ЦПХ с фенолами образуются плавы с характерной окраской, изменяющейся при добавлении концентрированного раствора аммиака (табл. 1).
Таблица 1
Аналитические эффекты реакций сплавления ЦПХ с фенолами
|
Реагент |
Окраска плава |
Окраска плава при добавлении концентрированного раствора аммиака |
|
Фенол |
Светло-розовый |
Желтое окрашивание |
|
Тимол |
Светло-желтый |
Интенсивно желтое окрашивание |
|
Резорцин |
Желто-коричневый |
Синее окрашивание |
Для доказательства наличия третичного атома азота были проведены осадительные и микрокристаллоскопические реакции с общеалкалоидными и специальными реактивами (табл. 2).
Таблица 2
Аналитические эффекты реакций ЦПХ с общеалкалоидными и специальными реактивами
|
Реагент |
Аналитический эффект |
Аналитический эффект микрокристаллоскопической реакции |
|
Реактив Драгендорфа |
Желто-оранжевый хлопьевидный осадок |
Прозрачные кристаллы различной формы |
|
Пикриновая кислота |
Желто-зелёный осадок |
Прозрачные желто – зеленые сферические кристаллы |
|
Реактив Майера |
Бело-розовый осадок |
Красные игольчатые сросшиеся кристаллы |
|
Реактив Зонненштейна |
Белый осадок |
Бесцветные кристаллы |
|
Реактив Шейблера |
Белый осадок |
Цилиндрические серо-белые кристаллы, собранные в пучки |
|
Раствор танина |
Светло-коричневый раствор |
Серо-зеленые сферические кристаллы |
|
Реактив Марки |
Розовый осадок |
Прозрачные игольчатые сросшиеся кристаллы |
|
Реактив Эрдмана |
Бело-розовый осадок |
Белые объемные игольчатые кристаллы |
|
Реактив Фреде |
Белый осадок |
Белые игольчатые кристаллы |
|
Калия дихромат |
Желто-оранжевый осадок |
Зеленые объемные кристаллы |
При разработке оптимальной методики хроматографического определения нами было изучено влияние диэлектрической проницаемости на хроматографическую подвижность препарата [4]. Было установлено, что в бинарной системе изопропанол – раствор аммиака концентрированный (5:2) коэффициент подвижности (Rf) для ЦПХ равен 0,3 ± 0,05.
Анализ титриметрических методов количественного определения ЦПХ показал, что относительная погрешность определения во всех случаях не превышает 1,35 %, что свидетельствует о прецизионности методик в условиях повторяемости (табл. 3). Однако содержание ЦПХ в субстанции, найденное титриметрическими методами, является несколько завышенным, поэтому для количественного определения ЦПХ следует подобрать более оптимальные методы.
Таблица 3
Сравнительная оценка методов количественного определения ЦПХ
|
Метод определения |
Хср, % |
SD |
x ± ∆x |
RSD |
|
1. Аргентометрия по Мору |
99,82 |
0,53 |
99,82 ± 0,56 |
0,61 % |
|
2. Аргентометрия по Фольгарду в модификации Кольтгоффа |
100,2 |
0,85 |
100,2 ± 0,89 |
0,90 % |
|
3. Обратная йодиметрия |
100,81 |
1,3 |
100,81 ± 1,37 |
1,35 % |
При проведении спектрофотометрического анализа водных растворов ЦПХ установлено, что спектры поглощения характеризуются положением трех максимумов в области 210-220 нм, 258 ± 2 нм и 340 ± 2 нм (рис. 1).
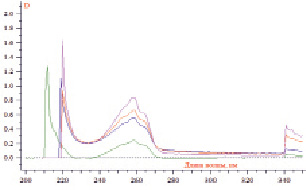
Рис. 1. Спектр поглощения водных растворов ЦПХ
Максимум при длине волны 258 ± 2 нм был выбран в качестве аналитической длины, так как он не изменяется при изменении концентрации растворов ЦПХ. Линейность предлагаемого метода определяли на 8 уровнях концентраций от теоретического содержания ЦПХ. Критерием приемлемости является коэффициент корреляции, величина которого должна быть не ниже 0,99 (рис. 2).
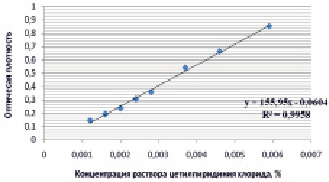
Рис. 2. Зависимость оптической плотности от концентрации водного раствора ЦПХ при длине волны 258 ± 2 нм
Для расчета коэффициента корреляции рассчитывали уравнение регрессии при длине волны 258 ± 2 нм, линейная зависимость наблюдается в интервале концентраций 1,2*10-3–5,9*10-3 %, коэффициент корреляции равен R = 0,9958, что соответствует валидационным критериям. По полученным данным был рассчитан удельный показатель поглощения (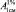 ) водных растворов ЦПХ, который равен 122,1.
) водных растворов ЦПХ, который равен 122,1.
Повторяемость методики определяли путем определения количественного содержания ЦПХ на 6 повторах (табл. 4). Критерий приемлемости выражается величиной относительного стандартного отклонения, которое не должно превышать 5 %. Установлено, что относительная погрешность определения составляет 0,32 %, что свидетельствует о прецизионности методики в условиях повторяемости [1, 2].
Таблица 4
Результаты количественного определения цетилпиридиния хлорида в водных растворах методом УФ-спектрофотометрии
|
Содержание ЦПХ, в % |
Xi – Xср |
(Xi – Xср)2 |
Метрологические характеристики |
|
98.65 |
0,46 |
0,2116 |
Xср = 98,19 |
|
98,15 |
0,4 |
0,1600 |
SD = 0,298 |
|
98,03 |
0,16 |
0,0256 |
x ± ∆x = 98,19 ± 0,324 |
|
98,04 |
0,15 |
0,2250 |
RSD = 0,32 % |
|
98,07 |
0,12 |
0,0144 |
|
|
98,2 |
0,1 |
0,0100 |
Правильность методики устанавливали путем определения количественного содержания цетилпиридиния хлорида в растворах, полученных путем добавления определенного количества стандарта к исследуемому раствору. Критерий приемлемости – средний процент восстановления при использовании растворов заданных концентраций, скорректированный на 100 %. Его средняя величина должна находиться в пределах 100 ± 5 %. Результаты измерений представлены в табл. 5.
Таблица 5
Определение правильности методики спектрофотометрического определения цетилпиридиния хлорида в водных растворах
|
Содержание ЦПХ, в мг |
Добавлено стандартного образца ЦПХ, в % |
Добавлено стандартного образца ЦПХ, в мг |
Расчетное содержание ЦПХ, мг |
Найденное содержание ЦПХ, мг |
Открываемость методики, R % |
|
0,57 |
50 % |
0,342 |
0,912 |
0,945 |
103,6 |
|
0,57 |
50 % |
0,342 |
0,912 |
0,930 |
101,9 |
|
0,57 |
50 % |
0,342 |
0,912 |
0,932 |
102,2 |
|
0,57 |
100 % |
0,57 |
1,14 |
1,16 |
101,8 |
|
0,57 |
100 % |
0,57 |
1,14 |
1,18 |
103,5 |
|
0,57 |
100 % |
0,57 |
1,14 |
1,16 |
101,8 |
|
0,57 |
160 % |
0,93 |
1,50 |
1,54 |
102,6 |
|
0,57 |
160 % |
0,93 |
1,50 |
1,53 |
102,0 |
|
0,57 |
160 % |
0,93 |
1,50 |
1,56 |
104,0 |
|
102,6 |
Процент открываемости методики УФ-спектрофотометрии составляет 102,6 %, что свидетельствует о правильности выбранной методики количественного определения. На основании проведенной валидационной оценки спектрофотометрического метода количественного определения ЦПХ установлено, что предлагаемая методика не отягощена систематической ошибкой, результаты анализа являются правильными, точными и имеют достоверно неразличающуюся воспроизводимость.
Выводы
1. Предложены химические методы идентификации и проведена оценка количественного содержания четвертичных аммониевых соединений в субстанциях на примере цетилпиридиния хлорида.
2. Для идентификации и оценки степени чистоты цетилпиридиния хлорида предложен метод хроматографии в тонком слое сорбента (ТСХ) в бинарной системе растворителей: изопропанол – раствор аммиака концентрированный (5:2), проявитель – реактив Драгендорфа, коэффициент подвижности ЦПХ равен 0,3 ± 0,05.
3. Проведена оценка количественного содержания ЦПХ титриметрическими методами, относительная погрешность определения не превышает 1,35 %, что свидетельствует о прецизионности данных методик в условиях повторяемости.
4. Разработана и проведена валидационная оценка методики количественного определения цетилпиридиния хлорида методом УФ-спектрофотометрии при длине волны 258 ± 2 нм, рассчитан удельный показатель поглощения водных растворов цетилпиридиния хлорида.
Библиографическая ссылка
Симонян Е.В., Ножкина Н.Н., Хачатрян М.А., Габитова Д.М. РАЗРАБОТКА МЕТОДОВ ИДЕНТИФИКАЦИИ И КОЛИЧЕСТВЕННАЯ ОЦЕНКА СОДЕРЖАНИЯ ЦЕТИЛПИРИДИНИЯ ХЛОРИДА // Международный журнал прикладных и фундаментальных исследований. 2016. № 5-3. С. 435-439;URL: https://applied-research.ru/en/article/view?id=9272 (дата обращения: 08.06.2026).

