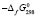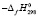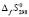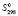Scientific journal
International Journal of Applied and fundamental research
ISSN 1996-3955
ИФ РИНЦ = 0,556
THERMODYNAMIC TRIANGULATION OF THE AG-GE-SE SYSTEM
Based on analysis of published data and from additional calculations the most reliable data have been selected for the entropy, enthalpy and free energy of formation silver selenide, germanium and silver selenogermanata: Δf H0298 (a-Ag2Se) = - 43.5, Δf H0298 (GeSe,cr) = - 82.9, Δf H0298 (GeSe2,cr) = - 103.7, Δf H0298 (a-Ag8GeSe6, cr) = - 290.8, Δf H0298 (a-Ag2Se) = - 50.3, Δf H0298 (GeSe,cr) = - 84.2, Δf H0298 (GeSe2,cr) = - 103.1, Δf H0298 (a-Ag8GeSe6, cr) = -312.4 kC·mol-1, Δf H0298 (a-Ag2Se) = 150.3, Δf H0298 (GeSe,cr) = 78.3, Δf H0298 (GeSe2,cr) = 112.6, Δf H0298 (a-Ag8GeSe6,cr) = 699.1 C·mol-1.К-1. It has been that the compound Ag2GeSe3 formed in the amorphous state is unstable and decomposes down into compounds Ag8GeSe6 and GeSe2. The triangulation Ag-Ge-Se system, based on the formation of a congruently melting ternary compound Ag8GeSe6, has been carried out and direct and inverse matrix to convert this system to the quasiternary subsystems Ag-Ag2Se-Ag8GeSe6, Ag2Se-Ag8GeSe6-Se, Ag8GeSe6-GeSe2-Se, Ag8GeSe6-GeSe2-GeSe, Ag8GeSe6-GeSe-Ge, Ag8GeSe6-Ag-Ge have been determined.
Халькогерманаты серебра являются перспективными функциональными материалами, обладающими интересными полупроводниковыми, фото- и термоэлектрическими и др. свойствами [5]. Оптимизация технологических режимов синтеза и выращивания монокристаллов новых многокомпонентных фаз и материалов на их основе требует наличия взаимосогласованную информацию для термодинамических и фазовых характеристик халькогенидных тройных систем, в частности для системы Ag-Ge-Se. В работе [1,9] в системе Ag-Ge-Se выявлены две тройные соединения Ag8GeSe6 и Ag2GeSe3. Если Ag8GeSe6 является конгруэнтно плавящимся соединением, то второе тройное соединение отсутствует в фазовых диаграммах, построенных на основании результатов РФА и ДТА в [6]. Возможно, соединение Ag2GeSe3 неустойчиво и распадается на фазы Ag8GeSe6 и GeSe2.
Целью нашей работы является оценка термодинамической устойчивости тройных соединений Ag8GeSe6 и Ag2GeSe3 относительно двойных соединений Ag2Se, GeSe и GeSe2 и триангуляция тройной систем Ag-Ge-Se.
Термодинамические расчеты и обсуждение
Термодинамические функции образования соединений Ag2Se, GeSe и GeSe2
Термодинамические функции образования соединений Ag2Se, GeSe и GeSe2 использовали для расчета термодинамических функция образования тройных соединений из двойных соединений. При этом проанализировали исходные источники, из которых заимствованы справочные данные. Термодинамические данные для соединений Ag2Se и GeSe, приведенных в различных источниках, находятся в соответствии [2, 3]. В то же время значения энтальпии образования соединения GeSe2, полученные разными авторами [7, 8] существенно отличаются. В работе [7] методом фторной калориметрии для стандартной энтальпии образования кристаллического и стеклообразного GeSe2 при 298.15 К получены следующие величины, соответственно: 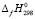 (GeSe2,кр) = - (103.7 ± ± 3.1) кДж·мол·1 и
(GeSe2,кр) = - (103.7 ± ± 3.1) кДж·мол·1 и 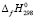 (GeSe2, cт) = - (91.6 ± 3.2) кДж·мол·1 . Стандартная энтальпия фазового перехода: GeSe2 (ст.) = GeSe2 (кр), составляет (-12.1 ± ± 4.2) кДж.моль-1. В работе [8] методом прямой калориметрии для стандартной энтальпии образования кристаллического и стеклообразного (аморфного) GeSe2 получены следующие величины
(GeSe2, cт) = - (91.6 ± 3.2) кДж·мол·1 . Стандартная энтальпия фазового перехода: GeSe2 (ст.) = GeSe2 (кр), составляет (-12.1 ± ± 4.2) кДж.моль-1. В работе [8] методом прямой калориметрии для стандартной энтальпии образования кристаллического и стеклообразного (аморфного) GeSe2 получены следующие величины 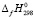 (GeSe2,кр) = -(84.4 ± 2)кДж·мол·1 и
(GeSe2,кр) = -(84.4 ± 2)кДж·мол·1 и 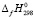 (GeSe2,cт) = -(76.5 ± 1) кДж·мол·1. Стандартная энтальпия фазового перехода: GeSe2 (ст.) = GeSe2 (кр), составляет (-7.9 ± ± 2.1) кДж.моль-1. Значение
(GeSe2,cт) = -(76.5 ± 1) кДж·мол·1. Стандартная энтальпия фазового перехода: GeSe2 (ст.) = GeSe2 (кр), составляет (-7.9 ± ± 2.1) кДж.моль-1. Значение 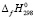 (GeSe2,кр) = - (62.8 ± 3.1) кДж.моль-1, представляется нам весьма заниженным. Значения стандартной энтропии Ag2Se, GeSe и GeSe2, приведенные в различных работах [2, 3, 8], не вызывали сомнения. Значения
(GeSe2,кр) = - (62.8 ± 3.1) кДж.моль-1, представляется нам весьма заниженным. Значения стандартной энтропии Ag2Se, GeSe и GeSe2, приведенные в различных работах [2, 3, 8], не вызывали сомнения. Значения 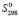 , а также энтропии образования
, а также энтропии образования 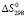 этих соединений приведены в табл. 1. Стандартные свободные энергии образования соединений, приведенные в табл. 1 вычислены по уравнению Гиббса-Гельмгольца:
этих соединений приведены в табл. 1. Стандартные свободные энергии образования соединений, приведенные в табл. 1 вычислены по уравнению Гиббса-Гельмгольца:
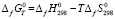 (1)
(1)
Для анализа зависимости свободной энергии образования соединений от состава на рис. 1 вначале вычислим свободную энергию реакции
GeSe(kr) + Se (kr) → GeSe2(kr) + 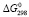 (2)
(2)
По данным [7]: 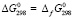 (GeSe2, кр)-
(GeSe2, кр)-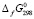 (GeSe,кр) = -103.7-(-84.2) = = -19.5 кДж.моль-1 (рис. 1, кр. 1). По данным [8]:
(GeSe,кр) = -103.7-(-84.2) = = -19.5 кДж.моль-1 (рис. 1, кр. 1). По данным [8]: 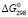 = -83.6-(-84.2 = 0.6 кДж. моль-1 (рис. 1, кр. 2). По данным [7]:
= -83.6-(-84.2 = 0.6 кДж. моль-1 (рис. 1, кр. 2). По данным [7]: 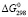 = -62.8-(-84.2 = 21.4 кДж.моль-1 (рис. 1, кр. 3). Последние две значения для свободной энергии реакции (2) не соответствуют действительности (рис. 1, кр. 2,3). Отметим, что GeSe является перитектическим соединением, а соединение GeSe2 является конгруэнтно плавящимся соединением с температурой плавления 742 °С.
= -62.8-(-84.2 = 21.4 кДж.моль-1 (рис. 1, кр. 3). Последние две значения для свободной энергии реакции (2) не соответствуют действительности (рис. 1, кр. 2,3). Отметим, что GeSe является перитектическим соединением, а соединение GeSe2 является конгруэнтно плавящимся соединением с температурой плавления 742 °С.
Термодинамические функции образования соединений Ag8GeSe6 и Ag2GeSe3
В работе [4] термодинамические функции образования кристаллических Ag8GeSe6 и Ag2GeSe3 определены измерением ЭДС концентрационных цепей типа (-) Ag (тв) | Ag4RbI5 (тв) | (Ag-Ge-Se) (тв) (+) в интервале температур 300-430К. В работе [9] термодинамические функции образования стеклообразных фаз на основе этих соединений определены измерением ЭДС концентрационных цепей типа (-) Ag (тв) | AgI (тв) | (Ag-Ge-Se) (стекло) (+) в интервале температур 480-580К.
Термодинамические функции образования соединений Ag8GeSe6 и Ag2GeSe3 также определили в этой работе расчетным путем, на основании данных двойных соединений Ag2Se и GeSe2 в табл. 1 по уравнению:
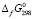 (Ag2GeSe3,кр) =
(Ag2GeSe3,кр) = 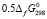 (Ag2Se ,кр) +
(Ag2Se ,кр) + 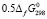 (GeSe2,кр) = –153.3кДж.моль-1 (3)
(GeSe2,кр) = –153.3кДж.моль-1 (3)
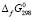 (Ag8GeSe6,кр) =
(Ag8GeSe6,кр) = 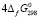 (Ag2Se ,кр) +
(Ag2Se ,кр) + 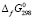 (GeSe2,кр) = –303.1кДж.моль-1 (4)
(GeSe2,кр) = –303.1кДж.моль-1 (4)
Поскольку химические реакции протекают убыванием свободной энергии Гиббса, то свободные энергии образования стабильных соединений должны быть больше (по абсолютной величине) от аддитивно вычисленных величин в (3,4).
Из рис. 2 следует, что приведенные в работе значения 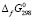 (Ag2GeSe3) меньше аддитивных величин в (3,4), что свидетельствует о термодинамической неустойчивости соединения Ag2GeSe3. В этой работе синтезировали и исследовали сплав этого состава. На основании РФА было выявлено, что соединение Ag2GeSe3 получается в стеклообразном состоянии при быстром охлаждении расплава. После отжига сплава РФА показал отсутствие линий для соединения Ag2GeSe3. Поэтому при триангуляции системы Ag-Ge-Se предполагали, что в этой системе в кристаллическом состоянии образуется только одно тройное соединение Ag8GeSe6 (рис. 3). Стандартную энтропию Ag8GeSe6 также определили расчетным путем по уравнению [10]:
(Ag2GeSe3) меньше аддитивных величин в (3,4), что свидетельствует о термодинамической неустойчивости соединения Ag2GeSe3. В этой работе синтезировали и исследовали сплав этого состава. На основании РФА было выявлено, что соединение Ag2GeSe3 получается в стеклообразном состоянии при быстром охлаждении расплава. После отжига сплава РФА показал отсутствие линий для соединения Ag2GeSe3. Поэтому при триангуляции системы Ag-Ge-Se предполагали, что в этой системе в кристаллическом состоянии образуется только одно тройное соединение Ag8GeSe6 (рис. 3). Стандартную энтропию Ag8GeSe6 также определили расчетным путем по уравнению [10]:
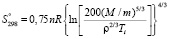 (5)
(5)
Здесь n – число атомов в молекуле Ag8GeSe6, R = 8.31 Дж.моль-1.К-1, M = 1410 – мольярная масса, Ti = 1158 К температура плавления, r = 7.1 плотность в г.см-3. Значение стандартной энтропии Ag8GeSe6, вычисленное по уравнению (5), практически совпадает (таблица) с результатом измерения ЭДС [4].
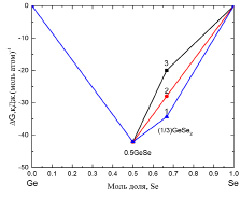
Рис. 1. Зависимости свободной энергии образования селенида и дисульфида германия в кристаллическом состоянии от состава: 1-по [7], 2-[8],3-[3]
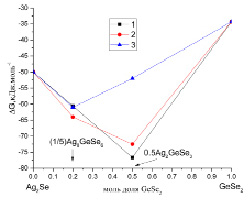
Рис. 2. Зависимости свободной энергии образования тройных соединений в кристаллическом состоянии от состава: 1-аддивный расчет по урав.(3,4), 2-[4], 3-[9]
Термодинамические функции соединений в кристаллическом состоянии
|
Вещество |
|
|
|
|
|
кДж.моль-1 |
Дж.моль-1.К-1 |
|||
|
α-Ag2Se |
50.3 ± 2[3] |
43.5 ± 0.5[3] |
22.7 ± 1 |
150.3 ± 1.5[3] |
|
GeSe |
84.2 ± 5[3] |
82.9 ± 5[3] |
5.18 ± 0.5 |
78.3 ± 1[3] |
|
GeSe2 |
103.1 ± 2.0[7] |
103.7 ± 3.1 [7] |
2.52 ± 0.1 |
112.6 ± 2[7] |
|
α-Ag8GeSe6 |
312.4 ± 5[4] |
290.8 ± 5[4] |
75.2 ± 6 |
699.1 ± 10[4] |
|
288.6 ± 5[9] |
261.8 ± 5[9] |
90.4 ± 5 |
714.4 ± 10[9] |
|
|
303.4 ± 5 аддитивный расчет по уравн.(4) |
278.4 ± 5 аддитивный расчет |
70.4 ± 5 |
696.2 ± 10 Расчет по уравн.(5) |
|
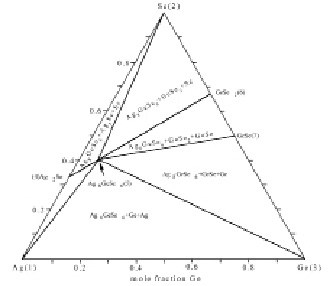
Рис. 3. Фазовые области системы Ag-Se-Ge в температурном интервале 300-500 К
Триангуляция системы Ag-Ge-Se
Для практического использования фазовых диаграмм тройных систем со сложным взаимодействием компонентов целесообразно их разделить на симплексы – квазибинарные, квазитройные и взаимные системы. Разделение системы Ag-Ge-Se на квазитройные системы с учетом образования одного тройного соединения Ag8GeSe6 представлено на рис. 3.
При переходе от одного стандартного состояния к другому пересчитываются концентрации компонентов. Для упрощения этой задачи и выполнения расчетов на компьютере целесообразно использовать матрицы, связывающие концентрации компонентов тройной системы Ag-Ge-Se с компонентами ее подсистем. Связь между концентрацией (моль доля) компонентов (zi) тройной системы и ее подсистем (xi) выражается формулами:
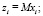
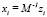 (6)
(6)
Здесь М и М-1 – квадратная матрица третьего порядка и обратная матрица, указывающие концентрации компонентов в узлах тройной системы и подсистем, соответственно.
Для подсистемы 1–4–5 (рис. 3):
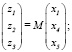
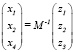 (7)
(7)
где z1, z2, z3 моль. доли Ag, Se, Ge в тройной системе Ag-Se-Ge; x1, x4, x5 – моль доли Ag, Ag0.667Se0.333 (Ag2Se) и Ag0.533Ge0.067Se0.4 (Ag8GeSe6) в квазитройной системе 1–4–5.
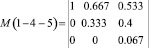 ;
;
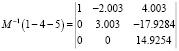 (8)
(8)
Следовательно,
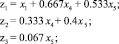
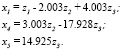
Для остальных квзитройных систем 4-2-5, 5-2-6, 5-6-7, 5-7-3 и 1-5-3 (рис. 3) представляем только прямые М матрицы, на основании которых с помощью компьютера можно определить обратные матрицы.
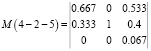 ,
,
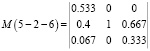 ,
,
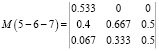 ,
,
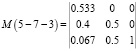 ,
,
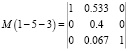 .
.
Заключение
Тройная система Ag-Ge-Se с образованием одного конгруэнтно плавящегося тройного соединения Ag8GeSe6 с помощью матриц третьего порядка разделена на 6 квазитройных подсистем Ag-Ag2Se-Ag8GeSe6, Ag2Se-Ag8GeSe6-Se, Ag8GeSe6-GeSe2-Se, Ag8GeSe6-GeSe2-GeSe, Ag8GeSe6-GeSe-Ge, Ag8GeSe6-Ag-Ge.
Библиографическая ссылка
Мамедов А.Н., Ибрагимова Ф.С. ТЕРМОДИНАМИЧЕСКАЯ ТРИАНГУЛЯЦИЯ СИСТЕМЫ AG-GE-SE // Международный журнал прикладных и фундаментальных исследований. 2016. № 7-4. С. 553-557;URL: https://applied-research.ru/en/article/view?id=9873 (дата обращения: 13.05.2026).