Современный мир вступил в стадию системного кризиса [1, 2]. На протяжении 10 тыс. лет всей истории цивилизации раз в несколько сот лет происходит совпадение трех уровней кризисов: кризиса глобальной цивилизации, кризисов мировых и локальных цивилизаций. Происходит переход к постиндустриальной цивилизации и формированию пятого поколения локальных цивилизаций. В ведущих странах мира пятый технологический уклад уходит в историю. Развитый мир переходит в шестой технологический уклад. Россия в плане технологическом находится, в основном, в первых поколениях пятого уклада. Мир движется в сторону инновационных наукоемких продуктов. Доля России на высокотехнологическом рынке мира сегодня составляет всего лишь 0,3%. Для того чтобы Россия вошла в технологический мир ХХI в. нужна стратегия инновационного развития. Руководством России политически определена стратегия инновационного развития [3]. В центре планируемых изменений человек, качество жизни человека. Но человек не исключительно потребляющий, а человек духовный — формирование нового человека, определяющий элемент формирующей стратегии.
Развитие фармацевтической отрасли предусматривает развитие конкурентных преимуществ национальной фармацевтической отрасли и осуществление ее перехода на инновационную модель развития — основная задача состоит в создании инфраструктуры для разработки инновационных препаратов с применением последних достижений науки и техники с использованием современных технологических платформ, основанных на экологически чистых технологиях.
За последнее время в медицине значительно расширилось применение фитопрепаратов и фитосырья в фармации. Лекарственное растительное сырье (ЛРС), составляющее основу фитопрепаратов и кормов по своему происхождению наиболее контаминировано микрофлорой и является наиболее вероятным переносчиком спор микроорганизмов. Микроорганизмы — первичная и основная причина биологических рисков, связанных с продовольствием и лекарственными средствами — присутствуют в окружающей среде. Как представлено на рис. 1 взаимодействие растений и микроорганизмов начинается с семян растений, которые контаминированы микроорганизмами. Воздействие микробов может быть полезным, безвредным или вредным для здоровья человека. Большинство видов микроорганизмов не представляет опасности для людей, но есть и такие, которые могут оказаться опасными и даже смертельными. Поэтому возникла необходимость в иных системообразующих подходах к обеспечению микробиологической безопасности. Таким подходом является анализ микробиологического риска (АМР). Понятие микробиологического риска есть функция вероятности наступления отрицательного эффекта для здоровья и величины этого эффекта как следствия вредного фактора (микроба, микробного токсина), присутствующего в продуктах [4]. Можно ли эту угрозу здоровью, вызванную загрязнением среды обитания, оценить количественно? Можно, если проводить анализ микробиологического риска при всех техногенных явлениях.
Рис. 1. Схема попадания микроорганизмов в растущее растение. 1 — Подсемядольное колено (гипокотиль); 2 — корешок; 3 — оболочка семени (кожура); 4 — семядоли; 5 — листовые примордии; 6 — почки с меристемами; 7 — узел; 8 — сосудистые ткани; 9 — латеральные корни; 10 — главный корень; 11 — корневые волоски; 12 — корневой чехлик.

Микробная контаминация растений зависит от окружающей среды (почва, воздух, вода). На растениях и внутри них может быть найдено широкое разнообразие бактериальных микроорганизмов, грибов и вирусов, а также следы от грызунов и насекомых. Предварительные исследования показали, что среди перечисленной микрофлоры могут находиться патогенные и условно-патогенные микроорганизмы, а также токсины и токсичные соединения. ЛРС, составляющее основу фитопрепаратов и пищевых продуктов по своему происхождению наиболее контаминировано микрофлорой и является наиболее вероятным переносчиком спор микроорганизмов. Поэтому очень высока потребность оценки рисков микробного загрязнения растений. Однако несмотря на использование систем НАССР и GMP сегодня они не являются столь эффективными, какими были в недалеком прошлом, и не позволяют справляться с заболеваниями, вызванными новыми и старыми, исчезнувшими, но вновь возникшими (так называемыми эмерджентными) патогенами. Число эмерджентных инфекций растет повсеместно, несмотря на строгое соблюдение гигиенических требований. Примерами за последние 20 лет являются сальмонеллезы. Число эмерджентных инфекций растет повсеместно, несмотря на строгое соблюдение гигиенических требований (примерами за последние 20 лет являются сальмонеллезы).
.Сравнительный анализ этих систем свидетельствует, что они дополняют друг друга и должны быть гармонизированы, что позволит создать единую комплексную систему анализа микробиологического риска в этих отраслях. Кроме того многие продукты питания и фитопрепараты непосредственно связаны с выращиванием растений.
Растительно-микробные взаимодействия являются основой поддержания жизни на планете [4], которые начали складываться задолго до появления человека. Следует отметить, что и пресноводные, и морские макро- и микроскопические растения колонизируются микроорганизмами, и их взаимодействия, определяются региональными условиями — почвой, воздушной средой и водной средой. Если рассматривать круговорот в природе, то растения поставляют кислород и продукты питания для человека, животных и существенной части микромира, а микроорганизмы осуществляют возврат питательных элементов для растений, разлагая и потребляя в качестве субстратов как отмершие растения, так и зачастую живые, и защиту растений от патогенных и условно-патогенных микроорганизмов. Взаимодействие микроорганизмов и растений приводит к возникновению микробно-растительных комплексов (симбиоз) в различных экологических регионах. Состав микробиоценоза не является одинаковым, а зависит от условий окружающей среды в данном регионе.
В 1978 г. сформулировали общую теорию существования биопленок, согласно которой большинство бактерий растут в замкнутых матрицах — биопленках, прикрепленных к поверхностям любых экосистем, они обеспечены питанием и содержат воду. Существенно, что они пространственно связаны с поверхностью бактериальных клеток и значительно отличаются от своих планктонных двойников. Сегодня большинством микробиологов признано, что значительное количество микроорганизмов в естественных и искусственно созданных средах существует в виде структурированных, прикрепленных к поверхности сообществ — биопленок.
Растения, как показано на рис. 1, имеют субстратную (корни) и надземную часть, что необходимо учитывать при анализе их микробной обсемененности. Субстратная (почвенная) часть находится в почве и непрерывно контактирует с почвенными микроорганизмами (грибы, актиномицеты, бактерии), вирусами и фагами, которые могут проникать в корни или колонизировать поверхность корней. При колонизации корней и волосков корней микроорганизмы образуют биопленки, где демонстрируют изменение фенотипа, выражающееся изменением параметров роста и экспрессии специфичных генов. Способность бактерий формировать биопленки — существенный фактор патогенности. Кроме того, аналогичные пленки микроорганизмов обнаруживаются в организме животных и человека. Сообщество организует единую генетическую систему в виде плазмид — кольцевых ДНК, несущих поведенческий код для членов биопленки, определяющих их пищевые (трофические), энергетические и другие связи между собой и внешним миром. На всех этих этапах вырабатывается резистентность микроорганизмов к антибиотикам, дезинфицирующим веществам и синтезированным соединениям.
Надземная часть растений постоянно контактирует с микроорганизмами воздуха и они могут оседать с пылью и водными каплями. Состав воздушной микрофлоры может периодически изменяться при изменении ветра, а так же зависит от наличия промышленных предприятий. При производстве лекарственных средств из растительного сырья важную роль играет не только контроль исходных материалов, условий хранения и переработки, но и его происхождение (предыстория).
В качестве точки отсчета взаимодействия микроорганизмов и растений логично избрать прорастание семени в почве (см. рис. 1 и 2). Исследования микробной обсемененности семян показали, что семена растений, попадающие в почву, уже контаминированы микроорганизмами, т. е. микробно-растительные отношения начинаются гораздо раньше. Для семян характерно наличие в них микроорганизмов (фитопатогенов), которые уже находятся внутри созревшего семени.
Рис. 2 Развитие растения из семени в почве и контакт микроорганизмов почвы с формирующейся корневой системой
Потенциально семя растения может нести на себе бактериальные клетки, их эндоспоры или цисты, конидиоспоры и/или обрывки гиф актиномицетов, обрывки мицелия грибов и/или их конидиоспоры, цисты простейших, а также, возможно, яйца нематод и вирусы. Численность разных групп микроорганизмов варьирует и зависит от многих факторов: географических и климатических факторов и в существенной степени определяются биологией самих микроорганизмов. Фактически невозможно предсказать, сколько на поверхности здорового семени может быть бактерий и грибов.
На поверхности и в покровах, а в некоторых случаях и в тканях разных семян можно обнаружить бактерии, принадлежащие к родам Agrobacterium, Arthrobacter, Bacillus, Burkholderia, Clavibacter, (Clostridium, Curtobacterium, Erwinia, Pseudomonas, Rhizobacter, Rhizomonas,Streptomyces, Xanthomonas и др., грибы родов: Acremonium, Alternaria, Aureobasidium, Aspergillus, Botrytis, Cephalosporidium, Cfaviceps, Drechslera, Fusarium, Gibberella, Helminthosporium, Humicola, Penicillium, Perenospora, Phoma, Phytophthora, Plasmopara, Puccinia, Pythium, Rhizoctonia, Septoria, Trichothecium, Ustilago, Verticillium и др. Среди перечисленных родов бактерий и грибов много истинных фитопатогенов и многие из них обнаруживаются в лекарственных растениях и фитопрепаратах. В семенах растений, даже находящихся в состоянии глубокого покоя, протекают процессы метаболизма, и, следовательно, происходят обменные процессы с окружающей средой. Многие семена растений обладают специфическим, характерным для соответствующего вида запахом за счет синтеза летучих органических веществ. Эти вещества являются потенциальными субстратами для микроорганизмов.
При попадании в благоприятные условия влажности и температуры семя растения набухает и прорастает (см. рис. 2). При набухании, а тем более прорастании в семени происходят молекулярно-генетические и физиолого-биохимические процессы. Основное действие на микробное сообщество поверхности семян оказывает «выброс» органических веществ из набухающего и прорастающего семени. Концентрация и состав таких веществ каждого вида специфичны. При прорастании семян пшеницы обнаруживаются углеводы (главным образом, глюкоза и фруктоза, а в целом — до 10 компонентов), органические кислоты (в большинстве своем — сукцинат, фумарат и малат) и до 16 аминокислот, среди которых доминируют аспарагиновая и глутаминовая, и «выброс» летучих органических веществ (ЛОВ). Будущее растение (рис. 1) контактирует с этими объектами, как формирующейся корневой системой, так и будущей надпочвенной частью — стеблем, пока проростком. Корень контактирует с неспецифическими для него микроорганизмами, т. е. такими, контакт с которыми не приводит к его инфицированию, и со специфическими, инфицирующими корень микроорганизмами. Среди инфицирующих имеются непатогенные и типичные патогены. К непатогенным относятся, например, клубеньковые бактерии, а из грибов — микоризные (эндо- и эктомикоризные ). Феномен более высокой плотности микроорганизмов вокруг корня за счет потребления экссудатов и ризодепозитов называется ризосферным эффектом. В сравнительных экспериментах с выращиванием стерильных растений в стерильной и нестерильной почве показано, что в ризосфере микробно-растительные взаимодействия выражаются, в частности, и в стимуляции выделения экссудатов растений. Численность микроорганизмов в ризосфере может превышать их численность в окружающей почве от нескольких процентов до десятков процентов и даже на порядок. Количество микроорганизмов в ризосфере может колебаться от миллионов до сотен миллиардов клеток на грамм сухой почвы.
Микробное сообщество развивается вдоль растущего корня волнообразно, т. е. зоны с более высокой плотностью микроорганизмов чередуются с зонами низкой плотности. Особенно много микроорганизмов содержится в нижней прикорневой части растений, что связано с попаданием микроорганизмов из почвы. В большом количестве обнаруживаются микроорганизмы на растениях, растущих на полях орошения, свалках, вблизи складирования навоза, в местах выпаса скота. При этом растения могут загрязняться патогенными микроорганизмами и могут быть хорошей питательной средой для размножения микроорганизмов. Одним из способов, препятствующих их росту на растениях, является процесс высушивания растений. Микроорганизмы в жизни растений выполняют функцию средообразования и общего питания. Они осуществляют разложение и минерализацию растительных остатков и органического вещества в целом, высвобождая и возвращая в почву минеральные элементы, необходимые для роста растений, а в атмосферу — СO2 и некоторые другие газы. Микроорганизмы продуцируют стимуляторы роста и токсические для растений вещества. Микроорганизмы фактически создают почву. Бактерии играют ключевую роль в обеспечении экосистем азотом.
Фитопатогенов среди грибов гораздо больше, чем среди бактерий. К фитопатогенным микроорганизмам относят бактерии, вирусы и грибы. Болезни, вызываемые бактериями, называют бактериозами. Среди возбудителей бактериозов встречаются псевдомонады, микобактерии, эрвинии, коринебактерии, агробактерии и др. Передача возбудителей бактериозов происходит через зараженные семена, остатки больных растений, почву, воду, воздух, путем переноса насекомыми, моллюсками, нематодами. В условиях повышенной влажности, низкой температуры на вегетирующих или скошенных растениях могут развиваться грибы родов Fusarium, Penicillium, Aspergillus и др., вызывающие у людей микотоксикозы.
Фитопатогенные микроорганизмы вызывают инфекционные болезни. Заражение растений происходит через инфицированные семена, почву, грунтовые и дождевые воды, насекомых. Основным источником является почва, так как в ней содержатся остатки неперегнивших растений. Фитопатогенные микробы могут проникать в растения через естественные образования и повреждения. Некоторые микроорганизмы вырабатывают ферменты, лизирующие кутикулу растений и облегчающие внедрение возбудителя. Попав в растение и достигнув критической концентрации, микроорганизмы вызывают заболевания. Различают общие поражения всего растения вследствие распространения возбудителя в сосудистой системе и местные или очаговые — поражения на листьях, стволах, ветвях, корнях и корневищах, возникающие при интрацеллюлярном распространении. По совокупности анатомических и физиологических изменений определяют тип болезни растений: камеде-, смоло-, слизетечения. Чаще вызывают бактерии рода Erwinia и актиномицеты (Ascomycetes), наблюдают у лиственных и хвойных деревьев. Большое разнообразие заболеваний растений вызывают различные микроорганизмы: бактерии родов Pectobacterium, Erwinia, Pseudomonas, Agrobacterium и грибов Ascomycetes, Corynebacterium и несовершенные грибы.
Принципиально важным является отклонение от нормы обменных процессов вплоть до качественных изменений клеточных структур у больных растений, что приводит к изменению химического состава тканей и снижению содержания активных веществ. Использование их в качестве сырья в аптечных условиях становится невозможным. Растительный организм обладает защитными механизмами, противодействующими внедрению и размножению фитопатогенных бактерий. К ним можно отнести особенности покровных тканей, высокую кислотность клеточного сока, образование биологически активных веществ — фитонцидов, подавляющих развитие микроорганизмов. Кроме того, лекарственное сырье загрязняется микробами во время сборки, сушки, измельчения, упаковки, хранения. Визуально видно, что признаками порчи лекарственного сырья является изменение цвета и гниение.
Предварительные исследования показали, что микрофлора может включать патогенные и условно-патогенные микроорганизмы, а также токсичные соединения. В связи с чем, необходимо проводить оценку микробиологических рисков пищевых продуктов и лекарственных средств растительного происхождения (табл. 1).
Таблица №1
Видовой состав микофлоры, выделенной из НЛС и сырья
|
Категория ЛС |
Виды грибов-контаминантов ЛС |
|
1. Препараты из сырья природного происхождения |
A. flavus, A. candidus, A. lanosum, A. flavipes, A. ventii, P. capsulatum, P. fellutanum, P. tardum, P. steckii, P. raciborskii, P. gorlenkoanum, P. purpurogenum, P. chermesium, P. herqei, P. wakzmanii, P. verruсosum, Rhodotorula sp., Pichia sp., Cryptococcus laurentii, Aureobasidium pullulans, Alternaria consortiall, Mucor sp., M. strictus, M. racemosus, Rhizopus sp., Botrytis cinerea |
|
2. Лекарственное растительное сырье |
A. orysae, A. niger, A. fumigatus, A. candidus, A. chevalieri, A. ustus, A. flavus, P. roseo-purpureum, P. verrucosum, P. meleagrinum, P. asperosporum, P. raciborskii, P. frequentans, P. steckii, P. decumbens, P. diversum, Trichoderma sp., T. hamatum, Mucor sp., M. racemosus, Al. consortial, Rhizopus sp., Cladosporium transchelii |
|
3. Вспомогательные материалы |
A. flavus, A. ochraceus, P. ochrochoron, P. verrucosum, P. frequentans, P. citrinum, P. asperosporum, P. raciborskii, Al. alternata, Al. solani, Mucor sp., M. racemosus, M. abundans, M. hiemalis, Rhizopus sp., Rh. nigricans, T. harzianum, Fusarium sp., Rhodotorula sp., Geotrichum sp., Acremonium charticola, Cladosporium cladosporioides. |
Универсальная стратегия, которой следует большинство РМС (растительно-микробный симбиоз), включает сигнальное взаимодействие растений с микробами, их обмен метаболитами, а также развитие специализированных для симбиоза клеточных и тканевых структур. Обмен сигналами является процессом, играющим ключевую роль во всех симбиозах и определяющим перекрестную регуляцию и координированную экспрессию генов партнеров.
Функционально и генетически интегрированные симбиозы возникли и эволюционировали, в первую очередь, как системы для восприятия, преобразования, хранения, а в ряде случаев, — для наследования сигнальной информации, получаемой от партнеров.
Высокая зависимость растений от этих взаимодействий отражается насыщенностью их геномов последовательностями ДНК, кодирующими предполагаемые рецепторы для сигналов, получаемых от микросимбионтов.
Процесс инфицирования начинается с адгезии клеток бактерий на поверхности корневых волосков. Корневые волоски бобовых продуцируют особые вещества — хемоаттрактаты для бактерий. К таким соединениям относятся флавоноиды и изофлавоноиды. В процессе узнавания принимают участие лектины, способствующие прикреплению бактерий к корневым волоскам. Флавоноиды и изофлавоноиды индуцируют экспрессию бактериальных nod-генов, которые отвечают за синтез веществ, называемых Nod-факторами, обеспечивающих межвидовое взаимодействие. В настоящее время известно более 24 веществ, продуктов экспрессии nod-генов, большинство из них ферменты. Компонент корневых экссудатов, аминокислоту триптофан, ризобии способны трансформировать в индолилуксусную кислоту (ИУК). ИУК по своей природе является ростовым гормоном, стимулирующим рост растительных клеток. Грибы, как и бактерии, вступают с растениями в симбиотические (мутуалистические) отношения. Партнерами такого симбиоза являются в первую очередь высшие грибы, а со стороны растений — небобовые растения, в том числе многолетние древесные растения. Речь идет о микоризообразовании. Микориза — наиболее широко распространенный тип РМС, который растения формируют с грибами, колонизирующими корни и другие подземные органы, и при этом часть микобионта (грибного партнера) находится внутри растения, а другая часть — в почве. Универсальной формой эндомикоризы (ЭМ) является арбускулярная микориза (AM), формируемая подавляющим большинством (8090% видов) наземных растений. Разделение микобионта на внутри- и внекорневую части отражает его ключевую функцию посредника между растением и почвой. В природных фитоценозах, где происходит жесткая конкуренция за почвенное питание, самостоятельное выживание растений сильно затруднено, что позволяет рассматривать зависимость большинства растений от микоризных грибов как экологически облигатную. Гриб «защищает» инфицированное растение от реальных фитопатогенов, в частности от грибов Fuzarium, способствует выработке у него устойчивости к токсинам и синтетическим соединениям. Такое явление называют «индуцированной устойчивостью» (ISR). В ходе образования ЭМ партнеры синтезируют ряд новых белков, которые служат индикаторами дифференциальной экспрессии генов, определяемой обменом партнеров молекулярными сигналами. Наиболее изучены гидрофобины — небольшие цистеин-богатые белки, которые накапливаются в гифах, контактирующих с растительными клетками, а также в плодовых телах гриба. Другая группа грибных белков, специфически синтезируемых при симбиозе, получила название SRAP (symbiosis-regulated acid proteins). Гены, кодирующие структуры гидрофобинов и SRAP, транскрипционно активируются при формировании ЭМ. Генетические основы эволюции растительно-микробного симбиоза представляют разнообразные функции: матричные процессы, обмен веществ и энергии, образование мембранных и поверхностных структур, клеточный цикл. В дополнение к хромосоме, в геноме «колийного типа» могут присутствовать более мелкие репликоны (плазмиды, эписомы, профаги), выполняющие частные адаптивные функции, включая синтез антибиотиков, использование редких источников питания, устойчивость к тяжелым металлам или ксенобиотикам. Изучение бактериальных симбионтов растений показало, что многие из них обладают гораздо более сложными, многокомпонентными (состоящими из нескольких сопоставимых по размеру репликонов) геномами, имеют в среднем намного более крупные геномы (6,73±1,26 млн пар нуклеотидов), чем свободноживущие бактерии (4,34±0,99 млн пар нуклеотидов). У быстрорастущих видов (Зуда) Rhizobium геномы содержат в дополнение к хромосоме многочисленные плазмиды, которые могут достигать необычайно крупных размеров. Впервые многокомпонентные геномы были выявлены у ризобий люцерны (S. meliloti): было показано, что практически все штаммы содержат в дополнение к хромосоме (около 3600 т.п.н.) две гигантские плазмиды (11001900 т.п.н.), а иногда еще и 16 «средних» плазмид размером 10400 т.п.к. Не менее сложные геномы выявлены у агробактерий — патогенов, образующих опухоли на растениях. Эти бактерии таксономически близки к быстрорастущим ризобиям. Было показано, что Зуда-плазмиды являются детерминантами основных симбиотических признаков ризобий: вирулентности, азотфиксирующей активности и хозяйской специфичности
Для некоторых Sym-плазмид показано участие в контроле адаптивно значимых признаков, важных для выживания в почве, например для катаболизма сложных и редких питательных субстратов, синтеза поверхностных компонентов клетки и бактериоцинов, а также кислотоустойчивость и скорости роста, существование микроорганизмов в сложных экосистемах «хозяин-среда». Адаптивная роль высокой геномной пластичности симбиотических микробов заключается в регулярных генных перестройках, являющихся источником «исходного материала» для коэволюции с хозяевами. В модельных опытах, проведенных на Е. coli, было показано, что мутации, снижающие скорость размножения, возникают с частотами 10-4, тогда как повышающие ее мутации — с частотами 4·10-9 на клетку [6]. Способность Sym-плазмид широко специфичных ризобий функционировать в неродственных донору реципиентах может быть результатом адаптации этих бактерий к функционированию в клубеньках разнородных хозяев. Особенностью некоторых ризобий является локализация sym-генов в составе специальных геномных элементов — «симбиотические острова» (СОС). После переноса в штамм-реципиент СОС обычно встраиваются в гены фен-тРНК или вал-тРНК, что характерно для мобильных геномных островов, кодирующих разнообразные (в том числе и патогенные) свойства бактерий [6]. Будучи лишенными собственной системы репликации, СОС могут переноситься между разными штаммами Mesorhizobium spp. с помощью интегразы типа Р 4. СОС были выявлены также у некоторых штаммов Bradyrhizobium, которые способны передавать свои sym-гены в почвенные и ассоциированные с растениями бактерии.
Отличительной особенностью СОС является их сниженное, по сравнению с другими частями генома, содержание ГЦ (гуанин + цитозин) пар оснований, что типично для ДНК-элементов, подвергающихся интенсивному переносу в популяциях. Эволюционное значение этого переноса заключается в том, что он может приводить к быстрому преобразованию свободноживущих бактерий в симбиотически активные форм.
Следует подчеркнуть, что по интенсивности переноса генов ризобии значительно уступают энтеробактериям (Escherichia, Salmonella), которые имеют системы для высокочастотного переноса генов (F- и F-факторы, эффективные трансдуцирующие фаги), и тем не менее проявляют строго клональную популяционную структуру [8]. Фактически все перечисленные микроорганизмы находятся в почве и попадают в продукты и препараты вместе с растениями. (Табл. №1)
В таблице 2 приведены различные микроорганизмы, которые идентифицированы при анализе различных типов сырья природного происхождения и различных групп лекарственного растительного сырья. Сравнительный анализ подтверждает их идентичность. Для получения качественных и безопасных пищевых и лекарственных препаратов целесообразно перейти на анализ и управление микробиологическим риском.
Таким подходом является анализ микробиологического риска (АМР). Понятие микробиологического риска есть функция вероятности наступления отрицательного эффекта для здоровья и величины этого эффекта, как следствия вредного фактора (микроба, микробного токсина), присутствующего в продукте [5]. Можно ли эту угрозу здоровью, вызванную загрязнением среды обитания, оценить количественно? Можно, если проводить анализ микробиологического риска при всех техногенных явлениях.
Методологическую схему принятия решений в отношении микробиололгического риска подразделяют на два крупных блока (по аналогии с методологией Quality Risk Management - QRM) оценку и/или анализ риска и управление риском (см. рис. 3).
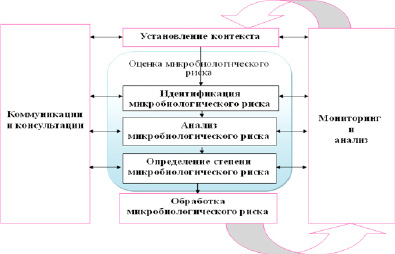
Рис. 3. Оценка риска (голубой цвет) входит центральной частью процесса управления риском (розовый цвет)
Задача первого блока — идентификация микробиологических опасностей, оценка воздействия и его последствий, характеристика микробиологического риска и сравнение его с другими рисками в целях определения степени приемлемости микробиологического риска и выработки приоритетов управления. Задача второго блока — разработка планов действия по снижению и контролю микробиологического риска, оценка их эффективности и выработка рекомендаций для принятия решений по снижению и контролю микробиологического риска в ККТ.
Представленная оценка микробиологического риска [7] проводится в каждой критической контрольной точке жизненного цикла получения пищевого продукта и жизненного цикла получения лекарственного фитопрепарата. Фактически предлагается проводить анализ и управление микробиологическим риском в форме мониторинга продовольственных продуктов и лекарственных препаратов. Для проведения анализа микробиологического риска целесообразно проводить полный анализ различных групп микроорганизмов только на стадии анализа сырья и готового лекарственного препарата. На остальных стадиях жизненного цикла достаточно использовать экспресс-методы анализа общего микробного числа.
Библиографическая ссылка
Габидова А.Э., Галынкин В.А., Тихонович И.А. РЕЗИСТЕНТНОСТЬ И АНАЛИЗ МИКРОБИОЛОГИЧЕСКОГО РИСКА В ФАРМАЦИИ // Международный журнал прикладных и фундаментальных исследований. 2016. № 12-7. С. 1307-1315;URL: https://applied-research.ru/ru/article/view?id=11034 (дата обращения: 23.05.2026).
DOI: https://doi.org/10.17513/mjpfi.11034

