По данным ВОЗ, ежегодно диагноз «рак» ставят 14 млн человек в мире. К 2020 году прогнозируется, что количество больных увеличится до 19 млн. В Казахстане ежедневно выявляется 100 новых случаев онкологических заболеваний. Опухоли головного мозга (далее ГМ) составляют до 5 % в структуре онкологических заболеваний центральной нервной системы и встречаются в любом возрасте. Опухоли головного мозга у детей в Казахстане на протяжении многих лет занимают второе место в структуре онкологической патологии детского возраста и составляет 11 % [1, 2]. До сегодняшнего дня в 4—5 % случаев опухолей ГМ допускаются диагностические ошибки. Поэтому исследования опухолей ГМ с применением позитронно-эмиссионной томографии с компьютерной томографией (далее ПЭТ/КТ) с использованием изотопов 18F нашли широкое применение и являются нередко основным методом для решения вопроса о тактике лечения пациента. Среди злокачественных новообразований ГМ преобладают глиомы (77 %) и метастазы из опухолей вне мозговой локализации [3]. Некоторые опухоли головного мозга, такие как медуллобластомы или доброкачественные астроцитомы мозжечка, развиваются главным образом только у детей.
Цель работы. Выбор оптимального радиофармпрепарата и применение его на ПЭТ/КТ в Казахстане для диагностики опухолей головного мозга.
Материалы и методы исследования
Позитронно-эмиссионная томография – это метод ядерной медицины, позволяющий оценить работу (функцию) органов и тканей, и в котором для получения изображений используют радиофармпрепараты (РФП), меченные позитрон-излучающими ультракороткоживущими радионуклидами (УКЖР). Основным доводом в пользу применения УКЖР явилось то обстоятельство, что их применение позволяет уменьшить время исследования и радиационную нагрузку на больного, так как большая часть препарата распадается уже во время исследования. Кроме того, многие элементы, имеющие позитрон-излучающие УКЖР, такие как 11C, 13N, 15O, а также 18F (выступает как аналог водорода), принимают самое активное участие в большинстве биологических процессов человеческого организма. Наряду с этим появляются новые изотопы для ядерной медицины. Так, например, 64Cu и 67Cu являются перспективными медицинскими радиоизотопами, подходящими для мечения многих радиофармпрепаратов для молекулярной визуализации и радиоиммунотерапии, так как они обладают благоприятными физическими свойствами. Они излучают как g-лучи (для томографии), так и g-лучи (для терапии) в своих распадах до основных состояний 64Zn и 67Zn, соответственно [4]. Методом ПЭТ/КТ можно исследовать любую функцию организма. Потенциал ПЭТ/КТ в значительной степени определяется арсеналом доступных радиофармпрепаратов.
Радиофармацевтическим препаратом – РФП называется химическое соединение, содержащее в своей молекуле определенный радиоактивный нуклид, разрешенное для введения человеку с диагностической или лечебной целью. Отличительной особенностью диагностического РФП при этом является отсутствие фармакологического эффекта. Разнообразие существующих РФП позволяет выбрать оптимальный вариант, в зависимости от целей исследования для наиболее адекватной ПЭТ-методики. В клинических исследованиях в подавляющем большинстве случаев применяется 18F-ФДГ. Причина широкого использования ФДГ в универсальности этого препарата. Высокий уровень накопления в патологических очагах по отношению к фону позволяет легко их идентифицировать, что делает ФДГ незаменимым в диагностике в первую очередь онкологических заболеваний, несмотря на наличие накопления и в активных воспалительных клетках, как гранулоциты и макрофаги.
Для получения РФП необходимо наличие ПЭТ-центра. В структуру ПЭТ-центра входят медицинский циклотрон, радиохимическая лаборатория по производству РФП и один или несколько ПЭТ томографов. Для комплексной оценки менингиом и их распространенности требуется ретроспективное совмещение разномодальных изображений, (например, ПЭТ/КТ с соответствующими МРТ-срезами), что является важной предпосылкой для правильной топографо-анатомической интерпретации находок. В любом случае возможность клинических исследований в каждом центре, в первую очередь, обусловлена доступностью конкретных РФП [5].
В отделе радиоизотопной диагностики Республиканского диагностического центра в настоящее время проводятся исследования на ПЭТ/КТ с применением РФП 18F- ФДГ для диагностики злокачественных опухолей, в том числе и опухолей головного мозга. За период с 2013 г. по 2016 г. проведено 28 исследований первичных опухолей головного мозга. Все пациенты были направлены после оперативного, лучевого или химиотерапевтического лечения. Среди них мужчин – 12 чел. (42,9 %), женщин – 11 чел. (39,3 %), детей (до 15 лет) – 5 чел. (17,8 %). По морфологической структуре опухоли ГМ пациентов было: с медуллобластомой – 8 чел. (28,6 %), астроцитомой – 5 чел. (17,8 %), анапластической глиобластомой – 6 чел.(21,4 %), олигодендроглиомой – 4 чел. (14,3 %), менингиомой – 5 чел. (17,8 %). После исследования у 25 пациентов (89,3 %) рецидива опухоли не выявлено (была корреляция с МРТ), у 3 пациентов (10,7 %) – сложно дифференцировать лучевой патоморфоз с продолженным ростом опухоли.
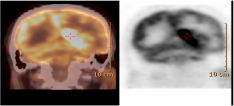
Рис. 1. Пациентка У.К., 65 лет, на ПЭТ/КТ с 18F-ФДГ опухоль головного мозга (глиобластома) в левой теменно-затылочной области
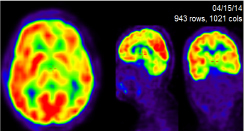
Рис. 2. ПЭТ/КТ с 18F-FDG головного мозга (состояние после лучевой терапии левой гемисферы по поводу олигодендроглиомы)
Результаты исследования и их обсуждение
По результатам наших исследований и по литературным данным, не все опухоли головного мозга возможно диагностировать на ПЭТ/КТ с использованием 18F-ФДГ.
Информативность ПЭТ с РФП при диагностике первичных опухолей ГМ [6].
|
Исследование |
Чувствительность, % |
Специфичность, % |
Диагностическая точность, % |
|
ПЭТ/КТ с 18F- ФДГ |
80–86 |
80–93 |
– |
|
ПЭТ/КТ с 18F- ФДГ (собственные данные) |
82 % |
89 % |
|
|
ПЭ/Т/КТ с 18F- ФЭТ |
93–95 |
96–99 |
97–98 |
Известно, что для оценки эффективности проведенного лечения используется целый ряд РФП, таких как, 11С-МЕТ, 18F- ФЭТ, 18F- ФДГ и 11С-БН. Для получения РФП на основе изотопа 11С необходима дополнительная мишень, и в условиях нашего центра этот вопрос пока не рассматривается. Недостатки 18F- ФДГ, такие как повышенное накопление этого РФП в коре ГМ и отсутствие гиперфиксации во многих опухолях мозга, предполагают необходимость использования других туморотропных РФП. Поэтому мы изучили другие РФП для диагностики опухолей ГМ. В настоящее время для планирования биопсии и дифференциальной диагностики рецидивов опухолей и постлучевых изменений наиболее широко используется ПЭТ с мечеными аминокислотами (далее АК) фтор-этил-тирозином (далее 18F- ФЭТ). Этот метод широко применяется также для планирования лучевой терапии. Важным преимуществом меченых АК в диагностике опухолей мозга и их рецидивов является тот факт, что нарушение проницаемости гематоэнцефалического барьера (далее ГЭБ) не влияет на их захват в опухолях ГМ. Было показано, что 18F- ФЭТ не накапливается в участках лучевого некроза [7]. Он имеет очень высокую специфичность для визуализации опухолей головного мозга (глиом) и применяется, в частности, для их разграничения от здоровой ткани (например, при планировании лучевой терапии) и для ранней диагностики рецидивов. Нами, совместно с учеными Клиники Vivantes г. Берлин и производственной базы ядерной медицины г. Юлих (Германия) проведена обработка данных по производству, контролю качества и использования ультра-короткоживущего РФП 18F-ФЭТ для клинического применения в нейроонкологии.
L-[18F] ФЭТ не накапливался в костном мозгу, почке или поджелудочной железе и, таким образом, может иметь применение в обнаружении периферических опухолей. Поглощение 18 F- ФЭТ в опухолевых клетках значительно выше, чем в макрофагах или гранулоцитах [7]. В естественных условиях, ФЭТ является метаболически стабильным. Процент неповрежденного ФЭТ из общей радиоактивности в плазме после внутривенного введения у людей составляет примерно 95 % через 5 мин после инъекции и примерно 87 % через 120 мин. Эти данные показывают, что доля метаболитов в плазме крови человека остается низкой во время исследования ПЭТ. Было обнаружено, что процент интактной ФЭТ в моче составляет 72 +/- 5 % через 60 мин и 61 p.i. +/- 3 % через 150 мин p.i. Метод ПЭТ/КТ с использованием 18F- ФЭТ – имеет очень высокую специфичность для визуализации опухолей головного мозга (глиом) и применяется, в частности, для их разграничения от здоровой ткани (например, при планировании лучевой терапии) и для ранней диагностики рецидивов.
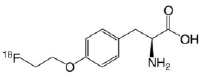
Химическая структура
Несколько исследований показали, что внутриопухолевое накопление 18 F- ФЭТ не зависит от нарушения гематоэнцефалического барьера. Поглощение ФЭТ в опухолях зависит от скорости ангиогенеза и плотности опухолевых клеток (9). Увеличенное поглощение 18F- ФЭТ иногда наблюдается в пост-терапевтических поражениях, возможно, вследствие пассивного притока трейсера. Это неспецифическое поглощение 18F- ФЭТ менее интенсивно и показывает более однородную картину по сравнению с поглощением 18F- ФЭТ в опухолевой ткани.
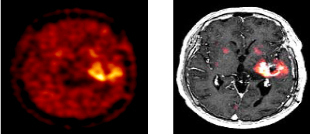
Рис. 3. Пациент А.А., 42 года. На ПЭТ/КТ с 18F- ФЭТ глиобластома левого полушария головного мозга
Перед применением препарата должен быть выполнен контроль качества в соответствии со стандартом GMP (good manufacturing practice), чтобы показать, что продукт безопасен для применения на пациенте и сохраняет свои качества в течение срока годности без особых изменений. Основными критериями качества для РФП [18F] ФЭТ являются концентрация радиоактивности > 95 % МБк / мл, радиохимическая чистота [18 F] ФЭТ> 95 % и [18F] фторид <5 %, измерение короткоживущих изотопов [18F]> 99 %. Определение химической чистоты и контроль химических примесей, в зависимости от способа получения, проводится в соответствии со стандартами ISOO. (2–[18F] фторэтил)-L-тирозин (ФЭТ) применяется внутривенно в виде болюсной инъекции. Эффективная доза согласно МКРЗ 60 (Международная комиссия по радиологической защите) составляет 16,5 m Sv / МБк для взрослых (масса тела 70 кг), что соответствует эффективной дозе 3,3 мЗв в ПЭТ исследованиях с использованием максимальной дозировки ФЭТ 200 МБк. Для очень маленьких детей минимальная доза 70 МБк необходима для получения изображения достаточно высокого качества, что эквивалентно экспозиции облучения 1,1 мЗв. Максимально необходимая доза составляет 200 МБк. Учитывая лучевую экспозицию, вызванную низкой дозой КТ мозга 1,2 мЗв, суммарная эффективная доза, вызванная исследованием ПЭТ / КТ с 18F-ФЭТ, составляет 2,3 – 6,1 мЗв [10].
Заключение
Производство и синтез РФП- L-[18F] ФЭТ его высокая стабильность в организме, быстрая кинетика накопления в мозгу и опухоли, его малое накопление в неопухолевой ткани и его простота синтеза, определяют дальнейшую оценку L-[18F] ФЭТ, как индикатора аминокислоты для опухолей головного мозга. В большинстве случаев, 18F- ФЭТ- ПЭТ позволяет четкое разграничение между новообразованиями и острыми воспалительными поражениями, а также между рецидивом и постлучевым некрозом. Также выявлено, что 18F- ФЭТ -ПЭТ/КТ информативна при оценке эффективности в дифференциальной диагностике рецидивов от постлучевых изменений у больных с метастатическим поражением головного мозга после стереотаксической радиохирургии [11].
В Казахстане пока еще нет серийного производства РФП. Известными производителями являются США, Япония, Германия и ряд других стран. В этом направлении нами ведется тесное сотрудничество с учеными Университета Charite и Клиники Vivantes г. Берлин, производственной базой ядерной медицины г. Юлих (Германия), Университетом Кюсю г. Фукуока, Япония.
Полноценная диагностика, совмещающая в себе компьютерную и позитронно-эмиссионную томографию с использованием более чувствительного РФП- 18F- ФЭТ, заметно снижает необходимость повторного лечения. Выявление опухолей головного мозга на ранней стадии сокращает затраты на лечение в несколько раз.
Библиографическая ссылка
Рыскулова Г.О., Прмантаева Б.А., Рыскулов А.Е., Бaйдуллaeвa Г.E. АНАЛИЗ ВОЗМОЖНОСТИ ПЭТ/КТ С 18F- ФДГ И ПЭТ/КТ С 18F- ФЭТ В ДИАГНОСТИКЕ ОПУХОЛЕЙ ГОЛОВНОГО МОЗГА // Международный журнал прикладных и фундаментальных исследований. 2017. № 9. С. 74-78;URL: https://applied-research.ru/ru/article/view?id=11829 (дата обращения: 16.05.2026).

