В настоящее время богатые и легкообогатимые месторождения руд благородных и цветных металлов практически отработаны, основой современной минерально-сырьевой базы Российской Федерации преимущественно составляют труднообогатимые бедные, тонковкрапленные и труднообогатимые руды. К таким рудам относятся золотомышьяковистые руды, это связано с тесной ассоциацией золота с мышьяксодержащими минералами. Такое золото называется невидимым, так как не поддается обнаружению оптическими методами. Упорные руды для достижения приемлемого уровня извлечения золота при их последующем цианировании требуют предварительной переработки. Все методы предварительной обработки сводятся к разрушению минеральной матрицы с целью высвобождения золота.
Термический анализ (калориметрия) – метод исследования физико-химических процессов, основанный на регистрации тепловых эффектов, сопровождающих превращения веществ в условиях программирования температуры. Данный метод широко применяют не только в аналитической химии, но и в геологии для идентификации различных минералов и горных пород. Также следует отметить, что термический анализ удобен при лабораторных исследованиях, не требует большого объема исходного материала и его возможно применять как экспресс-метод исследования минерального сырья. Особенно полезным данный метод может оказаться для упорного золотосодержащего сырья (в том числе сульфидного), из-за большой трудоемкости и сложности пробирного анализа [1].
Для подтверждения ранее полученных результатов термодинамического моделирования и расчета кинетических параметров обжига скородита были проведены исследования по термическому разложению скородита и пирита (монофракции), а также смеси скородита и пирита в соотношении 3:1 [2].
Материалы и методы исследования
Объектами исследования являлись: золотосодержащая окисленная скородитовая руда месторождения Козловское (Калганский район, Забайкальский край). По данным минералогического анализа руда содержит: кварц – 54 %, скородит – 35 %, полевые шпаты и алюмосиликатные породы – 11 %. В исследуемой пробе руды ценными компонентами являются золото (16,9 г/т) и серебро (52,5 г/т). А также некондиционный пиритный концентрат бывшего вольфрамо-молибденового комбината (г. Закаменск, Республика Бурятия). По данным химического анализа пиритный концентрат содержит, %: Sобщ – 38,3, Fe – 35,8, SiO2 – 24,2, Pb – 0,81, Zn – 0,78. Пиритный концентрат возможно использовать в качестве сульфидизатора при обжиге в атмосфере перегретого водяного пара [3].
Термический анализ проводили методом дифференциальной термогравиметрии (ДТГ) и дифференциальной сканирующей калориметрии (ДСК) с использованием прибора синхронного термического анализа Netzsch STA 449 F1 Jupiter.
Термограммы снимали в платиновых тиглях при следующих условиях: атмосфера – аргон, температурный интервал 20–1000 °С, режим нагрева – линейный, скорость нагрева образцов 10 °С/мин, масса навесок 15–20 мг. В процессе нагрева фиксировались изменения массы исследуемого образца минерала (кривая ТГ), скорость изменения массы (кривая ДСК), температура (T), а также тепловые эффекты реакций (Дж/г).
Результаты исследования и их обсуждение
Данные анализа, представленные на рис. 1, свидетельствуют о том, что разложение скородита происходит в 3 этапа. На кривых ДСК и ТГ видно, что в диапазоне температур 162–215 °С происходит потеря массы (до 5,35 %), с поглощением значительного количества теплоты (–205,3 Дж/г). Что объясняет потерю воды из скородита:
FeAsO4 • 2H2O → FeAsO4 + 2H2O ↑. (1)
При температуре 466–488 °С со значительной потерей массы (19,25 %) протекает процесс разложения безводного скородита по формуле
2FeAsO4 → Fe2O3 + As2O5. (2)
При нагревании образца выше 550 °С наблюдается экзотермичный пик (7,15 Дж/г), который указывает на разложение As2O5:
As2O5 → As2O3 + О2 ↑. (3)
По данным РФА конечным продуктом разложения скородита является магнетит (Fe3O4).
Термическое разложение пирита хорошо описано рядом авторов [4, 5]. Термограмма, представленная на рис. 2, получена на образце монофракции пирита, показывает, что разложение пирита происходит также в 3 этапа. В диапазоне температур 491–549 °С происходит термическая диссоциация пирита с образованием элементарной серы при незначительной потере массы с эндотермическим эффектом (–41,89 Дж/г):
2FeS2 → 2FeS + S2. (4)
При дальнейшем повышении температуры наблюдается значительный эндотермический пик с наибольшей потерей массы (16,19 %), объясняется это дальнейшим разложением пирита по суммарной реакции:
4FeS2 + 11О2 → 2Fe2O3 + 8SO2. (5)
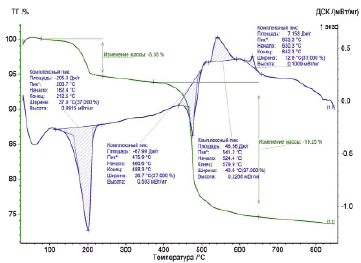
Рис. 1. Термограмма разложения скородита
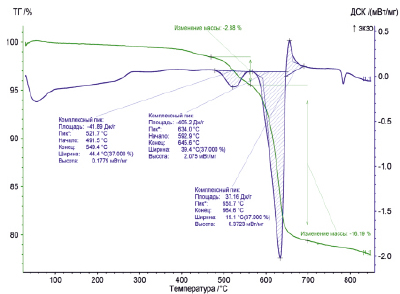
Рис. 2. Термограмма разложения пирита
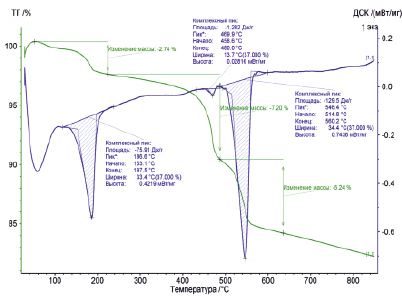
Рис. 3. Термограмма разложения смеси скородита и пирита
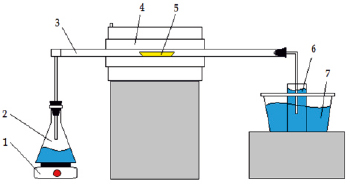
Рис. 4. Схема лабораторной установки для обжига в атмосфере перегретого водяного пара: 1 – нагреватель; 2 – сосуд с дистиллированной водой; 3 – реактор; 4 – печь; 5 – лодочка с рудой; 6 – контрольный раствор; 7 – емкость охлаждения контрольного раствора
Ввиду недостатка кислорода вероятно протекание следующей реакции:
3FeS2 + 8О2 → Fe3O4 + 6SO2. (6)
Конечным продуктом разложения пирита является пирротин (FeS), а также незначительное количество магнетита (Fe3O4).
Наибольший интерес вызывает термограмма разложения смеси скородита и пирита 3:1 (рис. 3), в данной пропорции смесь будет поступать на сульфидизирующий обжиг. При достижении интервала температур 153–197 °С происходит некоторая потеря массы (2,74 %), с поглощением значительного количества теплоты. Полученный эндотермический пик указывает на потерю воды скородитом.
На кривых ТГ и ДСК показано, что максимальная потеря массы (суммарно до 13,4 %) происходит при температуре 450–590 °С, также имеется максимальный эндотермический пик (–129,5 Дж/г), наиболее вероятно, что в этом интервале температур происходит разложение скородита и пирита, а также сульфидирование выделившегося оксида мышьяка элементарной серой. Конечными продуктами реакций являются магнетит (Fe3O4) и пирротин (FeS). Весь мышьяк выделяется в газовую фазу.
Для подтверждения результатов термического анализа были проведены экспериментальные лабораторные исследования для определения конечных продуктов обжига в атмосфере перегретого водяного скородитовой руды и пиритного концентрата на лабораторной установке «проточного» типа (рис. 4).
Данная лабораторная установка состоит из четырех основных узлов – электропечи, нагревателя, реактора и сосуда с поглотителем газов. Температура в реакторе измеряется термопарами типа ХА и регулируется микропроцессорным электронным терморегулятором МПРТ-22, который был установлен для автоматизации процесса обжига. При достижении требуемой температуры обжига в реактор подавали перегретый водяной пар, затем загружали алундовую лодочку с навеской скородитовой руды и пиритного концентрата массой от 2 до 3 г. Началом процесса обжига считали момент ввода навески шихты. Температура обжига 700 °С, продолжительность обжига 25 минут. Полученные огарки подвергались рентгенофазовому анализу.
На рис. 5 представлена рентгенограмма полученных огарков, установлено, что после обжига конечными железосодержащими фазами являются магнетит (Fe3O4) и пирротин (FeS).
Таким образом, на основании проведенных исследований установлены температурные диапазоны при разложения исследуемых минералов, а также преобладание эндотермических эффектов. Экспериментально подтверждено, что при обжиге смеси скородитовой руды и пиритного концентрата в соотношении 3:1 (температура обжига 700 °С, продолжительность обжига 25 минут), в атмосфере перегретого водяного пара конечными продуктами являются магнетит (Fe3O4) и пирротин (FeS).
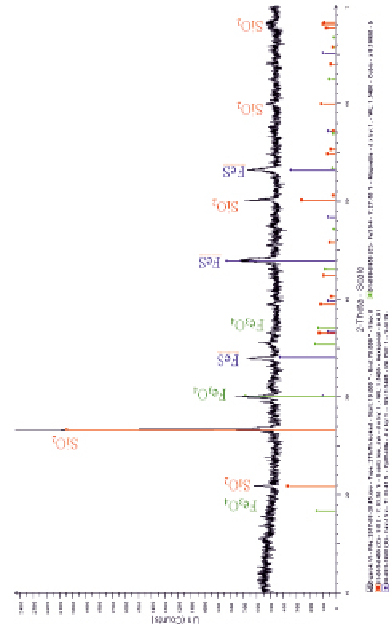
Рис. 5. Рентгенограмма огарка
Выводы
Выполнены исследования по термическому разложению монофракций скородита и пирита в атмосфере аргона. Определены температурные диапазоны и тепловые эффекты при разложении монофракций скородита, пирита и их смеси в соотношении 3:1. Показано преобладание эндотермических эффектов при разложении исследуемых минералов в инертной атмосфере. Результаты данного исследования помогут оптимизировать процесс обжига золотосодержащей скородитовой руды с пиритным концентратом в атмосфере перегретого водяного пара.
Библиографическая ссылка
Гуляшинов П.А., Палеев П.Л., Гуляшинов А.Н. ИЗУЧЕНИЕ ПРОЦЕССА ТЕРМИЧЕСКОГО РАЗЛОЖЕНИЯ СКОРОДИТА И ПИРИТА // Международный журнал прикладных и фундаментальных исследований. 2017. № 12-1. С. 22-27;URL: https://applied-research.ru/ru/article/view?id=11956 (дата обращения: 31.03.2026).

