Производные фенилбензимидазола нашли широкое применение в различных областях человеческой деятельности. 2-фенилбензимидазол (ФБИ) и 2-фенилбензимидазол-5-сульфоновая кислота (ФБИ-сульфоновая кислота) являются эффективными УФ-фильтрами. 2-ФБИ сульфоновая кислота входит в состав солнцезащитных средств [1]. ФБИ также представляет собой эффективный ингибитор атмосферной коррозии стали [2], используется в проявительных материалах для фотографии, а также как фунгицид. Флуоресцентные зонды на основе красителей фенилбензимидазольного ряда используются в диагностике [3]. Комплексы металлов с фенилбензимидазолом составляют основу органических светоизлучающих диодов [4]. Для селективного определения сульфид-ионов в воде служат датчики на основе фенилбензимидазола [5]. 6,4´-диамино-2-фенилбензимидазол используются в качестве мономера для производства арамидных нитей, используемых для изготовления продукции особого назначения и обладающих уникальными свойствами [6]. Требования к чистоте мономера, используемого в промышленности, чрезвычайно высоки, поэтому способы синтеза [7] и методы контроля качества этого соединения постоянно совершенствуются [8]. Спектрально-люминесцентные и кислотно-основные свойства фенилбензимидазола и его аминопроизводных были предметом исследования в ряде работ [9, 10]. В то же время фотохимические свойства этих соединений остаются малоизученными. Исключение составляет фенилбензимидазолсульфоновая кислота, фотодеградация которой исследуется в последние двадцать лет в связи с ее широким использованием в косметике [1, 11].
Цель исследования: изучение воздействия УФ-излучения на растворы 6,4´-диамино-2-фенилбензимидазола, 4´-амино-2-фенилбензимидазола и 6-амино-2-фенилбензимидазола методами абсорбционной и люминесцентной спектроскопии.
Материалы и методы исследования
Объектами исследования были 2-фенилбензимидазол (ФБИ), 4´-амино-2-фенилбензимидазол (АФБИ), 6-амино-2-фенилбензимидазол (ФАБИ), 6,4´-диамино-2-фенилбензимидазол (ДАФБИ), 6,4´-дибензоиламино-2-фенилбензимидазол (ДБАФБИ). Использовали ФБИ (Aldrich Chemical, 99 %), другие производные фенилбензимидазола были синтезированы и очищены в ИНЭОС. Все растворители имели квалификацию «для спектроскопии». Чистоту объектов исследования и растворителей проверяли по спектрам поглощения и на присутствие люминесцирующих примесей. Концентрация исследуемых растворов варьировалась от 5·10-5 до 2·10-7 моль/дм3. Спектры поглощения записывали на спектрофотометре Perkin Elmer 554 и UV-1800 Shimadzu. Спектры флуоресценции и возбуждения флуоресценции регистрировали на спектрофлуориметре MPF 44 Perkin Elmer и СМ2203 Solar с термостатом в кварцевых кюветах с толщиной поглощающего слоя 1 см. Для облучения растворов использовали ртутную лампу ДРШ-1000 и азотный лазер ЛГИ-505 с длиной волны 337 нм и импульсной мощностью 15 кВт. Облучение проводили в кварцевых кюветах с толщиной поглощающего слоя 1 см. При облучении растворов нефильтрованным светом лампы ДРШ-1000 использовали воздушное охлаждение. Облученные растворы анализировали на число компонентов путем определения ранга матрицы оптических плотностей по методу Уоллеса – Каца [12]. Концентрацию исходного вещества в облученных растворах определяли по интенсивности его флуоресценции. На основании этих данных строили кинетические зависимости расходования исходного соединения. Квантовый выход фотолиза (Ф) определяли в соответствии с [13].
Результаты исследования и их обсуждение
Среди исследованных соединений особый интерес представляет ДАФБИ, поскольку является мономером для получения полимеров с ценными термомеханическими свойствами. Фотохимические свойства ДАФБИ изучали в этанольных и щелочно-этанольных растворах, а также в ДМСО. Картина изменений спектров поглощения при облучении растворов в разных растворителях имела сходный характер. Спектр поглощения ДАФБИ в этаноле состоит из двух широких полос с максимумами при 336 и 278 нм [10]. При облучении этанольного раствора нефильтрованным светом ртутной лампы ДРШ-1000 его спектр поглощения претерпевает значительные изменения. Длинноволновая полоса испытывает гипсохромный сдвиг, ее интенсивность падает. В области 380–600 нм появляется широкое бесструктурное поглощение. В начальный период реакции (время облучения 1 мин 15 с) в серии спектральных кривых наблюдается 3 изобестические точки при 231, 317 и 360 нм. По мере увеличения времени облучения изобестика нарушается, меняется вид длинноволнового поглощения и исчезает полоса поглощения ДАФБИ с максимумом при 336 нм. Характер спектральных изменений указывает на то, что сначала образуется один продукт реакции, который затем также становится участником фотохимических превращений. Число поглощающих компонентов в растворе, облученном в течение 20 мин, равно 4.
Использование селективного лазерного возбуждения с длиной волны 337 нм не приводит к принципиальному отличию характера спектральных изменений раствора ДАФБИ в этаноле (рис. 1, а). Однако изобестические точки (231, 318 и 262 нм), наблюдаемые в серии спектров поглощения облученных растворов, сохраняются в течение 7 мин, и даже для раствора ДАФБИ, облученного в течение 13 мин, изобестика нарушается незначительно. Число компонентов в этом растворе равно 3, что находится в соответствии с наблюдаемыми спектрами возбуждения флуоресценции. Этанольные растворы, облученные лазером при комнатной температуре, кроме свечения ДАФБИ (λmax = 423 нм), при возбуждении в области максимума длинноволнового поглощения – длиной волны 430 нм обнаруживают слабое свечение с максимумом при 460 нм. В спектрах возбуждения флуоресценции при регистрации на длинах волн 490 и 520 нм имеются два максимума при 355 и 385 нм.
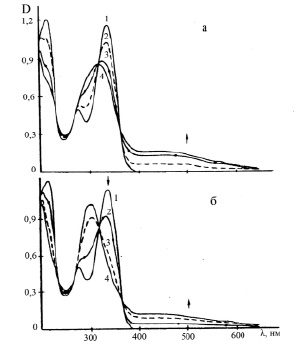
Рис. 1. Спектры поглощения исходного (1) раствора ДАФБИ и их изменения (2–4) при облучении растворов лазером ЛГИ с длиной волны излучения 337 нм: 2 – 2 мин, 3 – 7 мин, 4 – 13 мин; а – этанол, б – этанол с добавлением щелочи СКОН = 10-4 М
При добавлении в этанольный раствор щелочи в концентрации 10-3–10-4 М изменения спектра поглощения не происходит, что является свидетельством того, что в растворе присутствует нейтральная форма соединения. Под действием лазерного излучения с длиной волны 337 нм наблюдали исчезновение длинноволновой полосы поглощения ДАФБИ и появление другой полосы с λmax = 300 нм. В спектрах поглощения облученных растворов имеются 3 изобестические точки при 232, 317 и 365 нм (рис. 1, б), очень близкие значения, наблюдаемые для нейтральных этанольных растворов. Анализ матрицы оптических плотностей с использованием λ = 288, 300, 318, 332, 340 и 366 нм приводит к рангу матрицы оптических плотностей, равному 2, а с λ = 300, 332, 380, 400, 480 и 560 нм – число компонентов равно 4. Щелочно-этанольный раствор, облученный лазером в течение 20 мин при возбуждении в области максимума длинноволнового поглощения при комнатной температуре не флуоресцирует. При 77 °К возбуждение длиной волны 450 нм приводит к слабому свечению с λmax = 505 нм, а при возбуждении длиной волны 520 нм – к еще более слабому свечению с максимумом при 560–570 нм. Спектр возбуждения флуоресценции при регистрации на длине волны 580 нм имеет максимум при 475 нм.
Моноаминопроизводные ФБИ с аминогруппой в фенильном кольце и бензимидазольном цикле также подвержены фотолизу под действием УФ-излучения, при этом характер изменения спектров поглощения при облучении различен для АФБИ и ФАБИ и зависит от положения аминогруппы в молекуле. Облучение этанольных растворов АФБИ приводит к падению интенсивности полосы поглощения с λмакс = 316 нм и росту интенсивности широкой длинноволновой полосы с λмакс = 384 нм. Анализ матрицы оптических плотностей свидетельствует о том, что имеет место последовательный фотолиз соединения. В течение 5 мин облучения образуется только один фотопродукт, а по мере его накопления при увеличении времени облучения начинается его разложение (рис. 2). Спектр поглощения облученного раствора указывает на то, что продуктом реакции, ответственным за длинноволновое поглощение, является соединение хиноидной структуры.
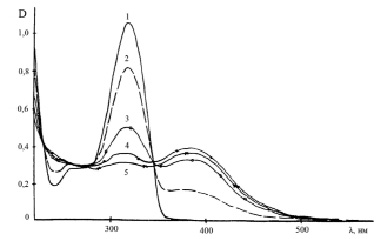
Рис. 2. Спектр поглощения щелочно-этанольного раствора АФБИ (1) и его изменения (2–5) при облучении нефильтрованным светом ртутной лампы ДРШ-1000. Время облучения: 2 – 30 с, 3 – 2 мин, 4 – 5 мин, 5 – 11 мин СКОН = 10-4 М
Иная картина наблюдается при облучении этанольного раствора ФАБИ: полоса поглощения с λмакс = 328 нм уменьшается и наблюдается ее небольшой гипсохромный сдвиг до 322 нм. В коротковолновой области растет полоса с λмакс = 280 нм, а в длинноволновой в течение первых двух минут при использовании нефильтрованного света ДРШ-1000 наблюдаются лишь небольшие изменения. По мере дальнейшего облучения наблюдается падение интенсивности полос с λмакс = 322 нм и λмакс = 280 нм. Спектр поглощения раствора ФАБИ, облученного 14 мин, представляет собой бесструктурную полосу с λмакс = 322 нм. Гипсохромный сдвиг в спектрах поглощения облученных растворов свидетельствует о фрагментации молекулы ФАБИ с образованием соединения, π-система которого меньше, чем у исходной молекулы.
Следует отметить, что в большинстве случаев характерной особенностью облученных растворов в подавляющем большинстве случаев является наличие бесструктурного длинноволнового поглощения в виде «хвоста». Спектральные особенности растворов исследованных соединений позволяют предположить, что одним из продуктов фотолиза ФБИ и его аминопроизводных является азометин с заместителями при двойной связи. Как было показано в [14], благодаря возможности двойственного включения группы –С=N- в сопряжение, молекулы азометинов обладают неплоской конформацией. Такое строение обуславливает, в частности, отличие спектра поглощения бензальанилина от изоэлектронных ему молекул, например стильбена и фенилбензимидазола. Характерной особенностью спектров поглощения азометиновых соединений является наличие длинноволнового долго не спадающего поглощения [14]. Сравнение спектров облученных растворов АФБИ и ФАБИ обнаруживает качественные отличия, которые связаны с положением аминогруппы в молекуле. Возможно, длинноволновое поглощение облученных растворов АФБИ и ДАФБИ обусловлено, в том числе, образованием димеров и соединений хиноидной структуры, имеющих протяженную π-систему, и вызвано наличием аминогруппы в фенильном кольце. Так, при действии УФ-излучения на водный раствор анилина наблюдались аналогичные спектральные особенности облученных растворов. Соотношение продуктов реакции зависит как от положения аминогруппы в соединении, так и от кислотности среды. Облучение этанольного раствора АФБИ приводит к продукту, поглощающему в длинноволновой области (рис. 2), а облученный раствор ФАБИ имеет интенсивную коротковолновую полосу и едва заметный «хвост» (рис. 3). Важную роль в фотохимических превращениях играет монопротонированная форма этих соединений, поскольку в возбужденном состоянии протоноакцепторные свойства пиридинового атома азота бензимидазольного цикла возрастают на 3–4 порядка [9]. Зависимость соотношения продуктов реакции от кислотности среды демонстрирует рис. 1. Так, облученный этанольный раствор ДАФБИ имеет более интенсивное длинноволновое поглощение и менее интенсивную коротковолновую полосу, чем щелочно-этанольный раствор этого соединения.
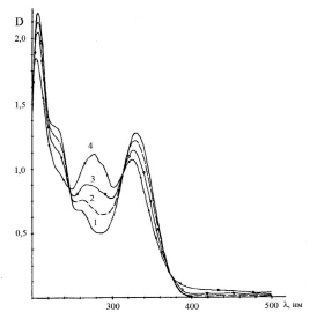
Рис. 3. Спектры поглощения этанольного раствора ФАБИ, облученного нефильтрованным светом ртутной лампы ДРШ-1000. Время облучения: 1 – 0; 2 – 15 с; 3 – 30 с; 4 – 1 мин
ФБИ и его аминопроизводные относительно легко вступают в фотохимические реакции, квантовые выходы фотолиза исследованных соединений представлены в таблице. Замена аминогрупп на бензоиламиногруппы не приводит к характерным изменениям спектров поглощения облученных растворов, однако фотолиз ДБАФБИ протекает менее эффективно. Вероятно, причиной фотохимической устойчивости бензоилпроизводного ФБИ является преобладание процессов деградации энергии электронного возбуждения.
Квантовый выход фотолиза ФБИ и его производных
|
Соединение |
Длина волны облучения, нм |
Растворитель |
Квантовый выход |
|
ФБИ |
313 (ДРШ-1000) |
Этанол |
0,1 |
|
АФБИ |
313 (ДРШ-1000) |
Этанол, 10-4М КОH |
0,13 |
|
ФАБИ |
313 (ДРШ-1000) |
Этанол |
0,15 |
|
ДАФБИ |
337 (ЛГИ) |
Этанол |
0,2 |
|
ДБАФБИ |
337 (ЛГИ) |
Этанол |
0,02 |
Заключение
Фотолиз аминопроизводных фенилбензимидазола протекает с образованием нескольких продуктов реакции. Наличие аминогруппы в фенильном кольце молекулы обуславливает длинноволновое поглощение облученных растворов 6,4´-диамино-2-фенилбензимидазола и 4´-амино-2-фенилбензимидазола. Гипсохромный сдвиг в спектрах поглощения облученных растворов 6-амино-2-фенилбензимидазола свидетельствует о фрагментации молекулы с образованием соединения, π-система которого меньше, чем у исходной молекулы. Высказано предположение, что одним из продуктов фотолиза является азометин с заместителями при двойной связи –N=C-, другие представляют собой производные бензимидазола а также соединения хиноидной структуры. Важную роль в фотохимических превращениях аминопроизводных фенилбензимидазола играет монопротонированная форма этих соединений, поскольку в возбужденном состоянии протоноакцепторные свойства пиридинового атома азота бензимидазольного цикла на несколько порядков больше, чем в основном. Введение аминогрупп в молекулу фенилбензимидазола увеличивает квантовый выход фотолиза. Квантовый выход фотолиза 6,4´-диамино-2-фенилбензимидазола в 2 раза выше, чем для незамещенной молекулы фенилбензимидазола. Замена аминогрупп на бензоиламиногруппы уменьшает эффективность фотолиза в 10 раз.
Библиографическая ссылка
Некрасова Л.П. ФОТОЛИЗ АМИНОПРОИЗВОДНЫХ ФЕНИЛБЕНЗИМИДАЗОЛА // Международный журнал прикладных и фундаментальных исследований. 2019. № 1. С. 60-65;URL: https://applied-research.ru/ru/article/view?id=12641 (дата обращения: 05.04.2026).

