В отличие от других соединений, лекарственные препараты создаются для направленного воздействия на организм человека. Большинство из них обладает побочным токсическим действием, которое к тому же может увеличиваться по истечении срока годности. В связи с этим проблема уничтожения таких лекарств заслуживает особого внимания.
Фактическими методами утилизации лекарственных препаратов в настоящее время являются: захоронение на специально отведенных полигонах, сжигание на свалках или высокотемпературная обработка в инсинераторах с доступом или без доступа кислорода.
Как показывает международный опыт, захоронение лекарственных препаратов на специальных полигонах и обычных свалках опасно загрязнением почвы, воздуха и водоносных слоев. Неорганизованное открытое сжигание на свалках вместе с прочими отходами представляет особую опасность, поскольку в процессе сгорания помимо окиси углерода в воздух выбрасываются как токсичные соединения (сера, мышьяк, фосфор), так и канцерогенные, в числе которых полициклические ароматические углеводороды (ПАУ), нитрополиарены, нитрозамины, полихлорированные бифенилы и другие бластомогены.
На мусоросжигательных заводах перерабатываются крупнотоннажные отходы фармацевтических производств и больших лечебных объединений, но это далеко не решает проблему. Дело в том, что основное количество неиспользованных препаратов накапливается в семьях, в небольших аптеках и местных больницах. В каждом отдельном случае их объемы невелики, но в сумме они составляют основную массу лекарств, загрязняющих биосферу, поскольку обычно выбрасываются с общим мусором или спускаются в канализацию.
Мировое сообщество давно обеспокоено этой проблемой, поскольку в питьевой воде некоторых регионов были обнаружены следы фенобарбитала и других лечебных препаратов, представляющих опасность. В связи с этим в ряде стран существует практика сбора у населения просроченных лекарств за небольшую плату, проводится разъяснительная работа, на этикетках и в листовках инструкций добавляются сведения, как обращаться с лекарством по истечении срока годности и т.д. [1, 2].
Одной из эффективных мер по предотвращению накопления и бесконтрольного выбрасывания просроченных лекарств в аптеках и небольших лечебных учреждениях явилось использование малотоннажных установок, в которых производится их высокотемпературная обработка с доступом или без доступа кислорода [3]. Такого рода устройства используются и в России для уничтожения медицинских отходов, относящихся по СанПиН 2.1.7.2790-10 к классу «Г», обращение с которыми регулируется соответствующим законодательством [4]. Экологическая оценка этих устройств включает среди прочих показателей атмосферный выброс канцерогенных соединений, образующихся при термической обработке отходов.
Данная работа посвящена исследованию потенциальной канцерогенной опасности дымовых выбросов двух специализированных инсинераторов ЭЧУТО-150-03 и ЧЖБ-1 при утилизации просроченных лекарственных препаратов, поскольку ранее этот аспект проблемы охраны биосферы в отношении малотоннажных устройств никем не изучался.
Материалы и методы исследования
Инсинератор ЧЖБ-1 представляет собой печь открытого типа, имеющую комплекс устройств для очистки дымовых выбросов (рис. 1).
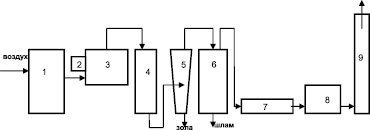
Рис. 1. Схема технологического процесса печи ЧЖБ-1: 1 – основная камера сгорания отходов; 2 – камера обезвреживания воды; 3 – камера высокотемпературного дожига; 4 – теплообменник; 5 – циклон типа ЦН; 6 – мокрый скруббер; 7 – дымосос; 8 – фильтр-улавливатель; 9 – труба дымовая
Отходы подаются в камеру сжигания, где идет горение с доступом кислорода (температура в камере 800–1000 °С); затем дымовые газы попадают в камеру, где при температуре 1200–1500 °С происходит дожиг несгоревших частиц и образовавшихся при горении газов. Время нахождения выбросов в камере дожига – несколько секунд. Камера дожига печи запатентована и является главной частью печи ЧЖБ [5]. В теплообменнике температура отходящих газов снижается до 300 °С. Циклон и мокрый скруббер очищают выбросы от частиц золы. Пройдя через дымосос и дополнительный фильтр, улавливающий остатки твердых частиц, дымовые газы через трубу выбрасываются в атмосферу.
ЭЧУТО-150.03
Современное устройство для экологически безопасной термической переработки небольших количеств отходов (до 50 кг в час) (рис. 2). Основной технологический принцип работы – непрямое двухступенчатое сжигание, включающее предварительное термическое разложение (пиролиз) органической части исходного сырья, сжигание газообразных продуктов с использованием выделяющегося тепла на поддержание процесса и дожиг коксового остатка. Температура пиролиза в реакторе 650 °С, температура дожига отходящих газов 1300–1400 °С. Все покидающие устройство продукты проходят через огневую зону, что в сочетании с дополнительными очистными устройствами должно обеспечивать экологически чистое уничтожение отходов [6, 7].
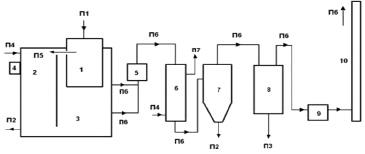
Рис. 2. Схема технологического процесса установки ЭЧУТО-150.03: 1 – термореактор; 2 – циклонная топка; 3 – топочное пространство; 4 – горелка; 5 – каталитический дожигатель; 6 – теплообменник; 7 – циклон; 8- скруббер; 9 – дымосос; 10 – труба дымовая. п1 – отходы; п2 – зола; п3 – шлам; п4 – воздух; п5 – ПГС; п6 – дымовые газы; п7 – теплосъём
Отбор проб и подготовка к физико-химическому анализу
На обеих установках сжигали по отдельности образцы просроченных лекарств трех типов; Антибиотики (ампициллина тригидрат – таблетки 250 мг); Противоопухолевые препараты (метотрексат таблетки 5 мг, уромитексан, 400 мг действующего вещества); Ферменты (панкреатин – таблетки 25 ед). Образцы сжигали вместе с упаковками (флаконы стеклянные и полипропиленовые, алюминий, коробки картонные), как это обычно делается на мусоросжигательных заводах. Отбор проб корпускулярной фракции дымовых выбросов из дымоходов ЧЖБ-1 и ЭЧУТО 150-03 производили на патрон с аэрозольным фильтром из ткани Петрянова АФА-ХА с использованием автоматического пробоотборника «ОП-442ТЦ».
В процессе сжигания проведено исследование содержания ПАУ в дымовых выбросах обеих установок, в воздухе рабочего помещения, а также в воздухе у основания трубы ЧЖБ-1. Отбор проводили на фильтры при скорости потока 10 л/мин. Для подготовки к спектральному и хроматографическому анализу на содержание ПАУ, а также для микробиологического метода исследования мутагенности, первичную экстракцию образцов проводили дихлорметаном. Качественный и количественный состав канцерогенных соединений в экстрактах определяли физико-химическими методами. Предварительно определяли содержание бенз(a)пирена (БП), как индикаторного вещества, характеризующего общий состав и концентрации остальных ПАУ. Для этого использовали стандартный метод, при котором экстракт, содержащий исследуемое соединение, разделяют с помощью тонкослойной хроматографии на окиси алюминия и выделяют фракцию, содержащую БП. Массовая концентрация бенз(а)пирена определяется путем измерения и последующего сравнения относительной интенсивности его аналитической линии в спектре люминесценции методом добавки при данной аналитической длине волны возбуждения люминесценции. Спектры люминесценции регистрируются фотоэлектрически при температуре жидкого азота (tкип = 77 °К) и возбуждении ультрафиолетовым излучением ртутно-кварцевой лампы [8]. Анализ ПАУ проводили на высокоэффективном жидкостном хроматографе YL9100 YPLC System с ультрафиолетовым детектором в градиентном режиме ацетонитрил:вода со скоростью потока 2 мл/мин. Для расчетов была проведена калибровка исследуемых соединений с использованием стандартной смеси веществ. Расчеты проводили с использованием программного обеспечения Clarity.
Определение мутагенности в бактериальном тесте Эймса
Потенциальную канцерогенность дымовых выбросов исследовали с помощью бактериального теста на мутагенную активность (тест Эймса – сальмонелла/микросомы), поскольку показателем потенциальной канцерогенности является способность соединения или смеси соединений вызывать мутации в наследственном аппарате клетки. Экстракты, которые использовались для физико-химического определения ПАУ, исследовали в соответствии с российским и международным стандартами [9–11]. Суть метода заключается в регистрации способности испытуемого соединения (смеси соединений в экстракте) и/или его метаболитов индуцировать генные мутации у индикаторных микроорганизмов в системе с метаболической активации in vitro. Были использованы индикаторные штаммы Salmonella typhimurium ТА100 и ТА98. Наличие мутагенного эффекта у исследуемых препаратов учитывали по индукции обратных мутаций от ауксотрофности по гистидину к прототрофности [12, 13]. Ввиду предполагаемого наличия в выбросах канцерогенов прямого и непрямого действия, была использована методика с активацией проканцерогенов микросомной фракцией клеток печени крысы (S9) и без активации смесью полихлорированных бифенилов [14].
Эксперимент сопровождали положительными контролями. В качестве позитивных контролей использовали вещества, индуцирующие мутации в клетках соответствующих штаммов-тестеров при наличии или отсутствии метаболической активации [15] Для вариантов без активирующей смеси нами был использован Азид натрия и 2,7-диамино-4,9диокси-5,10-диоксо-4,5,9,10-тетрагидро-4,9-диазапирен (ДДДТДП) активность фракции S9 контролировали мутагенами – БП и 2-ацетиламинофлуореном (ААФ) или аминофлуорен (АФ) для обоих штаммов – ТА98 и ТА100. В каждом контрольном и опытном варианте использовали по 3 чашки на дозу. Эксперимент повторяли дважды. Результаты учитывали при наличии мутагенного эффекта во всех вариантах позитивного контроля и нормальном фоновом уровне. Результаты экспериментов представлены в табл. 2–5. Во всех экспериментах статистическую обработку результатов проводили с использованием t-критерия Стьюдента для определения М ± m, где М – среднее значение, m – стандартное отклонение.
Результаты исследования и их обсуждение
Содержание канцерогенных ПАУ в экстрактах дымовых выбросов
В дымовых выбросах обеих установок определены 8 ПАУ (табл. 1). Содержание наиболее активного канцерогенного ПАУ бенз(а)пирена в дымовых выбросах ЧЖБ-1 и ЭЧУТО 150-03 на 2–3 порядка ниже, чем при неорганизованном открытом сжигании отходов, выполненном в предыдущих экспериментах. При этом содержание бенз(а)пирена в выбросах установки ЭЧУТО 150-03 было ниже в сравнении с выбросом ЧЖБ-1. В то же время по сравнению с ЭЧУТО 150-03, ЧЖБ-1 выбрасывал меньше слабых канцерогенов – бенз(а)антрацена и дибенз(a,h)антрацена, а также пирена, прекурсора канцерогенных нитропиренов.
Таблица 1
Содержание ПАУ в дымовых выбросах при сжигании отходов в ЧЖБ-1 без пиролиза и в ЭЧУТО 150-03 с пиролизом в мкг/м3
|
Концентрация ПАУ, мкг/м3 |
||||||||||
|
№ п/п |
ПАУ |
Антибиотики |
Противоопухолевые препараты |
Ферменты |
Воздух рабочей зоны |
Атмосферный воздух* |
Открытое сжигание** |
|||
|
ЧЖБ-1 |
ЭЧУТО |
ЧЖБ-1 |
ЭЧУТО |
ЧЖБ-1 |
ЭЧУТО |
|||||
|
1 |
Фенантрен |
120 |
126 |
66 |
63 |
143 |
156 |
28 |
32 |
|
|
2 |
Флуорантен |
6 |
51 |
н.и |
н.и. |
н.и. |
36 |
4,2 |
н.и. |
|
|
3 |
Пирен |
252 |
420 |
129 |
186 |
207 |
360 |
48 |
33 |
|
|
4 |
Бенз(а)-антрацен |
28 |
54 |
14 |
27 |
20 |
51 |
н.и. |
н.и. |
2420 |
|
5 |
Хризен |
30 |
36,9 |
13 |
10,5 |
15 |
27 |
0,98 |
0,90 |
|
|
6 |
Бенз(b)-флуорантен |
23 |
32,1 |
15 |
12 |
12 |
18 |
н.и. |
н.и. |
2707 |
|
7 |
Бенз(а)пирен |
6,1 |
0,6 |
2,7 |
0,84 |
3,1 |
0,72 |
0,18 |
0,09 |
2210 |
|
8 |
Дибенз(a,h)-антрацен |
7 |
18 |
9 |
15 |
13 |
24 |
н.и. |
7,8 |
197,6 |
Примечание. н.и. – не идентифицировано.
*замер у основания дымовой трубы.
**результаты сжигания твердых смешанных отходов из предыдущих исследований [16].
Поскольку утилизация антибиотиков, противоопухолевых препаратов и ферментов производилась вместе с упаковками, мы не можем отнести различия в содержании канцерогенов в их дыме к самим препаратам и утверждать, как это видно из табл. 1, что при сгорании противоопухолевых антибиотиков образуется меньше канцерогенных углеводородов, чем при сжигании антибиотиков и ферментов. В то же время можем констатировать, что в воздухе рабочей зоны и в атмосферном воздухе непосредственно у основания дымовой трубы значения концентрации БП соответствовали ПДК воздуха рабочей зоны – 150 нг/м3 [17].
Результаты биологических экспериментов
В представленных табл. 2–5 даны результаты двух повторных опытов определения мутагенной активности экстракта корпускулярной фазы дымового выброса. В каждом представлен естественный фон мутагенеза, позитивные контроли с использованием стандартных мутагенов и результаты исследований в вариантах с микросомальной активирующей смесью (+S9) и без нее (–S9). Активность каждой дозы экстракта представлена в виде средних значений от подсчета числа колоний ревертантов в трех чашках. В фоновом варианте частота индуцируемых мутаций не превышала стандартный уровень, соответствующий генетическим особенностям штаммов ТА100 и ТА98, а варианты позитивного контроля показали хорошую активность фракции S9, при которой промутагены ААФ, АФ и БП индуцировали высокий уровень реверсий. Высокая специфичность ответа на действие прямых мутагенов была подтверждена испытаниями штамма ТА98 с ДДДТДП (индуктор мутаций сдвига рамки считывания) и штамма ТА100 с азидом натрия (индукция мутаций замены пар оснований). Из этих данных следует, что, система тестирования (тест Эймса) соответствует стандартным параметрам.
Табл. 2 содержит данные, полученные при определении мутагенности выброса ЭЧУТО 150-03на штамме Salmonella typhimurium TA100, чувствительном к мутагенам, индуцирующим мутации типа замены пар оснований, а табл. 3 такого же рода данные, полученные при анализе выброса ЧЖБ-1. Общим результатом для обоих инсинераторов была предельно низкая мутагенность экстрактов их дымового выброса.
При сжигании в установке ЭЧУТО 150-03 антибиотиков и ферментов слабая активность была отмечена на обоих штаммах только при использовании предельно высоких концентраций экстракта без активации смесью S9, что говорит о наличии в дымовых частицах небольшого количества мутагенов прямого действия (табл. 2, 4).
При сжигании в ЧЖБ-1 мутагенная активность дымовых выбросов не проявлялась на обоих штаммах ни с активацией S9, ни без нее (табл. 3, 5). На штамме ТА98 (табл. 5) небольшой мутагенный эффект в отсутствии S9 был зарегистрирован только в экстракте дыма от сжигания ферментов, что так же, как и при использовании установки ЭЧУТО 150-03, говорит о наличии в выбросе прямых мутагенов.
Таблица 2
Действие экстракта дымовых выбросов установки ЭЧУТО 150-03 на индикаторный штамм бактерий ТА100
|
Исследуемое вещество |
Доза |
Штамм ТА 100 |
|||||||
|
–S9 |
+S9 |
||||||||
|
мкг/чашка |
M ± m |
Mi/Mo |
MA |
M ± m |
Mi/Mo |
MA |
|||
|
Контроль фона |
0 |
28 ± 0,9 37 ± 3,1 |
1,0 1,0 |
– – |
37 ± 3,6 47 ± 8,9 |
1,0 1,0 |
– – |
||
|
БП |
4,4 |
243 ± 15,6 263 ± 5,6 |
6,6 5,6 |
+ + |
|||||
|
ААФ |
22 |
237 ± 21,8 313 ± 18,2 |
6,4 6,7 |
+ + |
|||||
|
Окончание табл. 2 |
|||||||||
|
Исследуемое вещество |
Доза |
Штамм ТА 100 |
|||||||
|
–S9 |
+S9 |
||||||||
|
мкг/чашка |
M ± m |
Mi/Mo |
MA |
M ± m |
Mi/Mo |
MA |
|||
|
Азид натрия |
8,8 |
416 ± 14,5 384 ± 17,5 |
14,9 10,4 |
+ + |
|||||
|
л/чашка* |
|||||||||
|
Антибиотики |
0,0118 |
23 ± 3,6 35 ± 5,1 |
0,8 0,9 |
– – |
32 ± 2,4 41 ± 4,0 |
0,9 0,9 |
– – |
||
|
0,118 |
32 ± 3,3 42 ± 3,6 |
1,1 1,1 |
– – |
54 ± 4,9 47 ± 2,0 |
1,5 1,0 |
– – |
|||
|
0,59 |
47 ± 3,6 57 ± 3,8 |
1,7 1,5 |
– – |
68 ± 13,3 71 ± 3,8 |
1,8 1,5 |
– – |
|||
|
1,18 |
92 ± 9,0 115 ± 10,4 |
3,3 3,1 |
+ + |
72 ± 16,7 91 ± 2,9 |
1,9 1,9 |
– – |
|||
|
Ферменты |
0,0118 |
19 ± 2,2 35 ± 6,7 |
0,7 0,9 |
– – |
43 ± 4,2 48 ± 2,4 |
1,2 1,0 |
– – |
||
|
0,118 |
36 ± 0,7 38 ± 2,9 |
1,3 1,0 |
– – |
42 ± 1,1 44 ± 2,9 |
1,1 0,9 |
– – |
|||
|
0,59 |
37 ± 17,1 49 ± 3,6 |
1,3 1,8 |
– – |
55 ± 6,0 43 ± 7,8 |
1,5 1,2 |
– – |
|||
|
0,0118 |
93 ± 7,3 62 ± 4,2 |
3,3 1,7 |
+ – |
53 ± 2,9 58 ± 6,0 |
1,4 1,2 |
– – |
|||
|
Онкопрепараты |
0,0118 |
22 ± 1,3 38 ± 1,6 |
0,8 1,0 |
– – |
42 ± 3,8 45 ± 2,7 |
1,1 1,0 |
– – |
||
|
0,118 |
36 ± 6,2 37 ± 0,4 |
1,3 1,0 |
– – |
43 ± 4,0 48 ± 3,6 |
1,2 1,0 |
– – |
|||
|
0,59 |
49 ± 3,6 53 ± 1,1 |
1,8 1,4 |
– – |
43 ± 7,8 54 ± 3,8 |
1,2 1,1 |
– – |
|||
|
1,18 |
60 ± 6,7 83 ± 12,4 |
2,1 2,2 |
– – |
68 ± 12,9 60 ± 2,7 |
1,8 1,3 |
– – |
|||
Примечание. Результаты эксперимента № 1 даны в верхней строке прямым шрифтом, результаты повторного – курсивом в нижней строке.
Обозначения к табл. 2–5:
*л/чашка – доза на чашку в пересчете на 1 л выброса.
Mi/Mo – отношение числа ревертантов в опыте к числу ревертантов в контроле.
МА – мутагенная активность препарата.
«+» означает наличие, а « – » отсутствие мутагенной активности.
*н.р. – неразведенный экстракт, соответствует 1,18 литров дымового выброса на чашку.
Таблица 3
Действие экстракта дымовых выбросов ЧЖБ-1 на индикаторный штамм бактерий ТА100
|
Исследуемое вещество |
Доза |
Штамм ТА 100 |
|||||
|
–S9 |
+S9 |
||||||
|
мкг/чашка |
M ± m |
Mi/Mo |
MA |
M ± m |
Mi/Mo |
MA |
|
|
Контроль фона |
0 |
59 ± 4,0 60 ± 9,1 |
1,0 1,0 |
– – |
55 ± 4,0 64 ± 8,2 |
1,0 1,0 |
– – |
|
БП |
4,4 |
293 ± 40,4 338 ± 31,8 |
5,3 5,3 |
+ + |
|||
|
АФ |
8,8 |
253 ± 18,2 240 ± 33,1 |
4,6 3,8 |
+ + |
|||
|
Азид натрия |
8,8 |
389 ± 15,3 720 ± 40,0 |
6,6 12,0 |
+ + |
|||
|
л/чашка* |
|||||||
|
Окончание табл. 3 |
|||||||
|
Исследуемое вещество |
Доза |
Штамм ТА 100 |
|||||
|
–S9 |
+S9 |
||||||
|
мкг/чашка |
M ± m |
Mi/Mo |
MA |
M ± m |
Mi/Mo |
MA |
|
|
Антибиотики |
0,0118 |
58 ± 4,7 55 ± 4,0 |
1,0 0,9 |
– – |
52 ± 2,9 41 ± 4,0 |
0,9 0,6 |
– – |
|
0,118 |
68 ± 1,1 60 ± 2,2 |
1,2 1,0 |
– – |
52 ± 3,8 47 ± 2,0 |
0,9 0,7 |
– – |
|
|
0,59 |
59 ± 7,8 52 ± 2,2 |
1,0 0,9 |
– – |
57 ± 4,4 71 ± 3,8 |
1,0 1,1 |
– – |
|
|
1,18 |
65 ± 3,8 56 ± 10,2 |
1,1 0,9 |
– – |
63 ± 4,2 72 ± 10,2 |
1,1 1,1 |
– – |
|
|
Ферменты |
0,0118 |
55 ± 16,9 55 ± 4,0 |
0,9 0,9 |
– – |
50 ± 6,9 45 ± 2,7 |
0,9 0,7 |
– – |
|
0,118 |
71 ± 5,3 56 ± 1,6 |
1,2 0,9 |
– – |
59 ± 1,5 48 ± 3,6 |
1,1 0,8 |
– – |
|
|
0,59 |
77 ± 1,5 65 ± 2,0 |
1,3 1,1 |
– – |
54 ± 2,2 54 ± 3,8 |
1,0 0,8 |
– – |
|
|
1,18 |
106 ± 5,6 84 ± 9,6 |
1,8 1,4 |
– – |
71 ± 5,1 72 ± 12,7 |
1,3 1,1 |
– – |
|
|
Онкопрепараты |
0,0118 |
57 ± 4,2 64 ± 2,0 |
1,0 1,1 |
– – |
58 ± 6,7 48 ± 2,4 |
1,1 0,8 |
– – |
|
0,118 |
52 ± 9,3 58 ± 2,7 |
0,9 1,0 |
– – |
54 ± 6,9 44 ± 2,9 |
1,0 0,7 |
– – |
|
|
0,59 |
58 ± 3,1 59 ± 4,2 |
1,0 1,0 |
60 ± 2,0 49 ± 4,2 |
1,1 0,8 |
– – |
||
|
1,18 |
70 ± 10,2 71 ± 5,1 |
1,2 1,0 |
– – |
67 ± 2,2 66 ± 10,0 |
1,2 1,0 |
– – |
|
Примечание. Результаты эксперимента № 1 даны в верхней строке прямым шрифтом, результаты повторного – курсивом в нижней строке.
Таблица 4
Действие экстракта дымовых выбросов установки ЭЧУТО 150-03 на индикаторный штамм бактерий ТА98
|
Исследуемое вещество |
Доза |
Штамм ТА 98 |
|||||
|
–S9 |
+S9 |
||||||
|
мкг/чашка |
M ± m |
Mi/Mo |
MA |
M ± m |
Mi/Mo |
MA |
|
|
Контроль фона |
0 |
10 ± 1,3 10 ± 0,9 |
1,0 1,0 |
– – |
11 ± 2,0 8 ± 0,7 |
1,0 1,0 |
– – |
|
БП |
4,4 |
46 ± 6,2 43 ± 4,4 |
4,2 5,4 |
+ + |
|||
|
ААФ |
22 |
63 ± 5,7 86 ± 10,7 |
5,7 10,8 |
+ + |
|||
|
ДДДТДП |
8,8 |
242 ± 21,1 307 ± 11,1 |
24,2 30,7 |
+ + |
|||
|
л/чашка* |
|||||||
|
Антибиотики |
0,0118 |
12 ± 2,2 10 ± 1,0 |
1,2 1,0 |
– – |
11 ± 1,3 8 ± 1,3 |
1,0 1,0 |
– – |
|
0,118 |
19 ± 3,6 9 ± 2,2 |
1,9 0,9 |
– – |
11 ± 3,6 7 ± 2,0 |
1,0 0,9 |
– – |
|
|
0,59 |
37 ± 6,0 14 ± 4,4 |
3,7 1,4 |
+ – |
19 ± 3,5 13 ± 1,8 |
1,7 1,6 |
– – |
|
|
1,18 |
58 ± 3,3 31 ± 2,0 |
5,8 3,1 |
+ + |
35 ± 4,2 28 ± 2,4 |
3,2 3,5 |
+ + |
|
|
Окончание табл. 4 |
|||||||
|
Исследуемое вещество |
Доза |
Штамм ТА 98 |
|||||
|
–S9 |
+S9 |
||||||
|
мкг/чашка |
M ± m |
Mi/Mo |
MA |
M ± m |
Mi/Mo |
MA |
|
|
Ферменты |
0,0118 |
10 ± 0,4 12 ± 0,9 |
1,0 1,2 |
– – |
12 ± 2,0 28 ± 2,4 |
1,1 0,9 |
– – |
|
0,118 |
14 ± 2,0 9 ± 1,1 |
1,4 0,9 |
– – |
11 ± 3,6 10 ± 2,0 |
1,0 1,3 |
– – |
|
|
0,59 |
24 ± 2,2 17 ± 0,9 |
2,4 1,7 |
+ – |
15 ± 1,0 11 ± 2,2 |
1,4 1,4 |
– – |
|
|
1,18 |
37 ± 1,8 26 ± 1,6 |
3,7 2,6 |
+ + |
20 ± 7,1 11 ± 2,5 |
1,8 1,4 |
– – |
|
|
Онкопрепараты |
0,0118 |
10 ± 0,9 11 ± 1,5 |
1,0 1,1 |
– – |
10 ± 1,0 7 ± 0,7 |
0,9 0,9 |
– – |
|
0,118 |
14 ± 1,3 11 ± 0,5 |
1,4 1,1 |
– – |
14 ± 1,5 9 ± 1,1 |
1,3 1,1 |
– – |
|
|
0,59 |
26 ± 1,8 14 ± 3,0 |
2,6 1,4 |
+ – |
16 ± 6,5 15 ± 2,19 |
1,5 1,9 |
– – |
|
|
1,18 |
38 ± 1,8 15 ± 2,4 |
3,8 1,5 |
+ – |
18 ± 0,7 14 ± 2,4 |
1,6 1,8 |
– – |
|
Примечание. Результаты эксперимента № 1 даны в верхней строке прямым шрифтом, результаты повторного – курсивом в нижней строке.
Таблица 5
Действие экстракта дымовых выбросов ЧЖБ-1 на индикаторный штамм бактерий ТА98
|
Исследуемое вещество |
Доза |
Штамм ТА 98 |
|||||
|
–S9 |
+S9 |
||||||
|
мкг/чашка |
M ± m |
Mi/Mo |
MA |
M ± m |
Mi/Mo |
MA |
|
|
Контроль фона |
0 |
11 ± 2,2 8 ± 1,3 |
1,0 1,0 |
– – |
15 ± 2,9 14 ± 0,9 |
1,0 1,0 |
– – |
|
БП |
4,4 |
173 ± 7,6 153 ± 18,2 |
11,5 10,9 |
+ + |
|||
|
АФ |
8,8 |
193 ± 10,2 212 ± 7,6 |
12,9 15,1 |
+ + |
|||
|
ДДДТДП |
8,8 |
193 ± 18,2 154 ± 6,2 |
17,5 19,3 |
+ + |
|||
|
л/чашка* |
|||||||
|
Антибиотики |
0,0118 |
10 ± 1,6 10 ± 1,0 |
0,9 1,3 |
– – |
12 ± 1,8 11 ± 2,7 |
0,8 0,8 |
– – |
|
0,118 |
11 ± 0,4 9 ± 2,2 |
1,0 1,1 |
– – |
13 ± 1,8 13 ± 3,6 |
0,9 0,9 |
– – |
|
|
0,59 |
13 ± 4,2 11 ± 2,0 |
1,2 1,4 |
– – |
15 ± 1,1 13 ± 1,8 |
1,0 0,9 |
– – |
|
|
1,18 |
14 ± 1,1 9 ± 2,0 |
1,3 1,1 |
– – |
14 ± 2,0 15 ± 1,1 |
0,9 1,1 |
– – |
|
|
Ферменты |
0,0118 |
10 ± 2,7 9 ± 1,8 |
0,9 1,1 |
– – |
15 ± 2,4 12 ± 2,9 |
1,0 0,9 |
– – |
|
0,118 |
14 ± 2,0 9 ± 2,0 |
1,3 1,1 |
– – |
15 ± 2,0 11 ± 2,0 |
1,0 0,8 |
– – |
|
|
0,59 |
23 ± 1,8 9 ± 1,1 |
2,1 1,1 |
– – |
13 ± 1,8 15 ± 2,9 |
0,9 1,1 |
– – |
|
|
1,18 |
33 ± 4,7 20 ± 2,2 |
3,0 2,5 |
+ + |
17 ± 2,9 16 ± 5,8 |
1,1 1,1 |
– – |
|
|
Окончание табл. 5 |
|||||||
|
Исследуемое вещество |
Доза |
Штамм ТА 98 |
|||||
|
–S9 |
+S9 |
||||||
|
мкг/чашка |
M ± m |
Mi/Mo |
MA |
M ± m |
Mi/Mo |
MA |
|
|
Онкопрепараты |
0,0118 |
9 ± 1,6 9 ± 1,6 |
1,1 1,1 |
– – |
15 ± 3,5 13 ± 2,2 |
1,0 0,9 |
– – |
|
0,118 |
11 ± 1,1 9 ± 1,1 |
1,0 1,1 |
– – |
14 ± 2,2 16 ± 2,2 |
0,9 1,1 |
– – |
|
|
0,59 |
14 ± 2,2 8 ± 1,1 |
1,3 1,0 |
– – |
14 ± 3,3 14 ± 2,7 |
0,9 1,0 |
– – |
|
|
1,18 |
13 ± 5,6 9 ± 3,1 |
1,2 1,1 |
– – |
15 ± 0,4 15 ± 2,0 |
1,0 1,1 |
– – |
|
Примечание. Результаты эксперимента № 1 даны в верхней строке прямым шрифтом, результаты повторного – курсивом в нижней строке.
Ранее нами было показано, что реальная оценка генотоксической опасности продуктов термической переработки отходов возможна только при сочетании физико-химических и биологических методов. В частности, было найдено, что низкое содержание в выбросе отдельных канцерогенов не может служить показателем его мутагенной и канцерогенной безопасности, поскольку экстракты дыма, содержавшие бенз(а)пирен и бензфлуорантен в количестве на порядок ниже минимально мутагенного при изолированном применении, вызывали реверсии сальмонеллы в тесте Эймса. Кроме того, они разобщали межклеточные контакты в культуре клеток млекопитающих, что свидетельствовало о наличии в них промоторов, т.е. соединений, способных стимулировать независимый рост трансформированных клонов [18]. В связи с этим в данном исследовании физико-химические и биологические методы оценки потенциальной канцерогенности продуктов сжигания лекарств использовались параллельно.
Изучение канцерогенной безопасности работы установки ЭЧУТО 150-03 показало, что ее дымовой выброс при сжигании пластмассовых отходов биомедицинского назначения в беспиролизном режиме содержит в несколько раз меньшие концентрации канцерогенных углеводородов, чем при открытом сжигании, а включение пиролиза дополнительно уменьшает их еще на один-два порядка, приближая к ПДК в воздухе рабочей зоны. Соответственно уменьшалась и мутагенность экстрактов дыма [18]. В связи с этим мы использовали установку ЭЧУТО 150-03 в качестве контрольной для сравнения с ЧЖБ-1, ранее не изученной в этом плане.
Температуры термического разложения различных лекарственных препаратов при их переработке без упаковок исследовались рядом зарубежных авторов с использованием портативной установки (PGWTS – Pyrolysis–gasification waste treatment system), перерабатывающей за 3–4 часа путем пиролиза и газификации при температуре 550–700 °С до 16 кг медицинских отходов, в том числе лекарственных препаратов. Результаты их исследований приведены в табл. 6, из которой видно, что большинство исследованных лекарств разлагается в интервале 250–400 °С и только два из них – хлорамфеникол и сульфометаксазол – требуют более высокой температуры [3]. Авторы определяли остаток неизмененного препарата и его метаболиты, но ни в одном случае не поднимался вопрос о возможной мутагенности и канцерогенности атмосферного выброса. В установках ЧЖБ-1 и ЭЧУТО150-03 лекарства перерабатывались при значительно более высокой температуре при пиролизе, сжигании и дожигании, что должно было обеспечить полное их разложение.
Таблица 6
Температура разложения лекарственных препаратов в установке PGWTS [3]
|
Название* |
Фармакологическая группа |
Температура распада, °С |
|
5-фторурацил |
Противоопухолевый цитостатик |
282 |
|
Аллопуринол |
Ингибитор синтеза мочевой кислоты |
379–386 |
|
Амантадин |
Противовирусный и антипаркинсонический препарат |
360 |
|
Аспирин |
Аналгетик |
370 |
|
Атенолол |
Бэта-блокатор |
303–335 |
|
Карбамазепин |
Противоэпилептический препарат |
190–195 |
|
Хлорамфеникол |
Синтетический антибиотик |
200–704 |
|
Диклофенак |
Нестероидный противовоспалительный препарат |
>260 |
|
Эстрадиол |
Эстроген |
275–317 |
|
Этинилэстрадиол |
Эстроген |
178 |
|
Флуоксетин |
Антидепрессант |
200–300 |
|
Гликлазид |
Гипогликемический препарат |
271–429 |
|
Ибупрофен |
Нестероидный противовоспалительный препарат |
180–300 |
|
Индометацин |
Нестероидный противовоспалительный препарат |
330–430 |
|
Кетопрофен |
Нестероидный противовоспалительный препарат |
2 35–400 |
|
Сульфометаксазол |
Сульфаниламид |
380–600 |
|
Верапамил |
Блокатор кальциевых каналов |
300–320 |
Примечание. *Препараты сжигались без упаковок.
Опыт небольших британских медицинских и фармацевтических учреждений, для которых компания PyropureLtd разработала портативную печь PGWTS, показал рентабельность использования подобных устройств не только с экологической, но и с экономической точек зрения. Затраты на приобретение PGWTS окупались примерно в течение года за счет 95 % экономии средств, связанных с транспортировкой и платой за утилизацию отходов на мусоросжигающих заводах [3].
Наше исследование продемонстрировало относительную канцерогенную безопасность сжигания трех категорий просроченных лекарств в малотоннажных инсинераторах ЭЧУТО 150-03 и ЧЖБ-1. Хотя антибиотики, ферменты и противоопухолевые препараты сжигались по отдельности, охарактеризовать их специфический вклад в образование бластомогенных продуктов не представляется возможным, поскольку они перерабатывались вместе с блистерными упаковками, которые помимо подложки из картона или алюминиевой фольги изготавливаются из формованного пластика различного происхождения: поливинилхлорида, полистирола, полипропилена, полиэтилена, полиэтилентерефталата, ацетата целлюлозы и других пластиков. Эти пластики, особенно поливинилхлорид, при сгорании могут давать генотоксические соединения [16, 19, 20]. Несмотря на это, содержание канцерогенных ПАУ в дымовых выбросах обеих установок было невелико. Расчет с использованием полученных данных позволит определить приемлемую границу санитарно-защитной зоны, за пределами которой количество вредных, в том числе канцерогенных, составляющих будет снижено до ПДК содержания бенз(а)пирена в атмосферном воздухе населенных мест, установленной Постановлением Главного государственного санитарного врача РФ на уровне 1.10-6 мг/м3 [21].
Мутагенность экстрактов дымовых выбросов ЭЧУТО 150-03 была минимальной и определялась лишь в концентрированных экстрактах частиц. В выбросах ЧЖБ-1 мутагенная активность выбросов была аналогичной и тоже выявлялась в экспериментах без активации метаболизирующей фракцией S9. Это говорит о том, что мутации вызывали не ПАУ, превращающиеся в активные электрофилы (эпоксиды, диолэпоксиды, хиноны и др.) с помощью микросомной монооксигеназной фракции, а мутагены прямого действия, не определяемые использованными физико-химическими методами.
Поскольку количество канцерогенных соединений и уровень мутагенной активности выбросов от сжигания использованных групп препаратов вместе с упаковками не отличались от показателей, полученных ранее при переработке других биомедицинских отходов, можно считать, что собственный вклад лекарств в эти показатели потенциальной канцерогенности был незначительным.
Заключение
В целом уровень содержания канцерогенных ПАУ в выбросах ЭЧУТО 150-03 и ЧЖБ-1, а также генотоксичность выбросов снижены на порядки по сравнению с неорганизованным открытым сжиганием. Содержание бенз(а)пирена в воздухе рабочей зоны и в непосредственной близости к дымовой трубе соответствует ПДК, что позволяет рассчитать границы санитарно-защитной зоны. Полученные данные дают основание считать инсинераторы ЭЧУТО 150-03 и ЧЖБ-1 пригодными для уничтожения медицинских отходов типа «Г», аналогичных изученным в данном исследовании. Возможность использования данных установок для утилизации других типов лекарственных препаратов подлежит дальнейшему исследованию.
Библиографическая ссылка
Кривошеева Л.В., Хитрово И.А., Кирсанов К.И., Белицкий Г.А., Иванов А.А., Якубовская М.Г., Гафурова Н.А., Полянина В.Л., Аствацатуров А.Г., Старников М.А. КАНЦЕРОГЕННЫЕ ВЫБРОСЫ ПРИ ТЕРМИЧЕСКОЙ ПЕРЕРАБОТКЕ ПРОСРОЧЕННЫХ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ // Международный журнал прикладных и фундаментальных исследований. 2019. № 3. С. 28-38;URL: https://applied-research.ru/ru/article/view?id=12679 (дата обращения: 22.05.2026).
DOI: https://doi.org/10.17513/mjpfi.12679

